Eliminaatioreaktio
On orgaaninen kemia , poistaminen (tai β-eliminaatio ) on orgaaninen reaktio mikä muuttuu substituoitu alkaani ( halogeenialkaanit , alkoholit, jne.) Osaksi eteenin johdannainen, tai jopa osaksi aikeeni , jos lähtöaineena molekyyli, lisäksi poistuva ryhmä , n 'on vain alkaanityyppinen hiiliketju.
Edellytykset ovat ankarien lisäksi nukleofiilisen substituution olosuhteet , monessa suhteessa samanlainen ja samanaikainen reaktio: eliminaatio tapahtuu vahvan emäksen läsnä ollessa ja kuumentamalla reaktioseosta.
Yleinen yhtälö
Yksi tärkeimmistä esimerkkejä poistaminen on muuntaminen halogeenialkaanin on alkeeni ; sitten puhumme dehydrohalogenoinnista :
Yleisimmin käytettyjä emäksiä ovat sooda (Na + , HO - ), potaskaa (K + , HO - ), tai jopa alkoholaatin ioneja (RO - ) (saatu saattamalla natrium käytettäessä alkoholi ROH, vedetön ).
Aivan kuten nukleofiilisen substituution kohdalla, on olemassa monomolekulaarinen eliminaatio ja bimolekyylinen eliminaatio, jotka on yleisesti merkitty vastaavasti E1: ksi ja E2: ksi.
Tämän artikkelin loppuosassa esimerkit annetaan halogenoidun johdannaisen reagenssina.
Monomolekulaarinen eliminaatio
E1-kinetiikka
Yksimolekyylinen eliminointireaktio suoritetaan kahdessa vaiheessa: yksimolekyylinen vaihe, johon reagenssipuolella osallistuu vain halogenoidun johdannaisen molekyyli, joka on kineettisesti rajoittava vaihe, jota seuraa bimolekyylivaihe. Näin ollen reaktion kinetiikka riippuu kinetiikkaa määrittävän (tai rajoittavan ) vaiheen likiarvosta vain lajin RX konsentraatiosta.
Siksi reaktiolle on ominaista kokonaisjärjestyksen 1, osaluokkien 1 kinetiikka halogenoidun johdannaisen ja 0 suhteen emäksen B suhteen | : v = k. [RX] , jossa:
- [RX] edustaa halogenoidun johdannaisen pitoisuutta mol.L- 1: ssä
- v edustaa eliminaatioreaktion nopeutta. Se ilmaistaan mol.s −1 .
- k on nopeusvakio: se on itse asiassa, että kineettisesti rajoittava vaihe (k 1 ). Sen yksikkö, Ls −1 , johdetaan kahdesta muusta termistä.
E1: n mekanismi
Reaktio tapahtuu kahdessa vaiheessa.
- Ensimmäinen vaihe: nukleofugin lähtö, karbokation muodostuminen. tämä karbokationinmuodostusvaihe on hidas, palautuva vaihe ja asettaa nopeutensa koko reaktiolle.
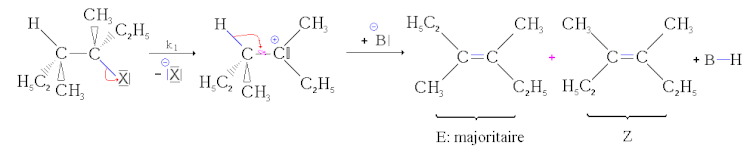
- Toinen vaihe: happo-emäs-reaktio. Pohja repii protonin. Sitten dubletti "taittuu" hiili-hiilisidoksen päälle kaksoissidoksen muodostamiseksi . Koska hiili-hiili-sidos voi pyöriä, voi muodostua kaksi stereoisomeeriä. Koska tämä reaktio on paljon nopeampi kuin edellinen, sen nopeus ei vaikuta kokonaisnopeuteen.

Stereoselektiivisyys ja regioselektiivisyys
StereokemiaKuten mekanismi osoittaa, läpikulku karbokationin kautta, joka on tasomainen rakenne, poistaa kaikki stereospesifisyyden elementit, toisin kuin (katso seuraava) bimolekyylin eliminaation mekanismi.
Mutta jos voi muodostua kaksi geometrista stereoisomeeriä, ne eivät muodostu samoissa suhteissa. Vakain isomeeri, toisin sanoen se, jolla on pienin energia, muodostuu pääasiassa (tämä on Zaitsevin sääntö). Siksi E-isomeeri muodostuu pääasiassa ilman mesomeeria. Toisaalta, jos vain yhden näistä kahdesta tuotteesta kaksoissidos voidaan sijoittaa mesomeerisesti, niin tämä muodostuu pääasiassa. Tätä kutsutaan osittaiseksi stereoselektiivisyydeksi.
 Regiokemia
Regiokemia
Kun useita perustuslaillisia isomeerejä voidaan muodostaa, muodostuu ensisijaisesti termodynaamisesti vakain alkeeni. Jos on vain alkyyliryhmiä, tämä on eniten substituoitu alkeeni. Jos mesomeria voi puuttua asiaan, se on konjugoitua alkeenia, joka on enemmistössä. Tätä kutsutaan regioselektiivisyydeksi tai Zaïtsevin säännöksi .
Kuitenkin joskus termodynaamisesti vähemmän vakaa alkeeni muodostuu ensisijaisesti, tähän viitataan Hofmannin eliminaationa . Tämä pätee erityisesti silloin, kun käytetty emäs on ruuhkainen (esim. KtBuO) tai kun on ammoniumionia, joka esimerkiksi eliminoituu. (Molekyyli, joka kuljettaa amiinia MeI: n läsnä ollessa monissa ekvivalenteissa, jotka ovat riittäviä ammoniumsuolan muodostamiseksi, ja sitten se asetetaan märän ja kuumennetun hopeaoksidin läsnäollessa . Alkaanin muodostuminen poistamalla Hofmann ja siten poistamalla. N (Me) ) 3.)
Vasteeseen vaikuttavat tekijät
E1-eliminaatioon vaikuttavat parametrit ovat:
- R- vaikutus: kineettisesti määrittelevä vaihe on karbokationin muodostuminen (eikä sen reaktiivisuus), joten mitä enemmän se on stabiili, sitä enemmän reaktiota suositaan.
- nukleofuge: C-poistuvan ryhmäsidoksen katkaisu on mekanismin avainvaihe, reaktio riippuu voimakkaasti tämän nukleofugen luonteesta. Mitä parempi lähtöryhmä, sitä nopeampi reaktio. Esimerkiksi alkoholien dehydratoimiseksi ensimmäinen vaihe on alkoholin protonointi oksoniumin muodostamiseksi ja siten parempi poistuva ryhmä (H 2 O⇒HO - ). Nopea lähtöryhmien sijoitus olisi:
(merkki ">" tarkoittaa: "paras lähtöryhmä kuin")
Huomaa, että emäs ei vaikuta tämän tyyppiseen järjestyksen 1 reaktioon, ja siltä osin kuin se ei puutu ensimmäisen vaiheen aikana, joka määrittää reaktion kokonaisnopeuden.
Halogeenijohdannaisen alkyyliryhmäMekanismi kulkee karbokationityyppisen reaktion välituotteen läpi. Jälkimmäinen on sitä vakaampi, mitä enemmän se korvataan. Siten reaktionopeus (siis karbokationin muodostumisen vuoksi) etenee primaarisista johdannaisista toissijaisiin ja sitten tertiäärisiin. Käytännössä vain jälkimmäiset ja muutamat sekundaariset johdannaiset reagoivat tällä mekanismilla.
NucleofugeMitä polarisoituvampi RX-linkki on, sitä helpompi on katkaista. Tämä sidos on siis heikkenevää labiliteettia ("haurautta") fluorista jodiin: F> Cl> Br> I.
(symboli ">" tarkoittaa: "nopeampi kuin")
Liuotin- Polariteetti: polaarinen liuotin stabiloi karbokationin; se tekee siten ensimmäisen reaktion helpommaksi. Siksi nopeus kasvaa liuottimen polaarisuuden myötä.
- Protikaatio: proottinen liuotin on enemmän haitta: se todellakin voi kilpailla karbokationin kanssa (vahvan) happo-emäs-reaktion aikana.
Kilpailu
Tämä reaktio ei ainoastaan kilpailee muiden poistamista, mutta myös reaktioiden kanssa nukleofiilisen substituutioita, erityisesti S- N 1 . Jälkimmäinen tapahtuu itse asiassa samankaltaisissa olosuhteissa (lämmityksen lisäksi).
Bimolekulaarinen eliminaatio
Kineettinen
Bimolekulaarisella eliminointireaktiolla on globaalin kertaluvun 2 ja osittaisen kertaluvun 1 kinetiikka suhteessa halogenoituun johdannaiseen RX ja emäkseen B: - . Reaktio tapahtuu yhdessä kaksimolekyylisessä vaiheessa, minkä vuoksi reaktion nopeus noudattaa tyyppilakia: v = k. [RX]. [B: - ] .
tai:
- [RX] edustaa halogenoidun johdannaisen pitoisuutta (ilmaistuna moolina L -1)
- [B: - ] edustaa emäskonsentraatiota (ilmaistuna moolina L- 1 )
- v edustaa eliminaatioreaktion nopeutta. Se ilmaistaan mol.s −1 .
- k on nopeusvakio. Sen yksikkö, Ls −1 .mol −1 , johdetaan kahden muun termin yksiköistä .
E2: n mekanismi
Bimolekulaarinen eliminaatio on kaksivaiheinen kaksivaiheinen reaktio.
Saman alkeisvaiheen aikana tapahtuu protonin repeämä emäksen kautta, kaksoissidoksen muodostuminen ja halogeeniatomin (nukleofugen) lähtö halogenidi-ionin muodossa. Puhumme synkronisesta tai yhteensovitetusta mekanismista.
Stereokemia
E2 on stereospesifinen reaktio .
Reaktio tapahtuu vain, kun vety ja poistuva ryhmä ovat anti-pleurplanar- asennossa .
Vasteeseen vaikuttavat tekijät
- E2: n reaktionopeus vaihtelee vain vähän riippuen tarkasteltavan halogenidin luokasta (ensisijainen: I, sekundäärinen: II, tertiäärinen: III). Kuitenkin mitä korkeampi luokka, sitä nopeampi reaktio (III> II> I) steerisistä syistä (eliminointi mahdollistaa lopullisessa tuotteessa olevien, suurten ja siten "isojen" substituenttien poistamisen lopputuotteessa, reagenssissa koska tässä kulkee valenssikulmasta 109 ° 28 'tässä "sp 3 " -hiilen tasolla , joka kantaa protonia H, valenssikulmassa 120 °, lopputuotteessa, jossa sama hiili on nyt "hybridisoitu sp 2 "). Primaarinen halogeenialkaani on yleensä edullinen tässä tapauksessa, mutta kun se on sekundäärisen halogeenialkaanin läsnä ollessa, E1- ja E2-tyyppiset reaktiot erotetaan potentiaalisten mesomeeristen vaikutusten perusteella ("mesomeerivaikutus: yleinen termi, joka määrittelee elektronisen vaikutuksen, joka vastaa varauksen, tässä positiivisen, siirtymiselle aryyliryhmälle, esimerkiksi rikkoutuneen CH-sidoksen välittömälle naapurille, siis "a: ssa", puhutaan vahvan emäksen "deprotonoinnista". Mikä tahansa substituentti hiiliketjussa, joka kykenee stabiloimaan karbeniumionin (C + karbokatio ) tämän tyyppisen elektronisen vaikutuksen avulla, edistää E1-mekanismia.
- Reaktionopeus kasvaa emäksen lujuuden myötä, joten tarvitaan vahvaa emästä.
- Lähtevän ryhmän nukleofuge-luonteella on myös vaikutus reaktioon, mutta tämä vaikutus ei ole ensisijainen parametri, toisin kuin yksimolekulaarinen eliminaatiomekanismi (E1).
- Bimolekulaarisen E2-eliminaation reaktiomekanismin edistämiseksi on järkevää käyttää aproottista liuotinta (DMSO, THF, tolueeni, n-heksaani jne.)
Kilpailu
Tämä reaktio kilpailee paitsi E1, mutta myös nukleofiilinen substituutio reaktioita, erityisesti S- N- 2 , joka tapahtuu samoissa olosuhteissa. Huomaa, että eliminointireaktio vaatii enemmän energiaa kuin vastaava korvausreaktio, yleensä kuumentamalla.
Huomautukset
Käytetty emäs on myös nukleofiili . Tämä selittää kilpailun vaihtojen reaktioilla. Reaktion lopussa löytyy sekoitettuja eliminaatiotuotteita ja korvaavia tuotteita.