Histone
Histoni H2A / H2B / H3 / H4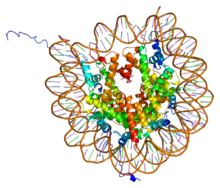 Edustus kompleksin, joka on muodostettu nukleosomiin hiukkasen (h3, h4, H2A, H2B), ja DNA- fragmentti, 146 emäsparin pitkä ( ATE 1AOI ).
Edustus kompleksin, joka on muodostettu nukleosomiin hiukkasen (h3, h4, H2A, H2B), ja DNA- fragmentti, 146 emäsparin pitkä ( ATE 1AOI ).
| Pfam | PF00125 |
|---|---|
| Pfam- klaani | CL0012 |
| InterPro | IPR007125 |
| SCOP | 1 tunti |
| SUPERFAMILY | 1 tunti |
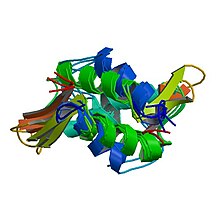 Rakenne histoni HIST1H1B (en) ( ATE 1GHC )
Rakenne histoni HIST1H1B (en) ( ATE 1GHC )
| Pfam | PF00538 |
|---|---|
| InterPro | IPR005818 |
| FIKSU | SM00526 |
| SCOP | 1hst |
| SUPERFAMILY | 1hst |
Histonit ovat proteiinit sijaitsevat tumassa on soluissa eukaryoottien ja arkkien . Ne ovat kromosomien tärkeimmät proteiinin ainesosat . Ne liittyvät itse asiassa läheisesti siihen DNA: han, jonka ne sallivat tiivistämisen, mikä muodostaa rakenteita, joita kutsutaan nukleosomeiksi : DNA kierretään histonien ympärille kuin lanka kelan ympäri. Histoneissa on erittäin runsaasti emäksisiä aminohappoja ( lysiini ja arginiini ), joiden positiivinen varaus fysiologisessa pH: ssa mahdollistaa vahvan vuorovaikutuksen negatiivisten varausten kantavien DNA: n fosfaattiryhmien kanssa .
Rakenne
Histonit ovat pieniä emäksisiä proteiineja, joiden molekyylimassa on 13-15 kDa. Niille on ominaista pallomainen C-terminaalinen domeeni, histonikertainen domeeni . Tämä domeeni, erittäin konservoitunut arkkien ja korkeamman eukaryooteissa , koostuu kolmesta α heliksien erottaa kaksi lyhyttä silmukkaa. Se sallii histonien dimeroinnin niin sanotussa kädenpuristuskuviossa , joka toimii perustana nukleosomin kokoamiselle .
Histonikertainen domeeni löytyy monista muista proteiineista kuin histoneista, ja se määrittelee proteiiniperheen, joka tunnetaan nimellä histonimainen .
Histonien N-pää on rakentamaton ja ulottuu DNA: n ulkopuolelle kootuksi nukleosomiksi. Näihin päihin pääsevät modifioivat entsyymit .
Erilaisia histoneja
Histonit sisältävät viisi proteiiniluokkaa, ryhmitelty kahteen luokkaan niiden roolin perusteella nukleosomin muodostumisessa:
- H2A- , H2B-, H3- ja H4- luokkien histonit muodostavat "ydin" histonit, jotka on nimetty siksi, että ne muodostavat nukleosomin ydinpartikkelin: Kunkin luokan kaksi histoniaa assosioituvat oktameeriin, jonka ympärillä DNA: n kaksoisjuoste noin 150 emäsparit;
- H1- luokan histonit ovat niin sanottuja "sitovia" histoneja: Tämän luokan histoni sitoo DNA: n paikassa, johon se tulee ja poistuu ydinpartikkelista, ja siten "sulkee" nukleosomin.
Jokainen luokka sisältää useita alatyyppejä (paitsi luokka H4), jotka erotetaan ilmentymisprofiilinsa mukaan:
- alatyypit, joiden ilmentyminen liittyy DNA-replikaatioon;
- alatyypit, joiden ilmentyminen on riippumatonta DNA-replikaatiosta;
- alatyypit, jotka ilmaistaan erityisesti tietyissä kudoksissa tai tietyissä kehitysvaiheissa.
Pyörivissä soluissa alatyypit, joiden ilmentyminen on kytketty replikaatioon, ovat hallitsevia kromatiinissa, minkä vuoksi niitä kutsutaan tavanomaisiksi tai kanonisiksi histoneiksi . Sitä vastoin muihin alatyyppeihin viitataan "histonimuunnelmina" ; ne edustavat yleensä alle 10% kaikista histoneista pyöräilevissä soluissa, mutta tämä osuus voi saavuttaa 50% erilaistuneissa soluissa.
Geenit koodaavat tavanomainen histonit ovat yleensä läsnä genomissa on useita kopioita järjestetty klustereita - esimerkiksi ihmisillä, kolmeen ryhmään kromosomeissa 1 ja 6; hiirissä kolme klusteria kromosomeissa 3, 11 ja 13. Niillä on eukaryoottisille geeneille epätyypilliset ominaisuudet, kuten intronien puuttuminen ja transkriptiopääte , jonka varren silmukkarakenne signaloi polyadenylaatiosignaalin sijaan . Sitä vastoin histonivariantteja koodaavat geenit ovat läsnä vain yhdessä tai kahdessa kopiossa ja jakautuvat erillään koko genomiin; Niillä kaikilla on ainakin yksi introni ja yksi polyadenylaatiosignaali.
Histonin ja DNA: n kondensaatio
Kahden nukleosomin välillä on noin 54 emäsparia, tämä arvo vaihtelee lajin mukaan (esimerkiksi hiivalla on sata ja kuusikymmentäviisi ). DNA-tiivistymisen seuraava taso sisältää muita ns. Ei-histoniproteiineja . "
Aste DNA: n kondensaatiota noin histoni nukleosomeihin ja ei-histoni-proteiinien on vaihteleva pitkin kromosomeja , on kromatiinin . Siinä on vähän ns. "Avointa" eukromatiinia ja se on RNA-polymeraasikoneiston käytettävissä . Siinä on runsaasti heterokromatiinia , jonka sanotaan olevan "suljettu" ja "saavuttamaton" transkriptiokoneistolle .
Tätä kondensaatioastetta säätelevät histonien N-terminaalisten päiden modifikaatiot, kuten fosforylaatiot , asetyloinnit , metylaatiot , ubikitinaatiot , sumoylaatiot jne. spesifiset entsyymit katalysoivat kaikki nämä modifikaatiot. Histonien kovalenttiset modifikaatiot toimisivat joko suoraan modifioimalla nukleosomien ympärillä käämittävän DNA: n tiivistymistä tai muodostamalla epäsuorasti "merkkejä", jotka mahdollistavat kromatiinin rakenteen muokkaamiseen kykenevien proteiinien rekrytoinnin . Strahl ja Allis ehdottivat koodina toimivien histonien kovalenttisten modifikaatioiden mallia ("histonikoodi") vuonna 2000 Nature- lehdessä . Tämä koodi ei kuitenkaan näytä olevan kaukana yleismaailmallisesta ja melko suhteellisen spesifinen tarkasteltavien geenien ja solujen mukaan.
Histonikoodi
Histonikoodi muodostaa suoran yhteyden histonihännän tiettyjen tähteiden modifikaation välillä, joka luo sidoksia proteiiniefektoreille, ja kromatiinien transkriptiotilaan .
Yksi histonimuutos voi vaikuttaa toiseen synergistisesti tai antagonistisesti; se on mekanismi, joka tuottaa ja vakauttaa tiettyjä sormenjälkiä.
Asetylointi (lisäys asetyyliryhmä) suoritetaan tiettyjä lysiinitähteiden kautta entsyymien nimeltä histoni asetyylitransferaasit (HAT).
Se vähentää yleensä nukleosomien välistä vuorovaikutusta sekä histonien hännän ja DNA-fragmentin välillä, joka muodostaa yhteyden nukleosomien välillä. Tämä johtaa kromatiinin rentoutumiseen, mikä saa sen siirtymään eukromatiinitilaan ja mahdollistaa siten paremman pääsyn muihin tekijöihin. Asetylaatio liittyy transkription aktivoitumiseen ja on helposti palautuva histonideasetylaasien (HDAC) vaikutuksen kautta.
Metylaatio , vuorostaan, voidaan suorittaa joko lysiini tai arginiini ja voi koostua lisätään yksi, kaksi tai kolme metyyliryhmää.
Metyloiduista tähteistä ja lisättyjen ryhmien lukumäärästä riippuen se liittyy transkription aktivoitumiseen tai tukahduttamiseen. Pitkään staattisena pidetyn histonimetylaation osoitetaan olevan palautuva modifikaatio, joka liittyy dynaamiseen prosessiin, vaikkakin vakaampi kuin asetylointi ja fosforylaatio. Yhä useampi histonidemetylaasi tunnistetaan.
Yleensä nämä kaksi modifikaatiotyyppiä ovat antagonistisia, ja lysiinien deasetyloinnin on edeltävä niiden metylointia. Tämä antagonismi johtaa tietyn dynaamisen tasapainon muodostumiseen heterokromatiinin (yleensä ei-ekspressoituva ja tietyillä avainhapoilla metyloidut) ja eukromatiinin (yleensä ekspressoituvat ja asetyloidut) alueiden välillä. Esimerkiksi histoni H3: sta peräisin olevan lysiinin 9 tiedetään liittyvän metyyloituna ympäröivään kromatiinin repressointiin. Tämän metylaation tunnistaa proteiini, HP1, joka sitoutuu siten metyloiduun H3: een. Puolestaan HP1 houkuttelee proteiinia Suv39, histonimetyylitransferaasia, joka kykenee metyloimaan viereisen nukleosomin histonin H3 lysiinin 9 ja niin edelleen. Siksi voimme nähdä, kuinka askel askeleelta H3-histonit metyloidaan ja kromatiini kondensoituu. Tämä heterokromatiinin tunkeutuminen kuitenkin lopetetaan, jos havaittu H3-lysiini 9 on jo asetyloitu. Tämä luo kilpailukykyisen tasapainon ekspressoitujen ja repressoitujen kromatiinidomeenien välillä.
Muutokset histonijänteissä toimivat epigeneettisinä "merkkeinä", jotka johtavat eri proteiiniluokkien rekrytointiin, koska asetyloidut tai metyloidut lysiinit tunnistetaan eri proteiinidomeeneilla. Lisäksi tiettyjen tekijöiden rekrytointi kromatiinitasolla edellyttää jo sitoutuneiden histonien ja proteiinien modifikaatioiden olemassaoloa. Histonikoodi tulkitaan sen vuoksi muiden kromatiiniin liittyvien tekijöiden yhteydessä, ja modifioitujen histonien ja muiden tekijöiden välisen vuorovaikutuksen yhdistelmä määrää, rekrytoidaanko proteiini kromatiiniin.
Histonimuunnelmat
Useista eukaryoottisista lajeista on löydetty histonivariantteja, joita kutsutaan myös ei-kanoonisiksi histoneiksi.
Näillä muunnoksilla on sekvenssi, joka eroaa tavanomaisten histonien sekvenssistä vain muutamalla tähteellä (ns. Homeomorfisten varianttien tapaus ) tai suuremmilla proteiinin osilla ( heteromorfisten varianttien tapaus ).
Histonimuunnelmilla on tärkeä rooli biologian eri osa-alueilla, kuten DNA: n korjaus, sentromeerinen organisoituminen, X-sukupuolikromosomin inaktivaatio ja urospuolisten sukusolujen spesifinen kondensaatio.
Histonit ja lämpötila
Rapussa ( Arabidopsis thaliana ) yksi histoni (H2A.Z) riittää tekemään taksonin herkäksi alle 1 ° C: n lämpötilan vaihteluille. Tämä histoni muokkaa DNA: n kelaamista itsessään ja kontrolloi siten tiettyjen molekyylien pääsyä DNA: han, joka estää tai aktivoi useita kymmeniä geenejä. Tämä "biotermostaatin" vaikutus vaikuttaa luonteeltaan yleiseltä, koska se havaitaan myös hiivassa .
Vuonna sperma
Histonit korvataan protamiinilla , runsaasti arginiinia ja kysteiiniä sisältävillä proteiineilla .
Kysteiinipitoisuus mahdollistaa disulfidisillan muodostumisen . Tämä rakenne suojaa DNA: ta mahdollisten lannoitukseen liittyvien liikkeiden aikana .
Huomautuksia ja viitteitä
- Annabelle Gérard, Sophie Polo ja Geneviève Almouzni " koodinimi: histones " Pour la Science , n o 46,Maaliskuu 2005( ISSN 0153-4092 , lue verkossa )
- Arents ja Moudrianakis 1995
- Sullivan et ai. 2002
- Fan ja Roberts 2006
- Brush et ai. 1985
- Wells ja Kedes 1985
- Marzluff et ai. 2002
- Kamakaka ja Biggins 2005
- Strahl ja Allis 2000
- Klose ja Zhang 2007
- Redon et ai. 2002
- Billon ja Cote 2011
- Foltz et ai. 2009
- Fernandez-Capetillo et ai. 2003
- Okada et ai. 2005
- Govin et ai. 2004
- Kumar ja Wigge 2010
- Perrier 2010
Katso myös
Bibliografia
- (en) Gina Arents ja Evangelos N. Moudrianakis , " Histonitaitto : läsnä oleva arkkitehtoninen motiivi, jota käytetään DNA: n tiivistämisessä ja proteiinidimeroinnissa " , Proc. Natl. Acad. Sci. USA , voi. 92, n ° 24,Marraskuu 1995, s. 11170–11174 ( PMID 7479959 , lue verkossa [PDF] )
- (en) David Brush , Jerry B. Dodgson , Ok-Ryun Choi , Priscilla Stevens ja James Douglas Engel , " Korvausvariantin histonigeenit sisältävät välissä olevia sekvenssejä " , Mol. Solu. Biol. , voi. 5, n o 6,1985, s. 1307–1317 ( PMID 2863747 , lue verkossa )
- (en) Li Fan ja Victoria Roberts , " Kompleksi linkkihistoni H5: stä nukleosomiin ja sen vaikutukset kromatiinin pakkaamiseen " , Proc. Natl. Acad. Sci. USA , voi. 103, n ° 22,2006, s. 8384–8389 ( PMID 16717183 , DOI 10.1073 / pnas.0508951103 , lue verkossa )
- (en) Oscar Fernandez-Capetillo , Shantha K. Mahadevaiah , Arkady Celeste , Peter J. Romanienko , R. Daniel Camerini-Otero , William M. Bonner , Katia MANOVA , Paul Burgoyne André Nussenzweig , ” H2AX vaaditaan chromatin remontin ja sukupuolikromosomien inaktivointi uroshiiren meioosissa ” , Dev. Cell , voi. 4, n o 4,2003, s. 497–508 ( PMID 12689589 )
- (en) Daniel Foltz , Lars Jansen , Aaron Bailey , John Yates , Emily Bassett , Stacey Wood , Ben Black ja Don Cleveland , " CENP-A-nukleosomien keskikohtainen kokoonpano välittää HJURP " , Cell , voi. 137, n ° 3,2009, s. 472–484 ( PMID 19410544 , DOI 10.1016 / j.cell.2009.02.039 , lue verkossa )
- (en) Jérôme Govin , Cécile Caron , Cécile Lestrat , Sophie Rousseaux ja Saadi Khochbin , " Histonien rooli kromatiinin uudistumisessa nisäkkäiden spermiogeneesin aikana " , Eur. J. Biochem. , voi. 271, n ° 17,2004, s. 3459–3469 ( PMID 15317581 , DOI 10.1111 / j.1432-1033.2004.04266.x , lue verkossa )
- ( fr ) Rohinton Kamakaka ja Sue Biggins , " Histonivariantit : poikkeamat? ” , Genes Dev. , voi. 19, n ° 3,Helmikuu 2005, s. 295-310 ( PMID 15687254 , DOI 10,1101 / gad.1272805 , lukea verkossa )
- (en) Robert Klose ja Yi Zhang , " Histonimetylaation säätely demetyyliminaation ja demetylaation avulla " , Nat. Ilm. Mol. Cell Biol. , voi. 8, n o 4,2007, s. 307–318 ( PMID 17342184 , DOI 10.1038 / nrm2143 )
- (en) S. Vinod Kumar ja Philip A. Wigge , " H2A.Z: tä sisältävät nukleosomit välittävät lämpöherkkää vastetta Arabidopsiksessa " , Cell , voi. 140, n o 1,2010, s. 136–147 ( PMID 20079334 , DOI 10.1016 / j.cell.2009.11.006 )
- (en) William Marzluff , Preetam Gongidi , Keith Woods , Jianping Jin ja Lois Maltais , ” Ihmisen ja hiiren replikaatiosta riippuvat histonigeenit ” , Genomics , voi. 80, n o 5,2002, s. 487–498 ( PMID 12408966 )
- (en) Takashi Okada , Makoto Endo , Mohan Singh ja Prem Bhalla , " Arabidopsiksen histoni-H3-geeniperheen analyysi ja mies-gametispesifisen variantin AtMGH3 tunnistaminen " , Plant J. , voi. 44, n o 4,2005, s. 557–568 ( PMID 16262706 , DOI 10.1111 / j.1365-313X.2005.02554.x )
- Jean-Jacques Perrier , " Proteiinilämpömittari kasveissa ", Tiede ,2010( lue verkossa )
- (en) Christophe Redon , Duane Pilch , Emmy Rogakou , Olga Sedelnikova , Kenneth Newrock ja William Bonner , " Histone H2A variantit H2AX ja H2AZ " , Curr. Opin. Luuta. Dev. , voi. 12, n o 22002, s. 162–169 ( PMID 11893489 )
- (en) Pierre Billon ja Jacques Côté , " H2H.Z-histonin tarkka laskeuma kromatiinissa genomin ilmentymiseen ja ylläpitoon " , Biochim Biophys Acta. ,lokakuu 2011( PMID 22027408 , lue verkossa )
- (en) Brian D. Strahl ja C. David Allis , “ Kovalenttisten histonimuutosten kieli ” , Nature , voi. 403, n ° 6765,2000, s. 41–45 ( PMID 10638745 , DOI 10.1038 / 47412 )
- (en) Steven Sullivan , Daniel Sink , Kenneth Trout , Izabela Makalowska , Patrick Taylor , Andreas Baxevanis ja David Landsman , " The Histone Database " , Nucleic Acids Res. , voi. 30, n o 1,tammikuu 2002, s. 341–342 ( PMID 11752331 , lue verkossa )
- (en) Dan Wells ja Larry Kedes , " Ihmisen histoni-cDNA: n rakenne: todiste siitä, että pohjimmiltaan ekspressoiduilla histonigeeneillä on sekvenssejä ja koodaavat polyadenylyloidut mRNA: t " , Proc. Natl. Acad. Sci. USA , voi. 82, n o 9,1985, s. 2834–2838 ( PMID 2859593 , lue verkossa [PDF] )