Alfa-potkuri
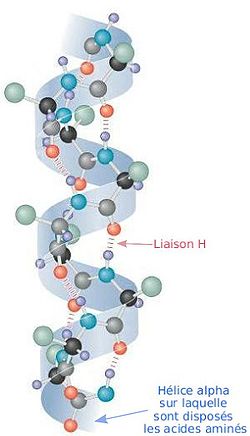
Alfakierteessä ( α helix ) on yhteinen sekundaarirakenne ja proteiinien . Se muodostuu kierteisen muotoisen polypeptidiketjun säännöllisestä käämityksestä oikealla pyörimisnopeudella, jossa aminohapon pääketjun kukin NH-ryhmä muodostaa vetysidoksen pääketjun C = O-ryhmän kanssa. neljäs sitä edeltävä aminohappo. Tätä toissijaista rakennetta kutsutaan joskus Pauling-Corey-Branson α-kierteeksi . Kierukan 3.6 13 nimeä käytetään myös tämän sekundäärirakenteen määrittelemiseen, arvo 3,6 vastaa aminohappojen lukumäärää kierukan korkeudessa; 13 on vetysidoksen sulkeman renkaan atomien lukumäärä. Proteiineissa läsnä olevien paikallisten rakenteiden tyyppien joukosta a-spiraali on eniten ennustettavissa oleva sekundaarirakenne ensisijaisen sekvenssianalyysin avulla sekä eniten levinnyt.
Löytö
1930-luvulla William Astbury tuo esiin erittäin tärkeitä muutoksia villakuitujen tai märkien hiusten röntgendiffraktiolla , kun ne venytetään. Tiedot osoittavat, että venyttämättömillä kuiduilla on toistuva molekyylirakenne 5,1 Å ( 0,51 nm ) välein .
Astbury olettaa, että venymättömät kuidut muodostavat taitetun rakenteen. Myöhemmin muiden tutkijoiden, kuten Maurice Hugginsin, kanssa hän ehdotti seuraavaa mallia:
- taitetut proteiinimolekyylit muodostavat kierteen, jota kutsutaan a-muodoksi;
- kuidun venyttäminen aiheuttaa kierteen purkautumisen muodostaen pidennetyn tilan, jota kutsutaan P-muodoksi.
Hans Neurath (vuonna) on ensimmäinen, joka kyseenalaistaa joitain malleja Astburyn atomien välisten steeristen vaikutusten ongelmista . Vaikka Astbury-malli on väärä, se on aloittelija Linus Paulingin , Robert Coreyn ja Herman Bransonin vuonna 1951 kehittämien proteiinien, joissa on α-kierre- ja β-levy (Astbury-nimikkeistö on säilytetty), uudemmat toissijaiset rakennemallit ja ehdottaa oikean ja vasemman potkurin olemassaolo teoreettisin perustein. Vuonna 1960 myoglobiinin kiderakenne osoitti suurimman osan suorista kierteistä. Neurathin ja Astburyn työ antoi HS Taylorille (en) , Maurice Hugginsille (en) ja William Braggille mahdollisuuden ehdottaa mallia, joka on lähellä α-spiraalia keratiinille .
Kaksi ratkaisevaa tekijää mahdollisti a-heliksin ominaisuuksien määrittämisen : toisaalta peptidien kristallografisten rakenteiden ja Pauling-ennusteen ansiosta saatujen sidosten geometrian tuntemus peptidisidoksen ja toisaalta hypoteesin hylkääminen kokonaismäärästä aminohappoja kierukkaa kohti. Keskeinen hetki α-heliksimallin löytämisessä tapahtui keväällä 1948. Tänä aikana Pauling sairastui ja joutui jäämään kotiin: joutokäynnillä hän piirsi polypeptidijonon paperiliuskaan huolehtien siitä, että tasomaiset peptidisidokset. Muutaman yrityksen jälkeen hän onnistuu saamaan mallin, jolla on fyysisesti uskottavat vetysidokset. Sitten Pauling työskentelee Coreyn ja Bransonin kanssa vahvistaakseen mallinsa ennen julkaisua. Vuonna 1954 Pauling sai ensimmäisen Nobel-palkintonsa tutkimuksestaan kemiallisen sitoutumisen luonteesta ja sen soveltamisesta monimutkaisten aineiden, kuten proteiinien ja α-heliksin rakenteen, selvittämiseen .
Rakenne
Geometria ja vetysidokset
Aminohapot käytettäessä α kierteessä on järjestetty kierrejouset rakenne jaolla kierto oikealle, jolloin kukin aminohappo on kulmassa 100 ° potkuriin ja aiheuttaa translaation 1,5 Å ( 0,15 nm ) akselia pitkin heliksin α. Dunitz kuvaa, kuinka Paulingin ensimmäisessä aihetta käsittelevässä artikkelissa kuvataan vasemmanpuoleista kierukkaa, todellisen rakenteen enantiomeeriä . On kuitenkin olemassa muutama lyhyt, vasemman sävelvoiman potkuri, joka koostuu pääasiassa glysiinistä , ainoasta akiraalisesta aminohaposta, muut kiraaliset biologiset L-aminohapot destabiloivat tämän tyyppisen rakenteen. Α-kierteen nousu (pystysuora etäisyys kahden peräkkäisen kierteen kierroksen välillä) on 5,4 Å ( 0,54 nm ), mikä vastaa 1,5: n ja 3,6: n tuloa. A-kierteen tyypillisin elementti on vetysidos aminohapon pääketjun NH-ryhmän ja sitä edeltävän neljännen aminohapon pääketjun C = O-ryhmän välillä. Virallisessa kansainvälisessä nimikkeistössä ehdotetaan kahta tapaa määritellä a-kierukka , säännössä 6.2 kuvataan a-heliksissä mukana olevien aminohappojen vääntökulmien φ, ψ toistoa; Sääntö 6.3 kuvaa a-kierteen geometrisena kuviona, jolle on tunnusomaista piki korkeus ja vetysidokset. Α heliksit voidaan tunnistaa ja ennustaa proteiinia, jossa käytetään ennustusta laskentamenetelmää, joista yksi on DSSP (toissijainen rakenteet Proteins sanakirja).
Rakenteet, jotka ovat samanlaisia potkuria, sisältävät potkurin 3 10 (jolla on vetysidos pääketjussa kolmen aminohapon välein) ja π-potkurit (joissa vety sitoutuu joka viiden aminohapon välein). Potkuria a voidaan kuvata potkurina 3.6 13 , tässä suoritusmuodossa indeksiarvo (13 kierukalle a) osoittaa vetysidoksen muodostaman silmukan mukana olevien atomien lukumäärän; luku 3.6 osoittaa aminohappojen lukumäärän kierukan kierrosta kohden.
Α-heliksissä mukana olevien aminohappojen pääketjussa on kaksitahoiset kulmat (φ, ψ), joiden keskiarvot ovat (-60 °, -45 °), kuten vastakkaisessa Ramachandran-kaaviossa on esitetty . Yleisemmin aminohapon kaksikulmaisen kulman and ja seuraavan aminohapon kaksikulmaisen kulman sum summa on lähellä -105 °; näin ollen a-kierteen muodostavien aminohappojen kaksikulmaiset kulmat muodostavat Ramachandran-kaaviossa diagonaalin arvojen (-90 °, -15 °) ja (-35 °, -70 °) välillä. Vertailun vuoksi kolmiulotteisten kulmien summa 3 10 kierteelle on -75 °, kun taas π-heliksille se on lähellä -130 ° . Yleinen kaava kiertokulmasta Ω aminohappoa kohden trans- isomeereistä muodostuneissa erityyppisissä polypeptidikierteissä saadaan yhtälöstä:
Α-potkurilla on erityisen kompakti rakenne, potkurin sisällä ei ole käytännössä mitään vapaata tilaa. Aminohapposivuketjut sijaitsevat helixin ulkopuolella ja ovat suuntautuneet hieman N-pään suuntaan (tätä suuntausta verrataan joskus joulukuusioksien järjestämiseen rungon ympärille). Tätä ominaisuutta voidaan käyttää pienellä resoluutiolla elektronitiheyskartoilla tutkittavan proteiinin hiilirungon suunnan määrittämiseksi.
2D-kaavio spiraalin α esityksestä
Kolme a-helix-esityksen 2D-kaavamuotoa käytetään osoittamaan suhteet peptidiketjun primaarirakenteen ja sekundaarirakenteen välillä. Sitten on mahdollista visualisoida a-heliksissä mukana olevien aminohappojen eri sivuketjujen fysikaaliset ominaisuudet ja spesifiset vuorovaikutukset . Kaksi niistä käytetään mallintamaan kierteen α ympäri sylinterimäinen osa: esitys kierukkapyörädiagrammi ( kierrepyörädiagrammi ) ja viime aikoina esitys Wenxiang (en) ( Wenxiang kaavio ).
Kierukkapyörän esitys mallintaa α-kierteen projisoimalla Ca-aminohappojen pääketjun hiilirungon heliksin akselin ympäri ylhäältä alas (katso vastakkaista mallia). Wenxiangin esitys on abstraktimpi kierrehaavan muodossa lehden tasossa. Molemmat esitykset mahdollistavat aminohapposekvenssin visualisoinnin käyttämällä yhden kirjaimen koodausta kussakin Ca: n kohdassa, käyttämällä tiettyjä värejä tai symboleja aminohappojen ominaisuuksien kuvaamiseksi. Hydrofobiset ja hydrofiiliset aminohapot mainitaan aina, ne ovat todellakin mukana a-heliksin vuorovaikutuksessa läheisen ympäristön kanssa. Joissakin esityksissä on esitetty positiivisesti ja negatiivisesti varautuneita aminohappoja samoin kuin epäselviä aminohappoja, kuten glysiini . Näissä malleissa ei ole yleistä käytäntöä aminohapposivuketjujen koodaamiseksi. Wenxiang-esitys tekee mahdolliseksi visualisoida aminohappojen suhteelliset sijainnit toistensa suhteen minkä tahansa pituisilla α-heliksillä , kun taas spiraalipyörän esitys on rajoitettu lyhyisiin α-spiraaleihin aminohappojen päällekkäisyyden vuoksi mallissa.
Nämä erilaiset mallit tarjoavat intuitiivisen ja visuaalisen 2D-esityksen hydrofobisten ja hydrofiilisten aminohappojen järjestelystä a-heliksissä , niitä voidaan käyttää heliksin / heliksin, heliksin / kalvojen tai proteiini / proteiini-vuorovaikutusten tutkimiseen. Useita verkkosivustoja ja ohjelmia on saatavana kierukkapyöräesitysten tuottamiseksi. Viime aikoina on luotu Wenxiang-niminen verkkopalvelin, jonka avulla voidaan jäljittää minkä tahansa α-kierteen Wenxiang-esitys .
A-heliksin viimeinen 2D-esitys on avata kierukka linjaa pitkin, joka on yhdensuuntainen heliksin akselin kanssa, ja sitten edustaa aminohappoja pystysuunnassa. Tämä esitys ei sovellu heliksien väliseen vuorovaikutukseen, mutta se on tapa visualisoida sisäisten membraaniproteiinien sekvenssijärjestely osoittamalla hydrofobisten aminohappojen sijoittuminen vuorovaikutuksessa kalvon kanssa ilman tarvetta tietää järjestelyä α-heliksien tilassa. .
Vakaus
Proteiineissa tutkitut a-heliksit muodostuvat neljästä yli neljänkymmeneen tähteeseen, keskimääräinen a-heliksi sisältää noin kymmenen aminohappoa ja muodostaa noin kolme kierrosta. Yleensä lyhyillä polypeptideillä ei ole a-kierukkarakennetta liuoksessa, polypeptidiketjun taittumisen entrooppisia kustannuksia ei kompensoida riittävällä määrällä stabiloivia vuorovaikutuksia. Α-heliksien sisällä olevien vetysidosten katsotaan olevan heikompia kuin β-arkeissa olevat, ja vesimolekyylit hyökkäävät helposti niihin. Hydrofobisissa ympäristöissä, kuten plasmamembraanissa , vesitrifluorietanolin (TFE) liuotinseoksen läsnä ollessa tai eristettynä kaasufaasissa, polypeptidit voivat omaksua vakaat a-kierukkarakenteet . Niin kutsuttujen silloitemolekyylien lisääminen peptidiliuoksiin voi stabiloida kierukkarakenteen.
Kokeelliset tekniikat a-heliksien tunnistamiseksi
Koska α-heliksien karakterisointi vetysidosten ja aminohappojen pääketjun hiilirungon avulla, yksityiskohtaisin kokeellinen todiste a-heliksin rakenteesta tulee röntgenkristallografialla saaduista analyyseistä (kuten esimerkissä vastapäätä). Peptidirungon karbonyyliryhmien happiatomit osoittavat alaspäin (kohti C-terminaalia ), mutta heijastuvat hieman; vetysidokset ovat käytännössä yhdensuuntaisia kierteen akselin kanssa. Rakenteelliset tutkimukset proteiinien suoritetaan NMR-spektroskopialla proteiinien (in) vastaavasti kuvataan α heliksien ansiosta tutkimuksissa ytimen Overhauser-ilmiöiden (NOE-vaikutus), joka esittää väliset kytkennät atomien vierekkäisten kierrosten. Joissakin tapauksissa yksittäiset vetysidokset voidaan tunnistaa heikkona kytkentänä NMR-spektroskopiassa.
On olemassa useita matalan resoluution menetelmiä a-heliksin karakterisoimiseksi. Kemiallinen siirtymä NMR-spektroskopia C α , C β , C ' hiiltä sekä jäljellä dipoli kytkimet (fi) ovat riittävät karakterisointia varten. Tutkimus sirkulaaridikroismia on α heliksien UV-kaukana (170- 250 nm ) on ominaista, kaksi minimit havaitaan noin 208 nm ja 222 nm . Luonnehdinta α heliksien mukaan infrapunaspektroskopialla käytetään harvoin, koska spektri α heliksien on liian monia yhtäläisyyksiä että satunnainen rakenteita , on kuitenkin mahdollista erottaa kaksi rakennetta, jonka vetyä deuteriuminvaihto- (fi) . Elektronimikroskopia alhaisessa lämpötilassa nyt mahdollista tunnistaa yksittäiset α heliksien sisällä proteiinin karakterisointi eri aminohappojen, jotka muodostavat kierteen on aktiivinen tutkimusalue.
Pitkiä ketjuja aminohappojen homopolymeerit muodostavat usein α heliksejä kun liukeneva. Nämä pitkät heliksit voidaan havaita dielektrisellä relaksaatiolla , virtauksen kaksimurtumisella (in) tai mittaamalla diffuusiovakio.
Aminohapot mukana
Useat aminohapot edistävät a-heliksien, kuten metioniinin , alaniinin , leusiinin , varautumattoman glutamaatin tai lysiinin (tai "MALEK": n käyttämistä yhden kirjaimen aminohappomerkinnöistä), muodostumista. Toisaalta proliinilla ja glysiinillä on destabilisoiva rooli a-heliksien luomisessa . Proliinin pääketjussa ei ole vetyä, eikä se voi muodostaa vetysidosta, ja lisäksi sen sivuketju häiritsee steerisesti edellisen kierroksen hiilirunkoa. Jos proliinia oli läsnä a-kierukassa , se aiheuttaisi kierteen pysähtymisen tai voimakkaan noin 30 °: n muodonmuutoksen kierteen akseliin nähden. Toisaalta proliini on usein a-heliksin ensimmäinen aminohappo , luultavasti sen rakenteellisen jäykkyyden vuoksi. Glysiinin läsnäolo a-heliksissä pyrkii häiritsemään rakennetta tämän aminohapon suuren konformaation joustavuuden vuoksi.
Aminohapon affiniteettitaulukko a-heliksin muodostuksessa
Taulukko esittää keskimääräisen vapaan energian A (E) (GG) eron, joka ilmaistaan Kcal: na / mol kutakin aminohappoa α-kierteessä suhteessa alaniinin vapaaseen energiaan (mielivaltaisesti kiinnitetty 0: een). Suuremmat positiiviset luvut osoittavat epäedullisimmat aminohapot a-heliksin muodostamiseksi . Näissä arvoissa voidaan kuitenkin havaita poikkeamia naapurijäämien luonteesta riippuen.
| Aminohappo | 3-kirjaiminen koodi | Yhden kirjaimen koodi | Δ (ΔG) ( kcal / mol (tuumaa) ) |
|---|---|---|---|
| Alaniini | Kohteeseen | AT | 0 |
| Arginiini | Arg | R | 0,21 |
| Asparagiini | Asn | EI | 0,65 |
| Asparagiinihappo | Asp | D. | 0,69 |
| Kysteiini | Cys | VS | 0,68 |
| Glutamiinihappo | Liima | E | 0,40 |
| Glutamiini | Gln | Q | 0,39 |
| Wisteria | Gly | G | 1.00 |
| Histidiini | Hänen | H | 0,61 |
| Isoleusiini | Saari | Minä | 0,41 |
| Leusiini | Leu | L | 0,21 |
| Lysiini | Liljat | K | 0,26 |
| Metioniini | Tavannut | M | 0,24 |
| Fenyylialaniini | Phe | F | 0.54 |
| Proline | Pro | P | 3.16 |
| Serine | Ser | S | 0,50 |
| Treoniini | Thr | T | 0,66 |
| Tryptofaani | Trp | W | 0,49 |
| Tyrosiini | Tyr | Y | 0.53 |
| Valine | Val | V | 0,61 |
Dipolaarinen hetki
A-heliksillä on kokonaisdipolimomentti, joka vastaa karbonyyliryhmien mikrodipolien summaa kierukan akselilla. Tämän dipolimomentin vaikutukset kierukassa ovat kiistanalaisia. A- heliksien N-terminaalinen pää liittyy usein negatiiviseen varaukseen, joka on peräisin aminohapon (glutamaatti tai aspartaatti) sivuketjusta tai joskus fosfaattiryhmästä. Useat tutkijat katsovat, että kierteen dipolimomentti liittyy tähän sähköstaattiseen vuorovaikutukseen, kun taas toiset, että N-päässä oleva vapaa NH-ryhmä voitaisiin mallintaa vetysidoksena.
" Käämi kela " super potkuri
Kierteisten kierteiden ( coiled coil ) ovat erittäin stabiileja muotoja, joissa vähintään kaksi α heliksiä kääritään yhteen super sekundaarirakenne. Tämän rakenteen muodostavat kierteet muodostuvat seitsemän tähteen jaksottaisten kuvioiden peräkkäin. Ensimmäinen ja neljäs aminohappo (tunnetaan niiden a- ja d-asemina) ovat melkein aina hydrofobisia (d-tähde on usein leusiini ), jotka ovat suuntautuneet superkäämi-kuvion sisäänpäin. Yleensä viides ja seitsemäs tähde (asema e ja g) ovat vastakkaisen varauksen aminohappoja ja muodostavat suolatasan, joka on vakautettu sähköstaattisten vuorovaikutusten avulla. Kuitumaisia proteiineja kuten keratiini tai varret myosiinin tai kinesiini usein hyväksyä kietoutunut rakenteita kuten dimeroidussa proteiineja. Superkelojen pari (joka muodostaa neljän heliksin nipun) on hyvin yleinen rakenne proteiineissa, löytyy ihmisen kasvuhormonista ja useista sytokromilajikkeista . Rop-proteiini, joka edistää plasmidi -replikaation in bakteereissa, on ainutlaatuinen tapaus, jossa polypeptidiketju muodostaa superhelix ja yhdistyksen kahden monomeerin koota nipun muodostamiseksi, jossa on neljä helices.
Α proteiinit
Myoglobiini ja hemoglobiini ovat ensimmäisiä proteiineja, joiden proteiinit on erotettu röntgenkristallografialla; niillä on hyvin läheiset taitokset ja ne muodostavat yli 70% a-heliksistä , loput aminohapoista muodostavat silmukoita ilman tyypillistä toissijaista rakennetta. Rakenteellinen luokitus proteiinien perustuu rakenteellisista domeeneista on tietokanta, joka koostuu useimpien α proteiineja.
Toiminnallinen rooli
DNA-vuorovaikutukset
Α heliksit ovat läsnä DNA : n rakenteellisissa sitoutumisyksiköissä , kuten helix-kyynärpää-helix , leusiinivetoketju ja sinkkisormimallit . A-kierteen halkaisija aminohappojen sivuketjuilla on noin 12 A (so. 1,2 nm ), joka vastaa B-muodon DNA-molekyylin pääuran pituutta.Superkela tai vetoketju ovat heliksien dimeerejä, jotka voivat olla vuorovaikutuksessa symmetrisesti kummallakin puolella DNA-molekyylin. Max-transkriptiotekijä esittää leusiinivetoketjun, joka koostuu superkäämisestä, joka on järjestetty dimeeriksi, joka kuljettaa kahta muuta heliksiä vuorovaikutuksessa kahden peräkkäisen DNA-pääuran vuoron kanssa.
Kalvoproteiinit
A-heliksit ovat kalvojen läpäisevien proteiinien rakenteen klassisia komponentteja, kierukan rakenteen muodostavat vetysidokset haudataan sekundäärirakenteen runkoon, aminohappojen hydrofobiset sivuketjut ovat vuorovaikutuksessa kalvojen kanssa. Kalvon läpäisevät proteiinit ankkuroidaan kalvoon vaihtelevalla määrällä a-heliksia , yksi yleisimmistä rakenteista muodostuu seitsemästä kalvon läpikuultavasta heliksistä, jotka muodostavat renkaan, kuten naudan rodopsiinin tai G-proteiiniin kytketyn reseptorin (RCPG) tapauksessa.
Mekaaniset ominaisuudet
A-heliksit voivat joutua venytysjännityksiin spiraalin akselilla pitkin, mikä havaitaan filamenteissa tai kanavissa, joissa on runsaasti a-kierteitä . Tälle venytykselle on tunnusomaista kolme vaihetta: vaihe I vastaa matalan rasituksen järjestelmää, jonka aikana kierukkaa venytetään homogeenisesti; vaihe II vastaa kierukan käännösten epäorganisaatiota rikkoutumalla vetysidoksissa, lopuksi vaihe III liittyy kierteen kovalenttisten sidosten muodonmuutoksiin.
Dynaamiset ominaisuudet
Proteiinien Α-heliksit voivat osoittaa matalataajuista harmonikka-tyyppistä liikettä, jota havainnoidaan Raman-spektroskopialla ja jolle on tunnusomaista lähes jatkumismalli. Spiraalit, joita ei ole vakautettu tertiääristen rakenteiden vuorovaikutuksella, osoittavat dynaamista käyttäytymistä, mikä johtuu pääasiassa heliksin asteittaisesta hajoamisesta sen päissä.
Potkuri - kelan siirtyminen
Aminohappojen homopolymeerit, kuten poly-lysiinit, kykenevät omaksumaan a-heliksirakenteen alhaisessa lämpötilassa hajoamalla korkeassa lämpötilassa. Tätä helix-kelan siirtymää on usein pidetty analogisena proteiinin denaturoitumisen kanssa . Tämä siirtymä on mahdollista mallintaa tilastollisella fysiikalla käyttämällä siirtomatriisia, joka perustuu kahteen parametriin, taipumukseen aloittaa kierukka ja taipumukseen venyttää kierre.
Alan spiraali alalla
Ainakin viidellä taiteilijalla on työssään ollut viittauksia α-kierteeseen: Julie Newdoll maalauksessa, Julian Voss-Andreae, Bathsheba Grossman, Byron Rubin ja Mike Tyka veistoksessa.
Julie Newdoll on suorittanut mikrobiologian tutkinnon alaikäisen taiteen kanssa. Hän on erikoistunut kuvien ja mikroskooppisten molekyylien innoittamiin maalauksiin vuodesta 1990 lähtien. Hänen maalauksensa Rise of the Alpha Helix (vuonna 2003) esittelee ihmishahmoja järjestettyinä α-heliksiksi .
Julian Voss-Andreae on saksalaisen kuvanveistäjä, joka valmistui kokeellisesta fysiikasta ja veistoksesta. Vuodesta 2001 hän on tehnyt veistoksia, jotka perustuvat proteiinien rakenteisiin, α-kierukka on yksi hänen suosikki aiheistaan. Hän teki α-heliksiveistoksia eri materiaaleista, mukaan lukien bambu tai kokonaiset puut. Vuonna 2004 hän teki muistomerkin kunniaksi Linus Paulingin , α-kierteen löytäneen miehen muistoa . Tämä veistos on valmistettu suuresta teräspalkista, jota on muokattu luomaan uudelleen α-kierteen rakenne. Tämä veistos on kirkkaan punainen 3 m korkeuteen asennetaan talon edessä, jossa Pauling lapsuutensa Portlandissa on Oregonissa .
Huomautuksia ja viitteitä
- (in) H Neurath , " Polypeptidiketjujen molekyylinsisäinen taitto suhteessa proteiinirakenteeseen " , Journal of Physical Chemistry , Voi. 44, n ° 3,1940, s. 296-305 ( DOI 10.1021 / j150399a003 )
- (en) JC Kendrew , RE Dickerson , BE Strandberg , RG Hart , DR Davies , DC Phillips and VC Shore , " Myoglobiinin rakenne: Kolmiulotteinen Fourier-synteesi 2 Å- tarkkuudella " , Nature , voi. 185, n ° 47111960, s. 422-427 ( PMID 18990802 , DOI 10.1038 / 185422a0 )
- (sisään) HS Taylor , " Suuret molekyylit atomiesitysten kautta " , Proceedings of the American Philosophical Society , voi. 85,1942, s. 1-12
- (in) M Huggins , " Kuituproteiinien rakenne " , Chemical Reviews , Voi. 32, n ° 21943, s. 195-218 ( DOI 10.1021 / cr60102a002 )
- (in) WL Bragg , JC Kendrew ja MF Perutz , " polypeptidiketjun konfiguraatiot kiteisissä proteiineissa " , Proceedings of the Royal Society A , voi. 203, n ° 1074,1950, s. 321-357 ( DOI 10.1098 / rspa.1950.0142 , lue verkossa )
- (vuonna) L Pauling , RB Corey ja HR Branson , " The Structure of Proteins: Two Hydrogen-Bonded Helical Configuration of the Polypeptide Chain " , Proceedings of the National Academy of Sciences of the United States of America , voi. 37, n o 4,1951, s. 205-211 ( PMID 14816373 , PMCID 1063337 , DOI 10.1073 / pnas.37.4.205 )
- lukea verkossa
- (sisään) J Dunitz , " Paulingin vasenkätinen α-Helix " , Angewandte Chemie International Edition , voi. 40, n ° 22,2001, s. 4167-4173
- (in) IUPAC-IUB Commission on Biochemical Nomenclature, " Lyhenteet ja symbolit polypeptidiketjujen konformaation kuvaamiseen " , Journal of Biological Chemistry , voi. 245,1970, s. 6489–6497 ( lue verkossa )
- lukea verkossa
- K Kabsch ja C Sander , " Proteiinin toissijaisen rakenteen sanakirja: vetysidottujen ja geometristen ominaisuuksien kuviotunnistus ", Biopolymers , voi. 22, n ° 12,1983, s. 2577–2637 ( PMID 6667333 , DOI 10.1002 / bip.360221211 )
- JS Richardson , ” Anatomy ja taksonomia Proteiinit ”, Advances in Protein Chemistry , vol. 34,yhdeksäntoista kahdeksankymmentäyksi, s. 167-339 [1] ( PMID 7020376 , DOI 10.1016 / S0065-3233 (08) 60520-3 )
- (en) SC Lovell , IW Davis , VW III Arendall , PIW Bakker , JM Word , MG- palkinnot , JS Richardson ja DC Richardson , " Rakenteen validointi Cα-geometrian avulla: φ, ψ ja Cβ-poikkeama " , Proteins , vol. 50, n ° 3,2003, s. 437–450 ( PMID 12557186 , DOI 10.1002 / prot.10286 )
- (in) RE Dickerson ja minä Geis , rakenne ja toiminta Proteiinit , Harper, New York,1969
- (en) TC Terwilliger , " α-heliksien nopea mallintaminen elektronitiheyskartoissa " , Acta Crystallographica , voi. D66,2010, s. 268-275 ( PMID 20179338 , PMCID 2827347 , DOI 10,1107 / S0907444910000314 )
- (en) M Schiffer ja AB Edmundson , " Kierukkapyörien käyttö proteiinien rakenteiden esittämiseen ja kierteisen potentiaalin omaavien segmenttien tunnistamiseen " , Biophys. J. , voi. 7, n o 2Maaliskuu 1967, s. 121-35 ( PMID 6048867 , PMCID 1368002 , DOI 10,1016 / S0006-3495 (67) 86579-2 , Bibcode 1967BpJ ..... 7..121S )
- (en) KC Chou , CT Zhang ja GM Maggiora , " Amfifiilisten heliksien hävittäminen heteropolaarisissa ympäristöissä " , Proteins , voi. 28, n o 1,Toukokuu 1997, s. 99–108 ( PMID 9144795 , DOI 10.1002 / (SICI) 1097-0134 (199705) 28: 1 <99 :: AID-PROT10> 3.0.CO; 2-C )
- (en) N Kurochkina , " Helix-helix-vuorovaikutukset ja niiden vaikutus proteiinimotiiveihin ja kokoonpanoihin " , J. Theor. Biol. , voi. 264, n ° 2Toukokuu 2010, s. 585–92 ( PMID 20202472 , DOI 10.1016 / j.jtbi.2010.02.026 )
- (sisään) D Eisenberg , RM Weiss ja TC Terwilliger , " Kierukkamainen hydrofobinen hetki: mitta kierteen amfifiilisyydestä " , Nature , voi. 299, n o 5881,1982, s. 371-374 ( PMID 7110359 , DOI 10.1038 / 299371a0 )
- (in) GP Zhou , " Jäämien hävittäminen proteiinissa LZCC Wenxiang -kaavio tarjoaa uusia oivalluksia proteiini-proteiini-vuorovaikutusmekanismiin " , J. Theor. Biol. , voi. 284, n ° 1,kesäkuu 2011, s. 142–148 ( PMID 21718705 , DOI 10.1016 / j.jtbi.2011.06.006 )
- (vuonna) GP Zhou , " cGMP: stä riippuvan proteiinikinaasi I -alfan leusiinivetoketjun kelatut kelat -domeenien rakenteelliset määritykset ja sen vuorovaikutus myosiinin kevyiden ketjujen fosfaasin myosiinia sitovan alayksikön kanssa " , Protein & Peptide Letters , vol. . 18, n ° 10,2011, s. 966-978 ( PMID 21592084 , DOI 10.2174 / 0929866511107010966 )
- lukea verkossa
- lukea verkossa
- (sisään) KC Chou , WZ Ling ja X Xiai , " Wenxiangin verkkopalvelin kaavioiden piirtämiseen Wenxiang " , luonnontieteet , voi. 3, n o 10,2011, s. 862-865 ( DOI 10.4236 / ns.2011.310111 )
- (in) RR Hudgins ja MF Jarrold , " Helix Formation in Unsolvated Alanine-Based Peptides: Helical Helical Monomers and Dimers " , Journal of the American Chemical Society , Voi. 121, n ° 14,1999, s. 3494-3501 ( DOI 10.1021 / ja983996a )
- (en) CN Pace ja JM Scholtz , " Peptidien ja proteiinien kokeellisiin tutkimuksiin perustuva helix-taipumusasteikko " , Biophys. J. , voi. 75, n o 1,Heinäkuu 1998, s. 422-427 ( PMID 9649402 , PMCID 1299714 , DOI 10,1016 / S0006-3495 (98) 77529-0 , Bibcode 1998BpJ .... 75..422N )
- (in) WGJ Hol ja PT van Duijnen , " Alfa-heliksidipoli ja proteiinien ominaisuudet " , Nature , voi. 273,1978, s. 443-446 ( DOI 10.1038 / 273443a0 )
- (in) JJ He ja FA Quiocho , " Paikallisten dipolien hallitseva rooli kompensoimattomien kustannusten stabiloimisessa sulfaatissa, joka on sitoutunut periplasmisen proteiinin aktiiviseen kuljetukseen " , Protein Science , Voi. 2,1993, s. 1643–1647 ( DOI 10.1002 / pro.5560021010 )
- (in) EJ Milner-White , " Typpiatomin osakuormitus peptidisidoksissa " , Protein Science , Voi. 6,1997, s. 2477–2482 ( DOI 10.1002 / pro.5560061125 )
- (sisään) T Ackbarow X Chen , S Keten ja MJ Buehler , " Hierarkiat, useita energiaesteitä ja vankkuutta hallitsevat alfa-kierteisten ja beeta- arkkiproteiinidomeenien murtumismekaniikkaa " , Proceedings of the National Academy of Sciences of the United States of America , voi. 104, n ° 42,2007, s. 16410–16415 ( PMID 17925444 , PMCID 2034213 , DOI 10.1073 / pnas.0705759104 )
- (in) PC Painter , THE Mosher ja C. Rhoads , " Matalataajuiset moodit proteiinien Raman-spektreissä " , Biopolymers , Voi. 21, n ° 7,Heinäkuu 1982, s. 1469–1472 ( PMID 7115900 , DOI 10.1002 / bip.360210715 )
- (in) KC Chou , " Matalataajuisten moodien tunnistaminen proteiinimolekyyleissä " , Biochem. J. , voi. 215, n ° 3,Joulukuu 1983, s. 465–469 ( PMID 6362659 , PMCID 1152424 )
- KC Chou , ” Matalataajuisten värähtelyjen (fononien) biologiset toiminnot. III. Kierukkarakenteet ja mikroympäristö ”, Biophys. J. , voi. 45, n ° 5,Toukokuu 1984, s. 881-889 ( PMID 6428481 , PMCID 1434967 , DOI 10,1016 / S0006-3495 (84) 84234-4 , Bibcode 1984BpJ .... 45..881C )
- (sisään) B Fierz , A Reiner ja T Kiefhaber , " Paikallinen konformaatiodynamiikka a-heliksissä mitattuna nopealla triplettisiirrolla " , Proceedings of the National Academy of Sciences of the United States of America , voi. 106, n ° 44,tammikuu 2009, s. 1057-1062 ( PMID 19131517 , PMCID 2633579 , DOI 10.1073 / pnas.0808581106 )
- Veistos asennetaan talon edessä, jossa Linus Pauling lapsuutensa Portlandissa on Oregonissa .
- (sisään) J Voss-Andreae , " Protein Sculptures: Life's Building Blocks Inspire Art " , Leonardo , voi. 38,2005, s. 41–45 ( DOI 10.1162 / leon.2005.38.1.41 )
- (fr) Tämä artikkeli on osittain tai kokonaan otettu Wikipedian englanninkielisestä artikkelista " Alpha helix " ( katso kirjoittajaluettelo ) .
Katso myös
Bibliografia
- (en) John Tooze ja Carl-Ivar Brändén , Johdatus proteiinirakenteeseen , New York, Garland Pub,1999( ISBN 0-8153-2304-2 ).
- (en) D Eisenberg , " Alfa-heliksin ja beetalevyn löytäminen, proteiinien tärkeimmät rakenteelliset piirteet " , Proceedings of the National Academy of Sciences of the United States of America , voi. 100, n ° 20,Syyskuu 2003, s. 11207–11210 ( PMID 12966187 , PMCID 208735 , DOI 10.1073 / pnas.2034522100 )
- (en) H Sugeta ja T Miyazawa , " Yleinen menetelmä polymeeriketjujen kierukkaparametrien laskemiseksi joukkovelkakirjojen pituuksista, sidekulmista ja sisäisistä kiertokulmista " , Biopolymers , voi. 5, n o 7,1967, s. 673-679 ( DOI 10,1002 / bip.1967.360050708 )
- (en) Wada , ” alfa-heliksin kuin sähköinen makro-dipoli ” , Advances in Biophysics ,1976, s. 1–63 ( PMID 797240 )
- (en) WG Hol , " Alfa-heliksidipolin rooli proteiinin toiminnassa ja rakenteessa " , Progress in Biophysics and Molecular Biology , voi. 45, n ° 3,1985, s. 149–195 ( PMID 3892583 , DOI 10.1016 / 0079-6107 (85) 90001-X )
- (en) DJ Barlow ja JM Thornton , ” Helix geometry in protein ” , Journal of Molecular Biology , voi. 201, n ° 3,Kesäkuu 1988, s. 601–619 ( PMID 3418712 , DOI 10.1016 / 0022-2836 (88) 90641-9 )
![{\ displaystyle 3 \ cos \ Omega = 1-4 \ cos ^ {2} \ vasen [\ vasen (\ phi + \ psi \ oikea) / 2 \ oikea]}](https://wikimedia.org/api/rest_v1/media/math/render/svg/289a67463099a87877ac9fca00daf052bb2edd9a)