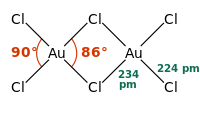Kulta (III) kloridi
| Kulta (III) kloridi | |

| |
| Henkilöllisyystodistus | |
|---|---|
| IUPAC-nimi | Kulta (III) kloridi |
| Synonyymit |
Auric kloridi |
| N o CAS | |
| N o ECHA | 100 033 280 |
| N O EY | 236-623-1 |
| N o RTECS | MD5420000 (vedetön) |
| Ulkomuoto | Punainen kiteinen kiinteä aine |
| Kemialliset ominaisuudet | |
| Raaka kaava | Au Cl 3 (Au 2 Cl 6 : n muodossa ) |
| Moolimassa | 303,326 ± 0,006 g / mol Au 64,94%, Cl 35,06%, |
| Fyysiset ominaisuudet | |
| T ° fuusio | 253,85 ° C (hajoaa) |
| Liukoisuus |
680 g · L -1 (kylmä vesi). Liukenee etanoliin ja dietyylieetteriin |
| Tilavuusmassa | 3,9 g · cm -3 ( 20 ° C , kiinteä) |
| Magneettinen herkkyys | -0.000112 cm³ / mol |
| Lämpökemia | |
| Kiinteä A f H 0 | -118 kJ / mol |
| Kristallografia | |
| Kristallijärjestelmä | monokliininen |
| Tyypillinen rakenne | |
| Koordinaatio | neliön suunnitelma |
| Atomien välinen etäisyys | 224 pm (Au - Cl ulkoinen) 234 pm (Au - Cl silloitus) |
| Linkkikulma | 90 ° (Au - Cl ulkoinen) 86 ° (Au - Cl silloitus) |
| Varotoimenpiteet | |
| NFPA 704 | |
|
0
1
0
(arvio) |
|
| Direktiivi 67/548 / ETY | |
 Xi Symbolit : Xi : Ärsyttävät R-lausekkeet : R36 / 37/38 : Ärsyttää silmiä, hengityselimiä ja ihoa. S-lausekkeet : S26 : Roiskeet silmistä huuhdeltava välittömästi runsaalla vedellä ja mentävä lääkäriin. S36 : Käytä sopivaa suojavaatetusta. R-lausekkeet : 36/37/38, S-lausekkeet : 26, 36, |
|
| Liittyvät yhdisteet | |
| Muut kationit |
Kulta (I) kloridi Hopeakloridi Platinum (II) kloridi Elohopea (II) kloridi |
| Muut anionit |
Kulta (III) fluoridi Kulta (III) bromidi |
| SI- ja STP- yksiköt, ellei toisin mainita. | |
Kulta (III) kloridin , kutsutaan yleensä kloridi auran , on yksi yhdisteistä yleisin on kulta . Sen kaava on Au Cl 3 . Roomalainen numero sen nimessä osoittaa, että kulta on hapettumistilassa +3, mikä on kullan vakain muoto yhdisteissä. Kulta muodostaa myös muita klorideja , kuten esimerkiksi kultaa (I) kloridia (AuCl), joka on vähemmän stabiili kuin Au Cl 3 . Klooriaurihappo (HAuCl 4 ), muodostunut tuote aikana liukenemisen kultaa kuningasvettä , on myös joskus kutsutaan "kulta kloridi", "happo kulta kloridi (III)" tai vaihtoehtoisesti ”kulta (III) kloridihydraattia” .
Kulta (III) kloridi on erittäin hygroskooppista ja liukoinen on veteen ja etanoliin . Se hajoaa yli 160 ° C: n (433 K) tai valossa ja muodostaa joukon komplekseja monien ligandien kanssa .
Rakenne
AuCl 3 on olemassa niin dimeeri , sekä kiinteän ja kaasufaasin; AuBr 3 -bromidi noudattaa samaa mallia. Jokainen Au-keskus on neliön muotoinen. Tämä rakenne on muistuma bi- asteen rakenteita hyväksyi AICI 3 ja FeCI 3 . AuCl 3: n sidokset ovat pääasiassa kovalentteja , mikä heijastaa kullan korkeaa hapettumistilaa ja suhteellisen korkeaa elektronegatiivisuutta (metallia varten).
Kemialliset ominaisuudet
Vedetön AuCl 3 alkaa hajota AuCl noin 160 ° C: ssa ; kuitenkin, tämä reaktio käännetään päinvastaiseksi disproportionaatiolla korkeammissa lämpötiloissa palata metallinen kulta ja AuCl 3 .
AuCl 3 → AuCl + Cl 2 (> 160 ° C ) 3 AuCl → AuCl 3 + 2 Au (> 420 ° C )AuCl 3 on Lewisin happo, joka muodostaa helposti komplekseja. Siten, kanssa kloorivetyhapon , klooriaurihappo (HAuCl 4 ) on muodostettu:
HCI: n vesiliuosta + AuCl 3 (aq) → H + AuCl 4 - (aq)Ionikloridit , kuten KCl, muodostavat AuCl 4 - ioneja AuCl 3: n kanssa .
Vesiliuokset AuCl 3 reagoida alkalin, kuten natriumhydroksidin , jolloin muodostuu sakka, ja epäpuhdas Au (OH) 3 , joka liukenee NaOH muodossa natrium- aurate ( NaAuO 2 ). Varovasti kuumennettaessa Au (OH) 3 hajoaa kulta (III) oksidiksi (Au 2 O 3 ) ja sitten metallikullaksi.
Valmistautuminen
Kulta (III) kloridi valmistetaan enimmäkseen klooraamalla metalli korkeissa lämpötiloissa:
2 Au + 3 Cl 2 → 2 AuCl 3Käyttää
Kulta (III) kloridi on yksi yleisimmistä kultayhdisteistä, ja sitä käytetään siksi lähtökohtana monien muiden kultayhdisteiden synteesille.
Esimerkiksi kaliumsyanidista (KCN) saadaan vesiliukoinen kompleksi KAu (CN) 4, jota kutsutaan myös kaliumdisyanoauraatiksi :
AuCl 3 + 4 KCN → KAu (CN) 4 + 3 KClSuolat kulta (III), erityisesti NaAuCl 4 (muodostettu AuCl 3 + NaCI ), tarjoavat myrkytön vaihtoehto suoloja elohopea (II) katalyyttejä varten reaktioissa alkyynejä . Yksi tärkeistä tämäntyyppisistä reaktioista on terminaalisten alkyynien hydraatio metyyliketonien tuottamiseksi , kuten:
Ketoneja muodostuu yleensä yli 90%: n saannolla näissä olosuhteissa. Käytetään aminoituneita sidoksia, joita voidaan käyttää kultaa (hapetustilassa 3) katalysaattorina.
Viime vuosina, AuCl 3 on herättänyt kiinnostusta orgaanisen kemian lievä happokatalyytin muut reaktiot, kuten alkylointi ja aromaattien ja muuntaminen furaanien ja fenolien (katso alla). Tällaisia reaktioita voidaan käyttää orgaanisessa synteesissä ja lääketeollisuudessa . Siten esimerkiksi 2-metyylifuraani (sylvaani) läpikäy lievän alkyloinnin metyylivinyyliketonilla asemassa 5:
Reaktio etenee 91%: n saannolla vain 40 minuuttia huoneenlämpötilassa, käyttäen vain 1% AuCl 3 on asetonitriili . Tämä saanto on merkittävä siinä mielessä, että sekä furaani että ketoni ovat yleensä hyvin herkkiä sivureaktioille, kuten polymeroinnille happamissa olosuhteissa. Joissakin tapauksissa, joissa on alkyynejä , voidaan muodostaa fenoli:
Reaktioon liittyy monimutkainen uudelleenjärjestely, joka johtaa uuden aromaattisen renkaan muodostumiseen.
Viitteet
- laskettu molekyylimassa välillä " Atomic painot Elements 2007 " on www.chem.qmul.ac.uk .
- NN Greenwood, A. Earnshaw, Chemistry of the Elements , 2 d toim., Butterworth-Heinemann, Oxford, Iso-Britannia, 1997
- Kemian ja fysiikan käsikirja , 71. painos, CRC Press, Ann Arbor, Michigan, 1990
- The Merck Index , 7. painos, Merck & Co, Rahway, New Jersey, USA, 1960
- H. Nechamkin, Elementtien kemia , McGraw-Hill, New York, 1968
- AF Wells, rakenteellinen epäorgaaninen kemia , 5. painos, Oxford University Press, Oxford, UK, 1984
- G.Dyker, Eldorado homogeenista katalyysiä varten? , julkaisussa Organic Synthesis Highlights V , H.-G.Schmaltz, T.Wirth (toim.), s. 48-55 , Wiley-VCH, Weinheim, 2003
- Y. Fukuda, K. Utimoto, J. Org. Chem. 56 , 3729 - 3731 (1991).
- ASK Hashmi, TM Frost, JW Bats, J. Am. Chem. Soc. 122 , 11553 - 11554 (2000).
- Hashmi, ASK; Rudolph, M.; Weyrauch, JP; Wölfle, M.; Frey, W. Beat, JW Angew. Chem. Int. Toim. 2005, 44, 2798-2801
Ulkoinen linkki
Käyttöturvallisuustiedote: Hazard.com
- (fr) Tämä artikkeli on osittain tai kokonaan otettu Wikipedian englanninkielisestä artikkelista " Gold (III) trichloride " ( katso luettelo kirjoittajista ) .