Hepatiitti C -virus
Hepatiitti C -virus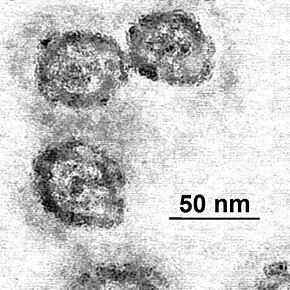 Hiukkaset, jotka ovat samanlaisia kuin hepatiitti C -viruksen.
Hiukkaset, jotka ovat samanlaisia kuin hepatiitti C -viruksen.
| Tyyppi | Virus |
|---|---|
| Ryhmä | Ryhmä IV |
| Perhe | Flaviviridae |
- epätäydellinen kirjoittaja - , päivämäärä määritetään Hepatiitti C
- puutteellinen kirjoittaja - , ajankohta vahvistettava
Hepatiitti C-viruksen ( VHC , Englanti lyhenne HCV "Hepatiitti C -virus" käytetään myös ranskaksi) on pieni vaipallinen virus , noin 60 nm halkaisijaltaan, jonka genomi on lineaarinen yksi - stranded RNA ja polariteetin. Positiivinen sisältämää ikosaedrinen proteiinia kapsidi . Sillä on suuri geneettinen vaihtelu: kuusi erilaista genotyyppiä on karakterisoitu ja seitsemäs on tunnistettu viime aikoina.
Hän on vastuussa hepatiitti C: stä . Sen esiintyvyys Kanadassa, Ranskassa ja Belgiassa on noin 1%; se nousee 22 prosenttiin tietyillä Afrikan alueilla (esimerkiksi Egyptissä). Sen tartuntatapa on pääosin parenteraalinen (pistely, naarmuuntuminen jne.) Ja vähemmässä määrin riskialttiiden seksuaalisten yhteyksien seuraukset. Kanadassa, jossa veripankkien kautta tapahtuvan kontaminaation riskiä ei käytännössä ole, suurin osa infektioista syntyy injektiohuumeiden käytöstä.
Sen tunnetut reseptorit ovat glykosaminoglykaanit , SR-B1 , CD81 (en) ja claudin-1 .
Hän on ainoa edustaja sellaista Hepacivirus kuluessa perheeseen sekä Flaviviridae , johon kuuluu kaksi muuta genre Pestivirus (in) ja flavivirusten .
Nykyään hepatiitti C tartuttaa noin 3% maailman väestöstä eli noin 170 miljoonaa ihmistä.
Sisään lokakuu 2020, fysiologian tai lääketieteen Nobel-palkinto myönnettiin Harvey J.Alterille , Michael Houghtonille ja Charles M.Ricelle hepatiitti C -viruksen löytämisestä.
Rakenne
HCV-hiukkasiin liittyy kroonisen potilaan erittäin pienitiheyksisiä lipoproteiinikomponentteja . Nämä hybridipartikkelit, joita kutsutaan lipoviruspartikkeleiksi tai LVP ( lipo- virohiukkaset ), sisältävät runsaasti triglyseridejä ja sisältävät virus-RNA: n, kapsidiproteiinin, vaippaglykoproteiinit E1E2 sekä alipoproteiinit B ja E.
Viruspartikkeleiden morfologialle oli tunnusomaista immunokapasiteetti, suoraan lähetyselektronimikroskoopin ristikoilla , mikä mahdollisti LVP: iden rakenteen säilyttämisen. Kukin niistä koostuu suuresta nukleokapsidista, joka ympäröi elektronirikasta keskiosaa, todennäköisesti viruksen genomia. Tätä kapsidia ympäröi itsessään epäsäännöllinen, puolipesuaineille herkkä puolikuu, joka todennäköisesti koostuu lipideistä. Hiukkasen koko määräytyy uskottavasti sen lipidikomponenteista. Tulokset viittaavat myös siihen, että potilaiden seerumi sisältää näiden LVP-hiukkasten lisäksi lipoproteiinien kaltaisia proteiineja sekä täydellisiä viruspartikkeleita.
Perimä
Hepatiitti C -viruksen genomi koostuu positiivisesta, yksijuosteisesta RNA: sta, jonka pituus on 9600 nukleotidia , joka koodaa yhtä polyproteiinia, jossa on noin 3000 aminohappoa . HCV-genomi koostuu kolmesta osasta. 5' -koodaamaton alue , joka koostuu 341 - 344 nukleotidista , on rakennettu neljään varsisilmukadomeeniin. Se on hyvin organisoitu ja erittäin konservoitunut alue, jonka samankaltaisuus saavuttaa vähintään 90% HCV-kantojen keskenään. Tämä alue sallii ribosomin 40S-alayksikön sitoutumisen IRES: n (Internal Ribosome Entry Site) tasolla, mikä mahdollistaa translaation aloituksen (itsenäisesti rajattu), lopuksi 5'-NC-alue kuljettaa muodostumiseen tarvittavan signaalipakkauksen nukleokapsidin.
3' -koodaamattomalla alueella on vaihteleva pituus 200 - 235 nt, se koostuu (5 '- 3') kääntämättömästä alueesta, joka on suoraan NS5B-proteiinin alavirtaan ja jonka pituus on 20 - 70 nt. koostumus vaihtelee isolaattien mukaan, mutta voimakkaasti konservoitunut intra-genotyyppisellä tavalla), vaihtelevan pituisen (30 - 150 emäsparin) polyuridyloidun alueen, sitten 98 nukleotidin sisältävän X-alueen, joka on erittäin konservoitunut, välillä. X-alue ja polyuridyloitu alue esiintyvät HCV-tarttuvuudessa.
Lopuksi, avoin lukukehys (tai ORF, avoin lukukehys ) on kooltaan vaihteleva (9024 - 9111 nukleotidia) isolaateista riippuen. Se koodaa polyproteiinia, joka on ko- ja posttranslationaalisesti pilkottu kymmeneksi proteiiniksi, seuraavaa sekvenssiä NH2-Kapsidi-E1-E2-p7-NS2-NS3-NS4A-NS4B-NS5A-NS5B-COOH noudattaen. Sitten tuotetaan kahden tyyppisiä proteiineja, rakenneproteiinit ja ei-rakenteelliset proteiinit.
- Rakenneproteiinit sisältävät kapsidin ja kaksi vaippaglykoproteiinia (E1 ja E2). On myös proteiini, jota kutsutaan p7-proteiiniksi, jolla näyttää olevan keskeinen rooli viruksen morfogeneesissä.
- Ei-rakenteelliset proteiinit tarjoavat entsymaattisia toimintoja, jotka ovat hyödyllisiä virussyklille:
- NS2 , joka on hydrofobinen proteiini, joka on kiinnittynyt solukalvoon (muodostettu NS2 / 3-proteaasista ),
- NS3 , joka on viruksen proteaasin kanssa helikaasi toiminto ( HCV-helikaasin ),
- NS4A , joka on NS3: n transmembraaniproteiinikofaktori ( proteaasi NS3-4A ),
- NS4B , joka on kalvoverkosta vastaava transmembraaniproteiini,
- NS5A , virusfosfoproteiini,
- ja lopuksi virus- NS5B- polymeraasi .
Replikointi
Tarttuva partikkeli sitoutuu solureseptoreihin vaippaglykoproteiinien E1 ja E2 kautta. Eri solujen reseptorit ovat mukana tässä tunnustamista: CD81, joka kuuluu perheeseen ja Tetraspanins , SR-BI (Human scavenger-reseptorin B-tyyppi 1), joka on glykoproteiini, ekspressoituu vallitsevasti maksassa, CLDN-1 on proteiini klaudiini perhe , ilmentyy voimakkaasti myös maksassa, se näkyy SR-BI: n ja CD81: n jälkeen. Cldn6 (in) ja CLDN9 (in) voisi osallistua myös merkintä HCV. Lopuksi OCLDN: llä ja EGF-reseptorilla olisi rooli viruksen soluun sisäänmenemisprosessin aikana.
Kun viruspartikkelin ja sen reseptorin välinen tunnistus on todettu, viruksen verhokäyrän ja solukalvon välillä tapahtuu fuusio happamassa pH-arvossa, mikä aiheuttaa virusvaipan konformaation muutoksen, viruspartikkelin karsimisen ja viruksen vapautumisen. positiivinen RNA viruksen genomista.
Vapautunut RNA (+) transloidaan solukoneiston (ribosomien, soluproteiinien) ansiosta endoplasman verkkokerroksen (ER) tasolla. Syntetisoidut virusproteiinit ovat välttämättömiä viruksen replikaatiolle. Ne liittyvät replikaatiokompleksiin ER-kalvojen tasolla lähellä lipidipisaroita. Sitten RNA (+) toimii matriisinauhana replikaatiotuotteen RNA (-) synteesissä, mikä sallii suuren määrän positiivisten säikeiden synteesin. Lopuksi positiivisten säikeiden sisällyttäminen tuleviin viruspartikkeleihin, jotka koostuvat kapsidiproteiineista sekä E1: stä ja E2: sta, alkavat sitten ER: stä. Viruspartikkelien solunulkoinen vapautuminen suoritetaan sitten eksosytoosirakkuloiden avulla solukalvoon.
Huomautuksia ja viitteitä
- Masahiko Kaito , Shozo Watanabe , Kyoko Tsukiyama-Kohara ja Kenjiro Yamaguchi , " Hepatiitti C -viruspartikkeli havaittu immunoelektronimikroskooppisella tutkimuksella ", Journal of General Virology , voi. 75, n ° 7,1994, s. 1755–1760 ( ISSN 0022-1317 , DOI 10.1099 / 0022-1317-75-7-1755 , luettu verkossa , käytetty 31. lokakuuta 2019 )
- J. M. Pawlotsky ” Hepatiitti C -virus ”, Lääketiede / Science , Vol. 18,2002, s. 303-314 ( DOI 10.1051 / medsci / 2002183303 , lue verkossa )
- 6. (PHAC-PHAC) Kanadan kansanterveysvirasto. 2009. ”hepatiitti C”. EHSSS: Akuutin hepatiitti C -virusinfektion epidemiologia Kanadassa, parannetun hepatiitin kannanvalvontajärjestelmän tulokset. Verkossa. < Http://www.phac-aspc.gc.ca/sti-its-surv-epi/pdf/hcv-epi-fra.pdf > [Tutustuttavissa 1. st Lokakuu 2011]
- (in) T. Sy , herra Jamal , " Epidemiology hepatiitti C (HCV) " , Int. J. Med. Sci. , voi. 3,2006, s. 41–46 ( PMID 16614741 , DOI doi: 10,7150 / ijms 3,41 )
- Kuka. Hepatiitti C - yleinen esiintyvyys (päivitys). Wkly Epidemiol Rec 1999; 49: 421 - 428
- Nobelin palkinnon virallinen verkkosivusto | https://www.nobelprize.org/prizes/medicine/2020/summary/
- Marie-Neige Cordonnier , " Hepatiitti C -virus on viimeinkin paljastettu ", Pour la science , n o 470,joulukuu 2016, s. 7.
- (sisään) Eric Piver, Audrey Boyer, Julien Gaillard Anne Bull, Elodie Beaumont, Philip Roingeard ja Jean-Christophe Meunier, " HCV: n ultrakonstruktionaalinen organisointi tartunnan saaneiden potilaiden verenkierrosta paljasti immunosähkömikroskoopilla jälkispesifinen " , Gut ,11. lokakuuta 2016( DOI 10.1136 / gutjnl-2016-311726 ).
- (in) E. Steinmann , " Hepatitis C-virus p7-proteiini on ratkaiseva kokoonpano ja vapauttaa infektoivien virionien " , PLoS taudinaiheuttajia , voi. 3, n o 7,2007( lue verkossa ).
- (in) J. Evans , T. von Hahn , MD Tscherne , AJ Syder Mr Panis , B. Wölk T. Hatziioannou , JA McKeating , PD Bienasz ja CM Rice , " Claudin-1-hepatiitti C -virus tarvitaan yhteisreseptoreina. myöhäistä vaihetta varten " , Nature , voi. 446,2007, s. 801-805 ( DOI doi: 10.1038 / nature05654 )