Asetoni
| Asetoni | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
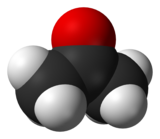 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Puolikehitetty kaava ja asetonin 3D-esitys. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Henkilöllisyystodistus | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| IUPAC-nimi | propan-2-oni | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synonyymit |
β-ketopropane |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100 000 602 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O EY | 200-662-2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 180 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| FEMA | 3326 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hymyilee |
CC (= O) C , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1 / C3H6O / c1-3 (2) 4 / h1-2H3 InChIKey: CSCPPACGZOOCGX-UHFFFAOYAF Std. InChI: InChI = 1S / C3H6O / c1-3 (2) 4 / h1-2H3 Vakio. InChIKey: CSCPPACGZOOCGX-UHFFFAOYSA-N |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ulkomuoto | väritön neste, jolla on tyypillinen haju. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kemialliset ominaisuudet | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kaava |
C 3 H 6 O [Isomeerit] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Moolimassa | 58,0791 ± 0,0031 g / mol C 62,04%, H 10,41%, O 27,55%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| pKa | 20 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dipolaarinen hetki | 2,88 ± 0,03 D | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molekyylihalkaisija | 0,482 nm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fyysiset ominaisuudet | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fuusio | -94,6 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° kiehuu | 56,05 ° C ( 760 mmHg ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Liukoisuus | sekoittuu veteen, etanoliin , dietyylieetteriin , estereihin , bentseeniin , dimetyyliformamidiin , kloroformiin , useimpiin öljyihin | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Liukoisuusparametri δ |
20,3 MPa 1/2 ( 25 ° C ); 22,1 J 1/2 · cm -3/2 ( 25 ° C ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tilavuusmassa |
yhtälö:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Itsesyttymislämpötila lämpötilan | 465 ° C tai 538 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Leimahduspiste |
−18 ° C (suljettu kuppi), −9.4 ° C (avoin kuppi) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Räjähdysrajat ilmassa | 2,15 - 13 tilavuusprosenttia | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kyllästävä höyrynpaine |
228 mbar lämpötilassa 20 ° C 360 mbar lämpötilassa 30 ° C 814 mbar lämpötilassa 50 ° C 1385 mbar lämpötilassa 65 ° C yhtälö:
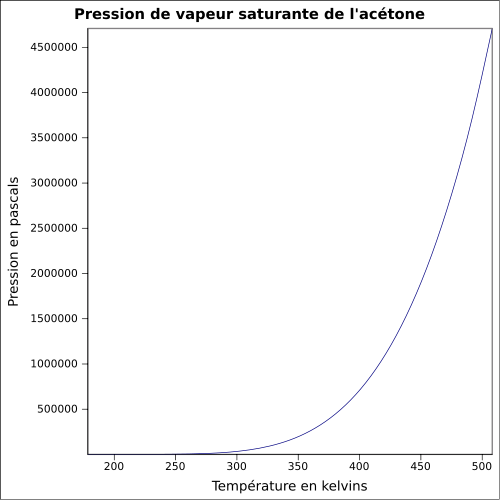
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dynaaminen viskositeetti | 0,32 cP ( 20 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kriittinen piste | 235 ° C , 46,4 atm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kolmoispiste | -94,5 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Äänen nopeus | 1203 m · s -1 kohteeseen 20 ° C: ssa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lämpökemia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 neste, 1 bar | 200,4 J · mol -1 · K -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 kiinteänä aineena | -249,4 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| A f H 0 -kaasu | -218,5 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 neste | -41 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| A fus H ° | 5,7 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ vap H ° | 31,3 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
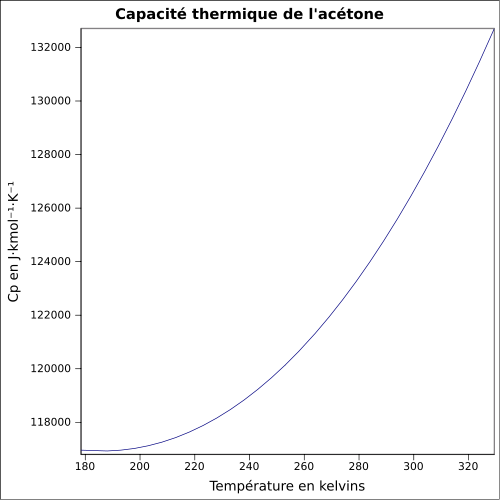
| C s |
125,5 J · mol -1 · K -1 (neste) 75 J · mol -1 · K -1 (kaasu) yhtälö:
yhtälö:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PCS | 1 789,9 kJ · mol -1 (neste) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sähköiset ominaisuudet | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 re ionisaatioenergia | 9,703 ± 0,006 eV (kaasu) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dielektrinen vakio | 21.01 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristallografia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristalliluokka tai avaruusryhmä | Pbcm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Verkon parametrit |
a = 6,393 Å b = 5,342 Å |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Äänenvoimakkuus | 366,55 Å 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Optiset ominaisuudet | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Taitekerroin | 1.3560 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Varotoimenpiteet | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Vaara H225, H319, H336, EUH066, P210, P233, P261, P280, P303 + P361 + P353, P370 + P378, H225 : Helposti syttyvä neste ja höyry H319 : Ärsyttää vakavasti silmiä H336 : Saattaa aiheuttaa uneliaisuutta tai huimausta EUH066 : Toistuva altistuminen voi aiheuttaa ihon kuivumista tai halkeilua P210 : Suojaa lämmöltä / kipinöiltä / avotulelta / kuumilta pinnoilta. - Tupakointi kielletty. P233 : Pidä astia tiiviisti suljettuna. P261 : Vältä pölyn / savun / kaasun / sumun / höyryjen / suihkeen hengittämistä. P280 : Käytä suojakäsineitä / suojavaatetusta / silmiensuojainta / kasvonsuojainta. P303 + P361 + P353 : Jos iho (tai hiukset): Poista kaikki saastuneet vaatteet välittömästi. Huuhtele iho vedellä / suihkulla. P370 + P378 : Tulipalon sattuessa: Käytä ... sammuttamiseen . |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  B2, D2B, B2 : syttyvä neste flash- kohta = -20 ° C suljetun kupin (menetelmä ei ilmoiteta) D2B : Toxic materiaali aiheuttaa muita myrkyllisiä vaikutuksia Silmien ärsytys eläimillä 1,0% tietojen mukaan ainesosa tietojen luettelo |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3 1 0 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kuljetus | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
33 : helposti syttyvä nestemäinen aine (leimahduspiste alle 21 ° C ) YK-numero : 1090 : ASETONI- luokka: 3 Tarra: 3 : Syttyvät nesteet  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hengitys | keuhkoputkien ärsytys, hengitysvaikeudet, juopuminen, samentuminen | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Silmät | punoitus, kipu | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nieleminen | juopumus, pakkomielle | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ekotoksikologia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| DL 50 | > 5000 mg · kg -1 (suun kautta), 20 g · kg -1 (kanin iho) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LogP | -0,24 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hajukynnys | alhainen: 3,6 ppm , 47,5 mg · m -3 ; yläosa: 653 ppm , 1 613,9 mg · m -3 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SI- ja STP- yksiköt, ellei toisin mainita. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Asetoni (substantiivi) on kemian yhdiste yksinkertaisin perheen ketonit . On empiirinen kaava C 3 H 6 O, se on propanaalin isomeeri . Sen virallinen nimi IUPAC on propanoni, mutta se tunnetaan myös nimellä dimetyyliketoni ja beeta-ketopropaani .
Philae Lander ja Rosetta luotain on havainnut tämän kymmenen atomin yhdiste on komeetta 67P / Tchourioumov-Guérassimenko , joka todistaa, että läsnä tämän molekyylin Solar System .
Fysikaalis-kemialliset ominaisuudet
Asetoni on väritön, syttyvä neste, jolla on tyypillinen melko hedelmäinen haju . Sen sulamispiste on -94,6 ° C ja kiehumispiste on 56,05 ° C . Sen ominaispaino on 0,783 ja 0,819 0 ° C: ssa . Se on yhdiste, joka liukenee hyvin veteen (se on napamolekyyli , jolla on lyhyt hiilipitoinen ketju ), etanoliin ja eetteriin . Asetoni on yksinkertaisin johdannainen alifaattisista ketonisarjoista, ja hiili-happi- kaksoissidoksen läsnäolo antaa sille suurimman osan reaktiivisuudestaan. Se on polaarinen aproottinen liuotin .
Asetoni muodostaa hydratsoni , jossa fenyylihydratsiinin ja oksiimi , jossa hydroksyyliamiinin . Vähentäminen mukaan amalgaami ja natrium muuntaa sen isopropyylialkoholi ; hapetus kromihapolla tuottaa hiilimonoksidia ja etikkahappoa . Se reagoi ammoniakin kanssa muodostaen di- ja triasetoniamiinia (en) (TAA). Se myös yhdistää suoraan vetysyanidia , jolloin muodostuu 2-hydroksi-2-metyylivoihappo nitriili . Tämän syaanihydriini , joka on välituote, muunnetaan rikkihappoa (H 2 SO 4) sulfatoitu metakryyliamidiesteri, jonka hydrolyysi tuottaa ammoniumbisulfaattia ja metakryylihappoa .
Vaikutuksesta eri reagenssien, kuten esimerkiksi kalkki , kaustinen potaska tai kloorivetyhappoa , asetoni on muunnetaan kondensaatiotuotteet tuotteita , osaksi mesityylioksidia C 6 H 10 O, In phorone C 9 H 14 O, Jne
Se muunnetaan mesityleeni C 9 H 12(symmetrinen trimetyylibentseeni) tislaamalla rikkihapon läsnä ollessa. Asetonia käytettiin myös tuotantoon värjäys ja indigo keinotekoinen. Jodin , emäksen ja veden läsnä ollessa se antaa jodoformia .
Asetonia käytetään myös jäähdytysnesteenä , koska seos kuivajään (CO 2kiinteä aine) johtaa -78 ° C: seen .
Tuotanto ja synteesi
Synteesi asetoni on kuvannut Jean Béguinin vuonna 1610, joka on valmistettu pyrolyysillä on lyijyasetaattia .
Asetoni, joka oli uutettu aikaisemmin puun pyrolyysin tuloksena syntyneestä pyroligeenihaposta , oli myöhemmin etikkahapon sivutuote .
Vuonna 1915 , Chaim Weizmann löydettiin edullinen tapa saada asetoni tärkkelys , joka helpotti tuotannon kordiitilla , räjähtävä .
Vuonna 2008 asetonin valmistuksessa eniten käytetty menetelmä oli kumeeniprosessi , joka mahdollisti sen (samoin kuin fenolin ) valmistamisen bentseenistä ja propeenista . Asetonin maailmanlaajuinen tuotanto on noin 1,5 miljoonaa tonnia vuodessa.
käyttää
Asetoni on liuotin, jota käytetään laajalti teollisuudessa ja laboratorioissa, koska sen etuna on liukeneminen erityisen nopeasti useilla orgaanisilla lajeilla ja koska se sekoittuu veteen. Se on myös muovien , lääkkeiden ja muiden synteettisen teollisuuden tuotteiden valmistuksen pohja . Asetonia käytetään erityisesti teollisuudessa bisfenoli A: n tuottamiseksi reaktiossa fenolin kanssa . Bisfenoli A on tärkeä osatekijä monissa polymeerejä , kuten polykarbonaatti- tai polyuretaani sekä epoksihartsit . Asetonia käytetään myös laajamittaisesti asetyleenin kuljetuksessa ja varastoinnissa : huokoisen materiaalin sisältävä astia täytetään asetonilla, johon aseteeni sitten liuotetaan (yksi litra asetonia liuottaa noin 250 litraa asetyleeniä).
Asetoni on myös pääkomponentti joillekin kynsilakan poistamiseen käytetyille liuottimille . Sitä käytetään myös liuottimena liiman ja selluloosakuitujen liuottamiseen . Asetonia ei suositella käytettäväksi tekokuiduissa (asetaatti, triasetaatti ja akryyli). Asetonia käytetään myös teolliseen rasvanpoistoon.
Asetonikylpyjä käytetään kappaleiden valmistamiseen plastinoinnin aikana .
Biologinen ja mikrobiologinen näkökohta
Asetoni on kehon ketoni , jota tavallisesti esiintyy hyvin pieninä määrinä virtsassa ja veressä . Suurempia määriä löytyy paaston jälkeen ja diabeetikoilla (joiden verensokerin hallinta on heikkoa), joilla on vaikea insuliinipuutos ; Asetonin aiheuttama hedelmäinen haju hengityksessä on yksi diabeettisen ketoasidoosin oireista .
Asetonia esiintyy luonnollisesti kasveissa , puissa , tulivuorikaasuissa , metsäpaloissa ja eläinrasvan hajoamistuotteena. Sitä on pakokaasuissa , tupakassa ja kaatopaikoissa . Ihmisen toiminta tuottaa sitä enemmän kuin luonto.
Se on yksi niistä syntyvien hajotustislauksesta puu , sokeri , selluloosa , jne. , ja tästä syystä sitä esiintyy aina raakapuun hengessä, josta suuri osa voidaan ottaa talteen jakotislauksella .
Terveys- ja turvallisuusvaikutukset
Altistuminen asetonille voi aiheuttaa ihoärsytystä tai -vaurioita . Suuri ja pitkäaikainen altistuminen voi aiheuttaa tajuttomuutta .
Laboratorioeläimillä tehdyt tutkimukset ovat osoittaneet munuaisten , maksan ja hermojen sekä sikiön vaurioita pitkäaikaisessa altistuksessa suurille annoksille asetonia. Uroseläimillä oli myös lisääntymishäiriöitä tai jopa kyvyttömyyksiä. Ei tiedetä, näkevätkö tällaiset vaikutukset ihmisillä.
Asetonin myrkyttömät millimolaariset annokset osoittavat kouristuksia estävää vaikutusta epilepsian eläinmalleissa. Raja-arvo (OELP) on asetettu 500 ppm ( 1210 mg · m -3 ) että Euroopan unionin .
Asetonin hengittäminen voi aiheuttaa keuhkoputkien ärsytystä, hengitysvaikeuksia ja asetonin nieleminen voi aiheuttaa myrkytystä ja samentumista .
Ammatillinen toksikologia
Lähde.
Suurilla pitoisuuksilla asetoni aiheuttaa keskushermostoa lamaavia vaikutuksia ja limakalvojen ärsytystä. Toistuva ihoaltistus voi laukaista kosketusihottuman. Tulipalo- ja räjähdysvaarojen takia asetonia varastoitaessa ja käsiteltäessä on toteutettava ennalta ehkäiseviä ja suojaavia toimenpiteitä: Henkilökohtainen suojaus valitaan työaseman olosuhteiden mukaan, eivätkä ne saa olla staattisen sähkön lähde. Alkuperäisten ja säännöllisten käyntien aikana kliinisessä tutkimuksessa etsitään neurologisten, silmä-, iho- tai kroonisten hengitysvaurioiden merkkejä. Naiset, jotka haluavat tulla raskaaksi, altistuvat mahdollisimman vähän hedelmällisyyden punalippujen takia.
Huomautuksia ja viitteitä
- ASETONI , kemiallisten aineiden turvallisuuden kansainvälisen ohjelman käyttöturvallisuustiedotteet, joita on käyty 9. toukokuuta 2009.
- (en) " ASETONI " , vaarallisten aineiden tietopankissa (käytetty 3. helmikuuta 2010 ) .
- (in) David R. LiDE , CRC Handbook of Chemistry and Physics , Boca Raton, CRC Press / Taylor ja Francis,17. kesäkuuta 2008, 89 th ed. , 2736 Sivumäärä ( ISBN 9781420066791 , verkkoesitys ) , s. 9-50.
- (en) Yitzhak Marcus, The Properties of Solvents , voi. 4, Englanti, John Wiley & Sons,1999, 239 Sivumäärä ( ISBN 0-471-98369-1 ).
- laskettu molekyylimassa välillä " Atomic painot Elements 2007 " on www.chem.qmul.ac.uk .
- Asetoni , INRS, toksikologinen taulukko FT3, 2008.
- (in) James E. Mark , Physical Properties of Polymer Handbook , Springer,2007, 2 nd ed. , 1076 Sivumäärä ( ISBN 0-387-69002-6 , lue verkossa ) , s. 294.
- (en) Robert H. Perry ja Donald W. Green , Perry's Chemical Engineers 'Handbook , Yhdysvallat, McGraw-Hill,1997, 7 th ed. , 2400 Sivumäärä ( ISBN 0-07-049841-5 ) , s. 2-50.
- (in) William M. Haynes , CRC Handbook of Chemistry and Physics , Boca Raton, CRC Press / Taylor ja Francis,1. st heinäkuu 2010, 91 th ed. , 2610 Sivumäärä ( ISBN 9781439820773 , online-esitys ) , s. 14–40.
- (in) Carl L. leuat , Handbook of termodynaamiset kaaviot , Voi. 1, Huston, Texas, Persianlahden pubi. Co,1996( ISBN 0-88415-857-8 ).
- (in) David R. LiDE , CRC Handbook of Chemistry and Physics , Boca Raton, CRC Press,18. kesäkuuta 2002, 83 th ed. , 2664 Sivumäärä ( ISBN 0849304830 , online-esitys ) , s. 5-89.
- (in) David R. LiDE , CRC Handbook of Chemistry and Physics , Boca Raton, CRC Press / Taylor ja Francis,17. kesäkuuta 2008, 89 th ed. , 2736 Sivumäärä ( ISBN 9781420066791 , verkkoesitys ) , s. 10-205.
- ” Asetoni ” , osoitteessa www.reciprocalnet.org (käytetty 12. joulukuuta 2009 ) .
- Sigma-Aldrichin toimittama käyttöturvallisuustiedote, kuultu28. syyskuuta 2019.
- " Asetoni " tietokannassa kemikaalien Reptox että CSST (Quebec organisaatio, joka vastaa työsuojelun), pääsee 25 huhtikuu 2009.
- (sisään) " Asetoni " sivustolla hazmap.nlm.nih.gov ( katsottu 14. marraskuuta 2009 ) .
- "asetoni" , ESIS: ssä (kuultu10. helmikuuta 2009).
- (sisään) Fred Goesmann Helmut Rosenbauer, Jan Hendrik Bredehöft Michel Hut, Pascale Ehrenfreund Thomas Gautier, Chaitanya Giri, Harald Krüger, Lena Roy, Alexandra J.MacDermott, Susan McKenna-Lawlor, Uwe J.Meieroisrich Guillermo M Muñoz Caro , Reinhard Roll, Andrew Steele, Harald Steininger, Robert Sternberg, Cyril Szopa, Wolfram Thiemann ja Stephan Ulamec, " Orgaaniset yhdisteet komeetalla 67P / Churyumov-Gerasimenko paljastaa COSAC-massaspektrometria " , Science , voi. 349, n ° 6247,31. heinäkuuta 2015( DOI 10.1126 / science.aab0689 , lue verkossa ).
- Jean Béguin, käännös. Jean Lucas Du Roi, Les elemens de chymie, de maistre Iean Beguin almosnier du Roy , Mathieu Le Maistre, ruë sainct Iean de Laterran à l'Arbre sec,1620( lue verkossa ).
- Likhodii et ai. , 2003.
- INRS FT3 toksikologinen arkki ,lokakuu 2018.
Katso myös
Ulkoiset linkit
- Kansainvälinen turvakortti , cdc.gov .
- (en) Asetoni , osoitteessa webbook.nist.gov .
- (en) Vaarallisten kemikaalien tietokanta osoitteessa ull.chemistry.uakron.edu .