Asetyleeni
| Asetyleeni | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Asetyleenin kolmiulotteinen rakenne | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Henkilöllisyystodistus | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| IUPAC-nimi | etyni | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100 000 743 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O EY | 200-816-9 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 6326 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hymyilee |
C # C , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1S / C2H2 / c1-2 / h1-2H |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ulkomuoto | väritön kaasu liuotettuna asetoniin paineen alla | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kemialliset ominaisuudet | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Raaka kaava |
C 2 H 2 [Isomeerit] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Moolimassa | 26,0373 ± 0,0017 g / mol C 92,26%, H 7,74%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fyysiset ominaisuudet | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fuusio | −80,7 ° C ( kolmoispiste ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° kiehuu | -84,7 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Liukoisuus | 1,185 g l −1 (vesi, 20 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tilavuusmassa |
yhtälö:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Itsesyttymislämpötila lämpötilan | 305 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Leimahduspiste | Syttyvä kaasu | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Räjähdysrajat ilmassa | 2,3 - 100 tilavuusprosenttia | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kyllästävä höyrynpaine | ajan 20 ° C : 4460 kPa
yhtälö:
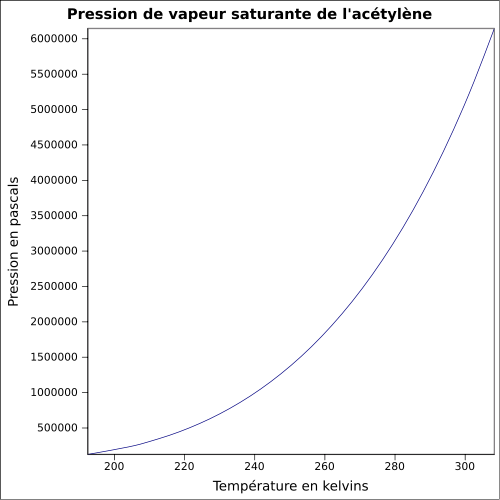
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kriittinen piste |
35,2 ° C 61,38 bar 0,1122 l / mol |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kolmoispiste | -80,8 ° C on 1,2825 bar | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lämpökemia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0- kaasu, 1 bar | 200,93 J mol −1 K −1 ( 1 bar ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| A f H 0 -kaasu | 226,73 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C s |
44,04 J mol -1 K -1 ajan 25 ° C: ssa
yhtälö:
yhtälö:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PCS | 1301,1 kJ · mol -1 ( 25 ° C , kaasu) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sähköiset ominaisuudet | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 re ionisaatioenergia | 11.400 ± 0.002 eV (kaasu) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristallografia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristalliluokka tai avaruusryhmä | Pa 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Verkon parametrit |
a = 6,140 Å b = 6.140 Å |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Äänenvoimakkuus | 231,48 Å 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Varotoimenpiteet | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Vaara H220, EUH006, H220 : Erittäin helposti syttyvä kaasu EUH006 : Räjähdysvaara joutuessaan kosketuksiin ilman kanssa |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
   A, B1, F, A : Paineistetun kaasun kriittinen lämpötila = 36,3 ° C B1 : Syttyvän kaasun alempi syttymisraja = 2,5% F : Voimakkaasti hajoavan reaktion alainen vaarallisen reaktiivinen materiaali Paljastuminen 1,0% luokituskriteerien mukaan Kommentit: Katso myös liuenneen asetyleenin WHMIS-luokitus . |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 4 0 3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kuljetus | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
239 : syttyvä kaasu, joka voi spontaanisti tuottaa väkivaltaisen reaktion YK-numero : 1001 : LIUKENEMATON ASETYLEENI Luokka: 2.1 Luokituskoodi: 4F : Paineessa liuennut kaasu, syttyvä; Etiketti: 2.1 : Syttyvät kaasut (vastaa ison kirjaimen F osoittamia ryhmiä); 
- YK-numero : 3374 : ASETYLEENI ILMAN LIUOTTIMIA Luokka: 2.1 Luokituskoodi: 2F : Nestekaasu, syttyvä; Etiketti: 2.1 : Syttyvät kaasut (vastaa ison kirjaimen F osoittamia ryhmiä);  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ekotoksikologia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LogP | 0,37 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hajukynnys | matala: 226 ppm korkea: 2584 ppm |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SI- ja STP- yksiköt, ellei toisin mainita. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Asetyleeni (kutsutaan etyynistä jota nimikkeistö IUPAC ) on kemiallinen yhdiste hiilivety luokan alkyynien on empiirinen kaava C 2 H 2. Sen löysi Edmund Davy vuonna Englannissa vuonna 1836 . Se on yksinkertaisin alkyyni, joka koostuu kahdesta hiiliatomista ja kahdesta vedystä . Kaksi hiiliatomia on kytketty kolmoissidoksella, joka sisältää suurimman osan sen kemiallisesta energiasta.
Kuvaus
Berthelot , vuonna 1862 , oli ensimmäinen tiivistetään asetyleeni, laitteessa nimeltä "Berthelot muna", tuottamalla valokaaren kahden elektrodien ja grafiitti kylpee ilmakehässä vedyn : 2 C + H 2 → C 2 H 2
Asetyleeni on väritön kaasu , käytännöllisesti katsoen hajuton puhtaana (mutta sille on yleensä ominaista luontainen valkosipulin haju, joka tulee epäpuhtauksista, erityisesti fosfiinista, kun sitä valmistetaan kalsiumkarbidista ).
Asetyleeni on erittäin helposti syttyvä ajan normaalissa lämpötilassa ja paineessa . Se on endoenerginen suhteessa hiileen ja vetyyn ja voi hajota spontaanisti, räjähdysmäisesti, kun paine on yli 100 kPa , ja jopa muutamaan baariin, missä tämä spontaani hajoaminen väistämättä tapahtuu . Tästä syystä se varastoidaan liuotettuna asetoniin tai dimetyyliformamidiin (DMF), jotka itse sisältyvät huokoiseen stabilointimateriaaliin.
käyttää
Asetyleenin sovellukset:
- Korkea hiilipitoisuus antaa erittäin valaisevan liekin, jota käytetään esimerkiksi asetyleenilampuissa kaivostyöläisille tai speleologeille.
- Asetyleenin korkea palamislämpö saavuttaa korkeat lämpötilat ( 3200 ° C puhtaassa hapessa), mikä tekee siitä ihanteellisen ehdokkaan hitsauksen polttoaineeksi. Yksi asetyleenin palamisen erikoispiirteistä on sen kaksivaiheinen palaminen: asetyleeni reagoi ensin hapen kanssa, jolloin saadaan hiilimonoksidia ja vetyä , sitten nämä tuotteet reagoivat toisessa vaiheessa hiilidioksidin ja veden muodostamiseksi. Hiilimonoksidi ja vety ovat pelkistäviä kaasuja, mikä tekee niistä suosittuja reagensseja teräshitsauksessa vähentämään rautaoksideja, jotka johtuvat raudan ja hapen reaktiosta korkeassa lämpötilassa, mikä mahdollistaa hitsin paremman homogenoitumisen ja siten paremman laadun. Hitsaus asetyleeni mahdollistaa kokoamisen eri metalleja ( teräkset , ruostumaton teräs, kupari seokset ), mutta myös tietyissä olosuhteissa alumiini seostetaan piitä .
- Asetyleeniä käytetään myös polttoaineena analyyttisissä laitteissa. Itse asiassa atomiabsorptiospektrometriassa (AAS), joka liittyy erilaisiin hapettimiin (ilma, puhdas happi, typpioksidi), se sallii tyypillisesti maa-alkalimetallien ionisoinnin ja määrittää niiden pitoisuuden Beer-Lambert-lain ansiosta .
- Asetyleeniä käytetään myös hapenleikkauspolttimissa. Propaani on kuitenkin edullinen, koska se on halvempaa. Mutta erittäin paksuissa leikkauksissa asetyleeni on välttämätöntä teräksen riittävän lämmittämiseksi ja liekinleikkauksen aloittamiseksi pienellä leveydellä.
- Asetyleenin saattaminen reagoimaan suolahapon kanssa on yksi tapa tuottaa vinyylikloridia ( polyvinyylikloridimonomeeri ).

Fysikaalis-kemialliset ominaisuudet
Asetyleenin kemialliset ominaisuudet selitetään suurelta osin kolmoissidoksen läsnäololla, joka johtuu yhden s- sidoksen päällekkäisyydestä (joka johtuu kahden sp- orbitaalin fuusiosta ) ja kahdesta p- sidoksesta, joka johtuu kahden 2p- orbitaalin sulautumisesta . Tämä 0,124 nm pitkä sidos, jolle on tunnusomaista 811 kJ : n energia , on vähemmän vakaa kuin yksittäiset (614 kJ ) ja kaksoissidokset (347,3 kJ ) ja on siksi reaktiivisempi.
Asetyleenin reaktiot
- Asetyleeni ja monoalkyyliasetyleenit ovat ainoat hiilivedyt, joilla on happoinen vety ja jotka voidaan vaihtaa metalliksi.
- Jotkut asetylenidit kuten räjähtävät iskuissa.
- Asetyleeni reagoi syaanivetyhapon kanssa muodostaen akryylinitriilin , akryylinitriilibutadieenistyreenin (ABS) ja styreeni-akryylinitriilin (SAN) monomeerin .
- Asetyleeni antaa bentseeni , jonka polymerointi alle lämmön vaikutuksesta.
- Jonka dimeroituminen läsnä ollessa katalyyttien, vinyyliasetyleeniä saadaan johon kloorivetyä lisätään , jotta saadaan kloropreeni, joka on polykloropreeni tai neopreeni monomeeriä .
Tuotanto ja synteesi
Asetyleeniä ei ole luonnossa (muita alkyynejä esiintyy satunnaisesti hiilivedyissä). Tärkeimmät teolliset menetelmät asetyleenin tuottamiseksi ovat:
Karbokemiallinen menetelmä
Raaka-aineina käytetään kalkkikiveä ja koksia tai hiiltä. Sulatetun reaktioväliaineen läpi kulkevalla sähkövirralla kuumennetussa korkean lämpötilan uunissa ( vähintään 1700 ° C ) tuotetaan kalsiumkarbidia reaktioiden mukaisesti: CaCO 3 → CaO + CO 2, CaO + 3 C + 108300 kaloria → SERTIn 2 + CO.
Karbidi reagoi käyttäjän kanssa tuottaen asetyleeniä, 1 kg karbidia yhdistettynä 562,5 g : aan vettä, jolloin vapautuu 350 l asetyleeniä: CaC 2 + 2 H 2 O → C 2 H 2 + Ca (OH) 2 + 31 000 kaloria.
Metaanin osittainen palaminen
Metaanin osittainen palaminen tuottaa myös asetyleeniä: 3 CH 4 + 3 O 2 → C 2 H 2 + CO + 5 H 2 O.
Alkaanien dehydraus
Raskaat maaöljyn ja maakaasun alkaanit krakataan kevyemmiksi molekyyleiksi, jotka dehydratoidaan korkeissa lämpötiloissa: C 2 H 6 → C 2 H 2 + 2 H 2.
Huomautuksia ja viitteitä
- ASETYLEENI , kemiallisten aineiden turvallisuutta koskevan kansainvälisen ohjelman käyttöturvallisuustiedote (t) , kuultu 9. toukokuuta 2009
- laskettu molekyylimassa välillä " Atomic painot Elements 2007 " on www.chem.qmul.ac.uk .
- (en) David R. Lide , CRC Handbook of Chemistry and Physics, 89. painos , Boca Raton, CRC Press / Taylor ja Francis,2009, "Orgaanisten yhdisteiden fyysiset vakiot"
- Merkintä "Asetyleeni" IFA: n (saksalainen työturvallisuudesta ja -terveydestä vastaavan elimen) kemikaalitietokantaan GESTIS ( saksaksi , englanniksi ), käytetty 14. huhtikuuta 2009 (vaaditaan JavaScriptia)
- (en) Robert H. Perry ja Donald W. Green , Perry's Chemical Engineers 'Handbook , USA, McGraw-Hill,1997, 7 th ed. , 2400 Sivumäärä ( ISBN 0-07-049841-5 ) , s. 2-50
- Clark, AM; Din, F., Kiinteiden, nestemäisten ja kaasumaisten faasien tasapainot matalassa lämpötilassa binaarijärjestelmissä asetyleeni - hiilidioksidi, asetyleeni - eteeni ja asetyleeni - etaani, trans. Faraday Soc., 1950, 46, 901.
- Tsonopoulos, C.; Ambrose, D., alkuaineiden ja yhdisteiden höyrynestekriittiset ominaisuudet. 6. Tyydyttymättömät alifaattiset hiilivedyt, J. Chem. Eng. Data, 1996, 41, 645-656.
- " Asetyleeni " , osoitteessa http://www.nist.gov (käytetty 14. huhtikuuta 2009 )
- (in) Carl L. leuat, Handbook of termodynaamiset kaaviot , Voi. 1, 2 ja 3, Huston, Texas, Gulf Pub. Co,1996( ISBN 0-88415-857-8 , 978-0-88415-858-5 ja 978-0-88415-859-2 )
- (in) David R. LiDE , CRC Handbook of Chemistry and Physics , Boca Raton, CRC Press,18. kesäkuuta 2002, 83 th ed. , 2664 Sivumäärä ( ISBN 0849304830 , online-esitys ) , s. 5-89
- (in) David R. LiDE, Handbook of Chemistry and Physics , CRC,2008, 89 th ed. , 2736 Sivumäärä ( ISBN 978-1-4200-6679-1 ) , s. 10-205
- " Asetyleeni " , osoitteessa www.reciprocalnet.org (käytetty 12. joulukuuta 2009 )
- Indeksinumero EY-asetuksen N: o 1272/2008 liitteen VI taulukossa 3.1 (16. joulukuuta 2008)
- " Asetyleeni " CSST: n (Quebecin työturvallisuudesta ja -terveydestä vastaava organisaatio) kemikaalien tietokannassa Reptox .
- " Asetyleeni " osoitteessa hazmap.nlm.nih.gov (käytetty 14. marraskuuta 2009 )
- Nowak Ph. (1999) - "L ' acétylène ", " Le P'tit Usania n o 7 " , USAN (käytetty 5. tammikuuta 2021 ) ( ISSN 1292-5950 ) , USAN, Nancy, s. 1
Katso myös
Aiheeseen liittyvät artikkelit
- Asetyleenihydraasi
- Alcyne
- Asetyleenilamppu
- Louis Bleriot
- Frédéric Chaplet
- Henri moissan
- Walter Reppe











