Hiilidioksidi
| Hiilidioksidi | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Hiilidioksidin rakenne. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Henkilöllisyystodistus | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| IUPAC-nimi | Hiilidioksidi | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synonyymit |
Hiilidioksidi, hiilidioksidi |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100 004 271 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O EY | 204-696-9 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ATC-koodi | V03 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 280 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ChEBI | 16526 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o E | E290 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hymyilee |
C (= O) = O , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1S / CO2 / c2-1-3 InChIKey: CURLTUGMZLYLDI-UHFFFAOYSA-N |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ulkomuoto | Nesteytetty, väritön ja hajuton paineistettu kaasu | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kemialliset ominaisuudet | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kaava |
C O 2 [Isomeerit] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Moolimassa | 44,0095 ± 0,0014 g / mol C 27,29%, O 72,71%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fyysiset ominaisuudet | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fuusio | −78,48 ° C (sublimaatio 760 mmHg ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° kiehuu | −56,6 ° C ( 5,12 atm ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Liukoisuus | veteen 20 ° C: ssa : 88 ml / 100 ml alle 1 bar CO 2, Eli 1,69 g / kg vettä (3,35 g ajan 0 ° C: ssa , 0,973 g ajan 40 ° C: ssa ja 0,576 g ajan 60 ° C: ssa ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tilavuusmassa |
1,87 kg m -3 ( kaasu ajan 15 ° C: ssa 1,013 bar ) ilmaa tiheämpiä yhtälö:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kyllästävä höyrynpaine |
5720 kPa ( 20 ° C ) 569,1 mmHg ( -82 ° C ); yhtälö:

|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dynaaminen viskositeetti | 0,07 mPa s ajan -78 ° C: ssa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kriittinen piste | 31,3 ° C ; 72,9 atm ja 0,464 g cm −3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kolmoispiste | −56,6 ° C - 5,11 atm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lämmönjohtokyky | 3,840 x 10 -5 cal cm -1 s -1 K -1 ajan 20 ° C: ssa |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Äänen nopeus | 259 m s −1 ( 0 ° C , 1 atm ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lämpökemia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 kaasu | −393,52 kJ mol −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
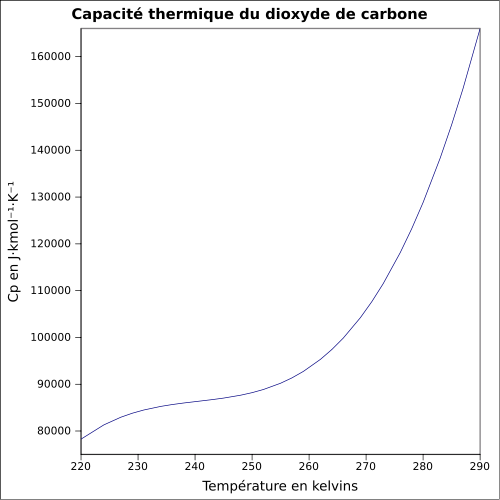
| C s |
yhtälö:
yhtälö:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sähköiset ominaisuudet | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 re ionisaatioenergia | 13,773 ± 0,002 eV (kaasu) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristallografia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristalliluokka tai avaruusryhmä | P42 / mnm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Mesh -parametrit |
a = 3,535 Å b = 3,535 Å |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Äänenvoimakkuus | 51,73 Å 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Optiset ominaisuudet | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Taitekerroin | 100045 (1 atm) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Varotoimenpiteet | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Varoitus H280 , P403 ja P410 H280 : Sisältää paineen alaista kaasua; voi räjähtää kuumennettaessa P403 : Varastoi paikassa, jossa on hyvä ilmanvaihto. P410 : Suojaa auringonvalolta. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 TO, : Puristettu kaasu kriittinen lämpötila = 31,1 ° C Disclosure 1,0% mukaan ainesosan tietojen luettelo |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kuljetus | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
20 : tukehduttava kaasu tai kaasu, joka ei aiheuta toissijaista riskiä YK -numero : 1013 : HIILIDIOKSIDI Luokka: 2.2 Luokituskoodi: 2A : Nesteytetty kaasu, tukehduttava; Etiketti: 2.2 : Palamattomat, myrkyttömät kaasut (vastaa ryhmiä, jotka on merkitty A: lla tai isolla O: lla); 
22 : jäähdytetty nesteytetty kaasu, tukehtuva YK-numero : 2187 : JÄÄHDYTETTY NESTEINEN Hiilidioksidi Luokka: 2.2 Luokituskoodi: 3A : Jäähdytetty nesteytetty kaasu, tukehtuva; Etiketti: 2.2 : Palamattomat, myrkyttömät kaasut (vastaa ryhmiä, jotka on merkitty A: lla tai isolla O: lla); 
- YK -numero : 1845 : HIILIDIOKSIDI, KIINTEÄ; tai CARBON SNOW -luokka: 9 Luokituskoodi: M11 : Muut aineet, jotka aiheuttavat riskin kuljetuksen aikana, mutta jotka eivät täytä minkään muun luokan määritelmää. Tag: 9 : Erilaiset vaaralliset aineet ja esineet  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SI- ja STP- yksiköt, ellei toisin mainita. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Hiilidioksidi , joka tunnetaan myös hiilidioksidia tai hiilidioksidin on epäorgaaninen yhdiste , jonka kemiallinen kaava on CO 2The molekyyli , jolla on lineaarinen rakenne, joka on muotoa O = C = O . Se esitetään lämpötilan ja paineen vakio -olosuhteissa , kuten väritön, hajuton kaasu .
CO 2on käyttää anabolian ja kasvien tuottamiseksi biomassan läpi fotosynteesin , prosessi, joka käsittää vähentää hiilidioksidin veden ansiosta valon energia vastaanotetaan Sun ja vangiksi klorofylli , vapauttamalla happea ja tuottaa monosakkaridit , ja ensimmäinen glukoosia jonka Calvin sykli . CO 2vapautetaan, läpi Krebs syklin , jota hajoamista on kasvien , eläinten , sienten (sienet, tai sienet ) ja mikro-organismit . Tämä katabolian erityisesti hapettaa lipidit ja hiilihydraatit vettä ja hiilidioksidia kanssa hapen ja ilman tuottaa tehoa ja vähennetään voima, vastaavasti muodossa ATP ja NADH + H + . CO 2on siis olennainen osa planeettamme hiilenkiertoa . Se on tuotettu myös palamisen ja fossiilisten polttoaineiden , kuten hiilen , maakaasun ja öljyn , sekä että orgaanisen aineen yleisesti. Se on ei - toivottu sivutuote suurissa teollisissa prosesseissa.
Merkittäviä määriä CO 2myös tulivuoret ja muut geotermiset ilmiöt , kuten geyserit, hylkäävät ne .
Tammikuussa 2021 Maan ilmakehään sisälsi 415,13 ppmv (miljoonasosaa tilavuudesta) CO 2tai 0,04153%. Tämä taso oli 283,4 ppmv 1839 mukaan jään ydintä otettu Antarktis , kokonaiskasvu oli noin 46% 182 vuosi.
CO 2on merkittävä kasvihuonekaasu , läpinäkyviä näkyvän valon , mutta absorboivat infrapuna-alueella , niin että se pyrkii estämään uudelleen päästöt tilaan lämpöenergian vastaanotetun päällä vaikutuksesta auringon säteilyn . Se on vastuussa noin 26%: sta kasvihuoneilmiöstä työssä maan ilmakehässä ( vesihöyrystä 60%); lisäämällä sen pitoisuus on osittain vastuussa lämpenemistä havaittiin ympäri planeettaa viime vuosikymmeninä on XX : nnen vuosisadan. Lisäksi happamoitumisen johtuvat liukeneminen ilmakehän hiilidioksidia voi vaaranna monien merieliöiden ennen loppua XXI th -luvulla.
Fysikaalis -kemialliset ominaisuudet
Ilmakehän paineessa, se sublimoituu on -78,5 ° C: ssa (muutos kiinteästä kaasumaiseen tilaan), mutta ei sula (muutos kiinteästä nestemäiseen tilaan).
Nestefaasi voi olla olemassa vain minimipaineessa 519 kPa ( ts. 5,12 atm ) ja lämpötila-alueella -56,6 ° C ( kolmoispiste ) enintään 31,1 ° C lämpötilassa 7,38 MPa ( ts. 72,8 atm ) ( kriittinen) kohta ).
Kyllästävä höyrynpaine
|
| Siirtyminen | Lämpötila | Piilevä lämpö |
|---|---|---|
| Höyrystys | 0 ° C | 234,5 kJ kg −1 |
| Höyrystys | -16,7 ° C | 276,8 kJ kg −1 |
| Höyrystys | -28,9 ° C | 301,7 kJ kg −1 |
| Sulautuminen | -56,6 ° C | 199 kJ kg −1 |
CO 2: ta olisi vähintään viisi kiinteää molekyylifaasia (olemassa "alhaisessa" paineessa, alle 30-60 GPa) ja kolme kiinteää polymeerifaasia (korkeammissa paineissa) . :
- molekyylivaiheet:
- I: “kuivajää”, jopa 800 K ja 11–12 GPa
- II: 400–5600 K ja paine 12–50 GPa
- III: yli 12 GPA ja alle 500 K
- IV: yli 11 GPa ja yli 500 K
- VII: 600–900 K (jopa 1000 K, ylikriittinen osa mukaan lukien) ja 11–20 GPa
- polymeerifaasit:
- V: yli 30 GPa ja yli noin 1300 K
- VI: lämpötila välillä noin 500 K ja 1300 K ja paine on suurempi kuin 30 (1300 K) 50 GPa: n (500 K)
- amorfinen, alle 500 K ja yli 50 GPa
Vesiliukoisuus
CO 2liukenee veteen ja muodostaa hiilihappoa H 2 CO 3 : CO 2 (aq)+ H 2 O (l) H 2 CO 3 (aq), Jossa K h = [H 2 CO 3] / [CO 2] ≈ 1,70 x 10 -3 kohteeseen 25 ° C: seen .
Se on myös rasvaliukoinen (liukenee rasva -aineisiin).
Hiilihappo on vain kohtalaisen vakaa ja se helposti hajoaa H 2 Oja CO 2. Toisaalta, kun hiilidioksidi liukenee emäksiseen vesiliuokseen (sooda, kalium jne.), Emäs deprotonoi hiilihapon muodostaen vetykarbonaatti- ionin HCO-
3, jota kutsutaan myös bikarbonaatti- ioniksi , sitten karbonaatti- ioni CO2-
3. Tällä tavalla, liukoisuutta CO 2on huomattavasti lisääntynyt. Kaliumkarbonaattia K 2 CO 3Esimerkiksi on liukoisuus on 1,12 kg / l vettä 20 ° C: ssa .
Näin kalkkikivi liukenee veteen pH- alueella , jolla happoinen vetykarbonaatti on stabiili, jolloin saadaan vetykarbonaatin (-vesien) (kalsiumin ja magnesiumin ...) liuos. Siksi se todennäköisesti saostuu, kun CO 2liuenneesta on poistettu kaasu, kuten muodostettaessa stalagmiitteja ja tippukivipylväitä . Kalkkikivessä on siis CO 2 : n läsnä ollessa, liukoisuus, joka laskee lämpötilan noustessa, kuten kaasut ja toisin kuin useimmat kiinteät aineet (joiden liukoisuus yleensä kasvaa lämpötilan mukana).
Tietyissä olosuhteissa (korkea paine + matala lämpötila) CO 2voidaan loukata ns. clathrate- vesihäkkeihin . Se on yksi mahdollinen keino teollisuuden erottaminen CO 2sisältyvät esi- tai jälkipolttokaasuun . Se on myös yksi suunniteltuihin CO 2 sitomiseenteollisuus- tai geologisen varastoinnin tutkittu, mahdollisesti korreloi meriveden suolanpoisto (teoreettisesti se voi jopa korvata metaanin hydraatti metaani ).
Tietohistoria
Hiilidioksidi on yksi ensimmäisistä kaasuista (yhdessä vesihöyryn kanssa ), jota kuvataan ilmasta erillisenä aineena. Vuonna XVII th -luvulla , kemisti ja lääkäri Flanderin Jan Baptist van Helmont havaittu, että palava hiili suljetussa astiassa, massa tuloksena tuhka on pienempi kuin hiiltä. Hänen tulkinta oli, että puuttuva massa oli transmuted osaksi näkymättömän ainetta, jota hän kutsui " kaasua " tai Spiritus sylvestre ( "villi henki").
Skotlantilainen kemisti ja fyysikko Joseph Black tutki hiilidioksidin ominaisuuksia tarkemmin 1750 -luvulla . Hän huomasi, että kuumentamalla tai kaatamalla happoa kalkkikivelle ( kalsiumkarbonaatista koostuva kivi ), tuloksena oli kaasun päästö, jonka hän kutsui "kiinteäksi ilmaksi", mikä heikensi vielä tuolloin opetettua flogistonin teoriaa . Hän huomasi, että se on ilmaa tiheämpää eikä se voi tukea liekkiä eikä eläimen elämää. Musta myös havainneet, että kun hiilidioksidia syötetään kalkkikiveä liuokseen ( kalsiumhydroksidin ), joka on sakka kalsiumkarbonaattia tuloksia. Hän käytti tätä ilmiötä havainnollistaakseen, että hiilidioksidia syntyy eläinten hengityksellä ja mikrobien käymisellä.
Vuonna 1772 englantilainen kemisti Joseph Priestley julkaisi työn nimeltä Veden kyllästäminen kiinteällä ilmalla , jossa hän kuvasi rikkihapon (tai "vitrioliöljyn, kuten sitä silloin kutsuttiin) kaatamista liituun", hiilen tuottamiseksi. sitten pakottaa kaasun liukenemaan vesikulhoon. Hän oli juuri "keksinyt" kuohuviiniä . Prosessi sitten siirtyi Johann Jacob Schweppe joka perusti vuonna 1790 , vuonna Lontoossa sooda tuotantolaitoksen tunnetaan Schweppes .
Vuonna 1781 , ranskalainen kemisti Antoine Lavoisier esiin sen, että tämä kaasu on tuotteen hiilen palaminen kanssa hapen .
Hiilidioksidia ensin nesteytetään 1823 mennessä Humphry Davy ja Michael Faradayn . Ensimmäisen kuvauksen kiinteästä faasista peräisin olevasta hiilidioksidista kirjoitti Charles Thilorier (fr) , joka vuonna 1834 avasi paineistetun nesteytetyn hiilidioksidikaasun säiliön ja havaitsi, että "lumessa syntyvän nesteen nopean haihdutuksen aikaansaama jäähdytys" "CO 2.
Käyttää
Hiilidioksidia markkinoidaan eri muodoissa eri käyttötarkoituksiin markkinoilla, joita hallitsevat suuret yritykset, kuten Messer , Air Liquide ja Air Products . Elintarviketeollisuuden osalta vertailustandardin Euroopassa julkaisee Euroopan teollisuuskaasuyhdistys (de ). Ranskassa se edustaa 70% kulutuksesta.
Kansainvälinen energiajärjestö julkaisi raportin käyttötavoista CO 2 syyskuussa 2019, jonka hän arvioi olevan 230 miljoonaa tonnia vuodessa , mukaan lukien 130 miljoonaa tonnia vuodessa lannoitteiden valmistukseen ja 80 miljoonaa tonnia vuodessa öljyn ja maakaasun tehokkaampaan talteenottoon. Tavoitteena Tämän raportin on arvioida niiden mahdollisuudet edistää kuittaaminen CO 2 päästöjä.. Hän päättelee, että tämä potentiaali on lyhyellä aikavälillä pieni ja pysyy pitkällä aikavälillä paljon pienempänä kuin hiilidioksidin talteenotto ja sitominen ; lupaavimpia keinoja ovat käyttö rakennusmateriaaleissa, polymeerien valmistuksessa ja kasvihuoneissa.
Kaasumaisessa muodossa
CO 2 on monia käyttötarkoituksia, mm.
- sammuttamiseen tulipalot : monet datakeskukset (tietokone palvelinhuoneissa) tai arkiston huoneissa on järjestelmä, joka siinä tulipalon sattuessa, täyttää tilan CO 2 joka sammuttaa palon;
- hiilihapotettujen juomien kuohuviini ;
- vuonna akvaarioissa ja kasvihuoneviljelyn paremmin kasvien kasvua;
- kontrolloidun ilmakehän pakkauksissa neutraloivana elementtinä;
- karbonaattiin liittyvässä juomaveden jakautumisessa liian aggressiivisen veden veden kovuuden (TH) nostaminen ;
- kalkkikiven liukeneminen kovassa vedessä (TH yli 25 ° F );
- olutpumput: olemalla kosketuksissa oluen pintaan, se estää sen hapettumisen ja pidentää säilyvyyttä toisin kuin (ympäröivää) ilmaa käyttävä kompressori;
- CO 2 käytetään myös joskussuurissa sikojen teurastamoissa, jotta ne tunnettaisiin ennen verenlaskua; sitä käytettiin lihan säilyttämiseen ;
- komponentti, joka on välttämätön fotosynteesin ilmiölle, joka antaa kasvien kasvua muuttamalla epäorgaanista ainetta orgaaniseksi aineeksi muodostaen siten puun;
- lämmönsiirtoneste tietyntyyppisissä ydinreaktoreissa, kuten Ranskan UNGG- sektorissa ;
- sitä käytetään sen diffuusion (diffuusio -kyvyn) avulla pneumoperitoneumin luomiseen laparoskopioiden aikana .
Nestemäisessä muodossa
Nestemäisessä muodossa sitä käytetään:
- kylmäaine tiettyjen elintarvikkeiden pakastamiseen ;
- kylmäaine elektroniikkateollisuudessa;
- sammutusaineena ns "hiilidioksidi" putki , joskus puhutaankin hiilihappolunta koska osa CO 2 neste kiinteytyy välittömästi sammuttimesta poistuttaessa, jolloin saadaan valkoinen jauhe sekoitettuna hiilidioksidikaasuun;
- ponneaine (ja joskus myös hiilihapotus) juomille, jotka tarjoillaan hanasta.
Kun sitä käytetään kylmäaineena , CO 2kantaa teollisen nimikkeistön nimeä "R744". Sen käyttö kylmäaineena on yleensä muuttunut demokraattisemmaksi viime vuosina: sitä pidetään "luonnollisena kylmäaineena", ja sen ilmaston lämpenemispotentiaali on hyvin pieni verrattuna "perinteisiin" kylmäaineisiin.
Ilmanpaineessa hiilidioksidi ei ole koskaan nestemäisessä muodossa. Se menee suoraan kiinteästä muodosta kaasumaiseen muotoon ( sublimaatio ).
Kiinteässä muodossa
Kiinteässä muodossa olevalla hiilidioksidilla on monia nimiä: "kuiva jää", "kuiva jää", "kuiva jää", "kuiva jää". Se tulee CO 2: n jähmettymisestänestemäinen. Saadaan kuivajää, joka sitten puristetaan kuivajään saamiseksi.
Kiinteässä faasissaan tämä kuivajää sublimoi jäännöksiä, sublimoitumisentalpian ollessa 573 kJ kg -1 (tai 25,2 kJ mol -1 ) lämpötilassa -78,5 ° C ja 1 atm . Siksi sitä löydettiin nopeasti useita käyttötarkoituksia kylmäaineena.
Sitä markkinoidaan eri esityksissä käytön mukaan:
- rakeina ( halkaisijaltaan 3 mm riisinjyvän kokoinen ): pääasiassa puhdistukseen ja kryogeeniseen kuorintaan ;
- sauvoissa (noin 16 mm pitkiä ):
- tuotteiden säilyttämiseksi ja kuljettamiseksi valvotussa lämpötilassa (lääkkeet, pakastettujen elintarvikkeiden kuljetus, näytteiden kuljetus jne.),
- tapahtumissa: veden kuiva jää muodostaa erittäin tiheän sumun, joka liukuu säiliön seinämiä pitkin;
- perustutkimukseen tai soveltavaan tutkimukseen, esimerkiksi:
- kemiassa kylmäaineena sekoitettuna orgaaniseen liuottimeen (useimmiten asetoniin ) lämmön johtamiseksi paremmin, harvemmin reagenssina. Tässä kentässä käytämme termiä "Carboglace" Ranskassa tai vain "carbo" puhetulla kielellä, emmekä koskaan termiä "kuivajää", jota toisaalta suositaan Quebecissä;
- sillä viiniyttämällä : se hidastaa käyminen ja estää hapetus ;
- läpipainopakkauksissa tai lohkoissa:
- ilmansyöttöön ( catering ), pitopalveluihin, hautausjohtajiin jne. ;
- leivissä:
- paksu sumu (erikoistehosteet, elokuva, video).
Kiinteää hiilidioksidia esiintyy myös hiilidioksidilumen muodossa Marsin planeetan napoilla , joissa se peittää jäätiköt (lähinnä vedestä koostuvan) ja niiden reuna -alueet paikallisen talven aikana sekä hiilidioksidin muodossa jää. alemmalla leveysasteella, myöhään illalla paikallisten lähteiden varhaisessa vaiheessa ( viikinkimaalareiden , Sojourner roverin , Phoenixin laskeutumiskuvan ja lukuisten HRSC -kuvien ottamat valokuvat ). Tärkeät talletukset on geologisesti eristetty etelänavalle.
Ylikriittisessä vaiheessa
Kriittisen pisteensä jälkeen hiilidioksidi siirtyy ylikriittiseen vaiheeseen . Nesteen ja kaasun tasapainokäyrä keskeytyy kriittisessä pisteessä, mikä takaa ylikriittiselle vaiheelle fysikaalis-kemiallisten ominaisuuksien jatkuvuuden ilman vaihemuutosta. Se on vaihe, joka on yhtä tiheä kuin neste, mutta joka varmistaa kuljetusominaisuudet (viskositeetti, diffuusio) lähellä kaasun ominaisuuksia. Ylikriittistä hiilidioksidia käytetään vihreänä liuottimena, ja uutteet eivät sisällä liuotinjälkiä.
Tässä muodossa se toimii:
- aineen uuttaminen :
- Kofeiinin ja kahvia ,
- poistaminen 2,4,6-trikloroanisoli (TCA) kohteesta korkkien käsiteltiin kloori (tai hypokloriittia), jotta antaa korkin maun viini jälkeen pullotus,
- kemiallisten tai biologisten yhdisteiden uuttaminen,
- kemiallisten yhdisteiden puhdistus (liikkuva faasi kromatografiassa , erityisesti SFC: ssä );
- kuljetus- ja varastointiaine hiilidioksidin geologisessa sitomisessa (harvinaisissa teollisissa sovelluksissa);
- jäähdytysaine aktiivisten ainesosien mikronoitumisen mahdollistamiseksi .
Teollisten prosessien sivutuote
Se on sivutuote suurten teollisissa prosesseissa. Yksi esimerkki on akryylihapon tuotanto , jota tuotetaan yli viisi miljoonaa tonnia vuodessa. Haasteena näiden prosessien kehittämisessä on löytää sopiva katalyytti ja prosessiolosuhteet, jotka maksimoivat tuotteen muodostumisen ja minimoivat CO 2 -tuotannon..
Reaktiivisuus
Hiilidioksidi on erittäin stabiili molekyyli, jonka normaalin entalpian muodostumisaste on −393,52 kJ mol −1 . Hiilellä on positiivinen osavaraus, mikä tekee molekyylistä heikosti elektrofiilisen . Esimerkiksi karbanioni voi suorittaa nukleofiilinen additio CO 2ja muodostetaan karboksyylihappo hydrolyysin jälkeen. Lisäksi CO 2voidaan käyttää muodostamaan orgaanisia karbonaatteja , jonka lisäksi epoksit .
Lopuksi CO 2voidaan vähentää, esimerkiksi hiilimonoksidin , jonka sähkökemian kanssa redox-potentiaali on -0,53 V verrattuna standardin vetyelektrodin tai hydraamalla .
Myrkyllisyys
Ulkoilma sisältää noin 0,04% CO 2 vuonna 2019 (412 ppm tammikuussa 2019).
Tietystä ilmassa olevasta pitoisuudesta tämä kaasu on vaarallinen tai jopa hengenvaarallinen tukehtumis- tai asidoosiriskin takia , vaikka CO 2ei ole kemiallisesti myrkyllistä. Altistumisen raja-arvo on 3% viidentoista minuutin aikana. Tätä arvoa ei saa koskaan ylittää. Pidemmälle, terveysvaikutukset ovat sitäkin vakavampia kuin CO 2 pitoisuuslisääntynyt. Näin ollen 2% CO 2: ssailmassa hengityksen amplitudi kasvaa. Hengitysnopeus kiihtyy 4%: lla (tai 100 kertaa ilmakehän nykyinen pitoisuus). 10%: lla näköhäiriöitä, vapinaa ja hikoilua voi esiintyä. 15%: lla se on äkillinen tajunnan menetys . 25%: lla hengityspysähdys johtaa kuolemaan.
Väkevän hiilidioksidin hengittäminen aiheuttaa ilmanvaihdon tukkeutumisen, jota joskus kuvataan väkivaltaiseksi kuristumisen tunteeksi, hengenahdistukseksi, hengitysvaikeudeksi tai puristavaksi rintakehäksi , mikä voi nopeasti johtaa kuolemaan, jos altistuminen pitkittyy.
Mukaan ANSES, tutkimusten mukaan ”pitoisuuksia liittyy luontaisia terveysvaikutuksia CO 2(kynnys noin 10000 ppm, joka vastaa hengitysteiden asidoosin (veren pH -arvon lasku) esiintymistä , joka on ensimmäinen kriittinen CO 2 -vaikutus) ” . Hengitysteiden asidoosia voi esiintyä jopa 1% (10000 ppm ) CO 2: stailmassa, jos terveellinen aikuinen, jolla on kohtalainen fyysinen kuormitus, hengittää vähintään 30 minuuttia ja mahdollisesti aikaisemmin haavoittuvissa tai herkissä henkilöissä. Nämä hinnat "ovat korkeammat kuin sääntely- ja / tai normatiiviset raja -arvot ilman uusimislaadulle Ranskassa ja kansainvälisesti, jotka yleensä vaihtelevat 1 000–1 500 ppm CO 2: n välillä. ". Pienessä kokeellisessa tutkimuksessa (johon osallistui 22 aikuista) pääteltiin, että CO 2: lla oli vaikutustaon psychomotricity ja henkinen toiminta (päätöksenteko, ongelmanratkaisu) 1000 ppm (tutkimus Satish et ai. , 2012), mutta tämä tutkimus on todistettu tutkimuksissa, joilla on suurempi tilastollinen teho. ANSES toteaa, että tästä yleisestä kaasusta on viime kädessä vähän epidemiologisia tutkimuksia, mukaan lukien mahdolliset CMR -vaikutukset (syöpää aiheuttavat, perimää vaurioittavat ja lisääntymiselle vaaralliset).
Hiilidioksidi on väritön ja raskas kaasu, joka kertyy levyihin, ja kokematon henkilö on vaikea havaita sitä.
Sisäilmassa
Ihmiset viettävät yhä enemmän aikaa suljetussa ilmapiirissä (noin 80-90% ajasta rakennuksessa tai ajoneuvossa). Mukaan ANSES ja eri toimijoiden Ranskassa, CO 2 nopeusrakennusten sisäilmassa (liittyy ihmisten tai eläinten majoittumiseen ja polttolaitosten läsnäoloon ) ilmanparannuksella painotettuna "yleensä noin 350–2 500 ppm ” .
Kodeissa, kouluissa, päiväkodeissa ja toimistoissa ei ole systemaattista suhdetta hiilidioksiditasojen välilläja muut epäpuhtaudet sekä CO 2sisätiloissa ei ole tilastollisesti hyvä ennuste ulkotieliikenteeseen (tai lentoliikenteeseen) liittyvistä epäpuhtauksista. CO 2on parametri, joka muuttuu nopeimmin (jossa kosteusolosuhteissa ja hapen kun ihmisten tai eläinten kerätään suljettuun tai huonosti ilmastoidussa huoneessa. Vuonna köyhissä maissa paljon avoimia tulisijoja lähteitä ovat CO 2ja CO päästää suoraan elämän paikalle. Tai pysyä koko päivän ilmassa CO 2 -hinnalla600 ppm saavuttaminen tai ylittäminen heikentää kognitiivisia kykyjämme (ajattelu, päättely, muistaminen, päättäminen). Pienet muutokset CO 2 -tasoissa ympäristöterveysnäkymissä julkaistun tutkimuksen mukaanilmassa vaikuttavat voimakkaasti monimutkaiseen ajattelu- ja päätöksentekokykyymme. Tämän tason 600 ppm saavutetaan usein sisäilman jossa se usein ylittää 1000 ppm , useita kertoja päivässä esimerkiksi keskimääräinen pitoisuus 3110 mg / m 3 CO 2tutkituissa luokkahuoneissa; lasten kykyjen vahingoksi).
Erityistapaus on urheiluhallit, joissa fyysinen rasitus lisää hapen tarvetta ja lisää hiilidioksidia .pelaajat (ja katsojat) ovat vanhentuneet. Esimerkiksi jääkiekkopelien aikana CO 2kasvaa 92: sta 262: een minuutissa minuutissa (enimmäkseen aikuiset miehet). Jäähallin keskellä CO 2 -tasoylittää 1000 ppm kussakin ottelussa (Norjan kansanterveyslaitoksen suosittama enimmäiskynnys). In situ -mittaukset osoittavat, että pelaaja hengittää enemmän rikastettua CO 2 -ilmaaettä katsojat ja että CO 2laskeutuu lepoaikana ja nousee peliajan aikana. Pelin jälkeisenä iltana suljetussa jääkiekkohallissa CO 2 -tason palauttaminen kestää melkein kymmenen tuntiaalhainen (600-700 ppm ), mikä on edelleen normaalin yläpuolella. Lisäksi kylmissä, lauhkeissa tai kuumissa maissa monet urheiluhallit ovat ilmastoituja; energiansäästön vuoksi ulkoilmaa ei uusita jatkuvasti tai riittävästi. Aikana jääkiekkopelistä, naiset ja lapset tuottavat vähemmän CO 2kuin miehet, mutta samassa huoneessa, aste tason nostamista CO 2urheiluhallin ilmassa on verrattavissa, ja kaikissa tutkituissa tapauksissa kahden ottelun välinen tauko ei vähennä CO 2 -pitoisuuttaniin paljon, että toisen jakson alku on yhtä heikko kuin ensimmäisen jakson alku. Kun katsojien määrä kasvaa, CO 2 -tasohuoneessa kasvaa vielä enemmän. Ulkopuolelle johtavien ovien avautumisten / sulkemisten lukumäärä vaikuttaa myös ilman uusiutumiseen ja siten CO 2 -määrään.kuntosalilla. Tutkimukset ovat osoittaneet kognitiivisen suorituskyvyn ja päätöksenteon tai oppimisen heikkenemisen, kun CO 2lisääntynyt. Harvat tutkimukset ovat keskittyneet saman CO 2: n vaikutukseen yksilön tai joukkueen urheilusuorituksesta.
MajoituksissaSitä ei säännellä kotin ilmassa; mutta se on mitattava "sulkeutumisen ja ilman uusiutumisen laadun indikaattorina" tietyissä suljetuissa paikoissa sellaisten standardien perusteella, joilla ANSES: n mielestä ei ole terveydellistä perustaa.
Muissa kuin asuinrakennuksissaRanskassa osastojen terveyssäännöissä (RSD) suositellaan, ettei 1000 ppm: n (miljoonasosaa) kynnystä ylitetä "normaaleissa käyttöolosuhteissa" ja 1300 ppm : n toleranssilla paikoissa, joissa se on kielletty. Tupakointi ( "ilman nimenomaista näiden kahden arvon terveysperusta " ANSESin mukaan.
Asetus 5. tammikuuta 2012asettaa sisäilman laadun valvonnan tietyissä herkkää yleisöä vastaanottavissa laitoksissa, kuten lapset se ehdottaa laskettaessa "synnytyksen indeksi" kutsuttu "Icône indeksi" (ehdottaman tieteellisen ja teknisen keskuksen Rakennus (CSTB) perusteella taajuus ylittää CO 2 tasossa.verrattuna kaksi kynnysarvot 1000 ja 1700 ppm: in luokissa .
Työpaikalla , kysymys turvallisuudesta ja ennaltaehkäisyyn liittyvät riskin hiili hiilidioksidi myrkytys on suuri huolenaihe vähentääkseen riskiä työtapaturmien . Puuttumisen vuoksi epidemiologisista tiedoista, sitä ei kuitenkaan pidetä merkityksellisenä Ranskassa indikaattorina terveydellistä laatua sisäilman mennessä ANSES, joka ei tarjoa ohjearvo sisäilman laatua (IGAI) tähän. Saastuttavia.
Suurina pitoisuuksina, jotka ovat lähellä 50–100%, kuten niitä, joita esiintyy ihmisen tekemissä hiilidioksidiliuskoissa työpaikalla, voi olla vaikutusta hermostuneeseen hämmästykseen ja välittömään tajunnan menetykseen , jota seuraa nopea kuolema ilman ulkopuolista apua. Nämä onnettomuudet aiheuttavat suuren riskin toiselle onnettomuudelle , koska todistajat voivat ryntää uhrin avuksi ajattelematta omaa turvallisuuttaan ja joutua myös päihtymyksen uhriksi.
CO 2 maan ilmakehässä
Hiilidioksidia on normaalisti vain maapallon ilmakehässä pieninä määrinä. Se mitataan indeksillä , jota kutsutaan vuotuiseksi kasvihuonekaasuindeksiksi (AGGI) vuodesta 1979 lähtien. Sitä ympäröi sata maalla ja merellä sijaitsevaa asemaa, jotka sijaitsevat arktiselta alueelta etelänavalle.
Koska teollinen vallankumous , koska jatkuvasti palamisen erittäin suuria määriä fossiilista hiiltä , kun taas väheneminen tulipalot , metsissä ja kasvillisuuden alueilla on jatkunut, määrä CO 2ilmassa nousee säännöllisesti (tammikuussa 2021: 415,13 ppm tilavuudesta, tai myös 632,96 massa-ppm. Tämä vastaa yhteensä massa CO 2ilmakehän paino noin 3,258 × 10 15 kg (noin kolme tuhatta gigatonnia ) . Tämä sisältö oli 283,4 ppmv 1839 alkaen jäätikkökairauksiin otettu alueelta Poinsett korkki on Etelämantereen , kokonaiskasvu oli noin 42% vuonna 177 vuotta. CO 2 -asteilmakehän odotettavissa lopussa XXI th -luvun on arviolta 540 ja 970 ppmv valittujen simulaatioiden (ISAM malli ja Bern-CC malli). Vuosi 1990 (joka vastaa noin 2,1 W / m 2 ylijäämää verrattuna vuoteen 1980 ) on Kioton pöytäkirjan viitevuosi (sen AGGI -indeksi on siis 1). On perustettu erityinen hiiliryhmää ja kasvihuonekaasuja käsittelevä tutkimusryhmä .
Aikana t CO 2 -pitoisuuseroaa jokaisella pallonpuoliskolla, ja jokaisella pallonpuoliskolla on säännöllisiä kausivaihteluita (vrt. "sahahammas" -kuvio oikealla olevassa kaaviossa, mikä osoittaa CO 2- pudotuksenin kausi on kasvillisuuden ja kasvua talvella). On myös alueellisia vaihteluita, erityisesti ilmakehän rajakerroksen tasolla eli maan lähellä olevissa kerroksissa.
CO 2-tasot ovat yleensä korkeammat kaupunkialueilla ja asunnoissa (jopa kymmenen kertaa taustatasoa suuremmat).
Pian maapallon muodostumisen jälkeen (kauan ennen elämän ilmestymistä), kun aurinko oli lähes puolet ”kuumasta”, CO 2: n alkupaineoli noin 100 000 kertaa korkeampi kuin nykyään (30–60 ilmakehää CO 2( eli 3 000 000 - 6 000 000 pascalia), eli 100 000 kertaa nykyinen CO 2 -määrä noin 4,5 miljardia vuotta sitten).
Sitten elämä ja fotosynteesi ilmestyivät ottamalla CO 2: nilmakehästä ja vedestä muuttaakseen sen karbonaattikiveiksi ja kivihiileksi, öljyksi ja maakaasuksi, josta suuri osa hautautui syvälle maan syvyyteen. CO 2 -asteon silti kokenut joitain huippuja, joilla on paljon vähemmän merkitystä (kaksikymmentä kertaa korkeampi kuin tänään noin puoli miljardia vuotta sitten, mutta aurinko oli silloin vähemmän kuumaa kuin tänään (aurinkosäteily kasvaa ajan myötä ja on kasvanut noin 40% viimeisen neljän viimeisen aikana) miljardia vuotta) määrä CO. 2laski vielä neljä-viisi kertaa Jurassicin aikana , sitten laski hitaasti, paitsi nopeutetusti geologisesti lyhyen jakson aikana, joka tunnetaan nimellä " Azolla-tapahtuma " (noin 49 miljoonaa vuotta sitten).
Tulivuoritoiminnan lähettää myös CO 2(jopa 40% tiettyjen tulivuorien päästöistä subaeriaalisten purkausten aikana on hiilidioksidia) ja tietyt kuumia lähteitä myös (esimerkiksi Italian Bossoleton alueella Rapolano Termen lähellä, jossa altaan muotoisessa syvennyksessä noin 100 m halkaisijaltaan, rauhallisena yönä, CO 2voi nousta 75% muutamassa tunnissa, riittää tappamaan hyönteisiä ja pieniä eläimiä. Mutta kaasumassa lämpenee nopeasti, kun alue on aurinkoinen, ja hajaantuu sitten ilman konvektiovirroilla päivän aikana. Paikallisesti korkeita CO 2Tuottama veden häiriöt tämän syvän järven kyllästetty CO 2voi myös tappaa (esimerkki: 37 kuolemaa CO 2 -purkauksen aikanaalkaen järven Monoun vuonna Kamerunissa vuonna 1984 ja 1700 uhreja ympäri Nyosjärvi (myös Kamerun) vuonna 1986.
CO 2 -päästötIhmisen toiminnan aiheuttamat päästöt ovat tällä hetkellä yli 130 kertaa suuremmat kuin tulivuorien päästöt, mikä on lähes 27 miljardia tonnia vuodessa vuonna 2007. Vuonna 2012 Kiina oli maailman johtava hiilidioksidipäästö 27%: lla kokonaismäärästä, ja Yhdistynyt kuningaskunta Toiseksi osavaltiot tuottavat 14% maailman kokonaismäärästä. Vuonna 2016 YK: n ilmatieteen laitos raportoi, että hiilidioksidipitoisuus saavutti uuden kaikkien aikojen korkeimman tason, 403,3 ppm , ja vuoden 2017 El Niñon lämpötilaennätys rikottiin OMM: n mukaan, kun taas 405 ppm , CO 2 ilma ei ole koskaan ollut näin korkea noin 800 000 vuoteen.
Global CO 2 päästötkasvoi 2,7% vuonna 2018, mikä on seitsemän vuoden suurin kasvu. Vuonna 2019 raportin, CO 2 pitoisuudetsaavutti 407,8 ppm vuonna 2018, mikä havainto korreloi myös metaanipitoisuuksien nousun kanssa (CH 4) Ja typpioksiduulin (N 2 O-).
Kasvien ravintoaine
Korkeampi CO 2 -tasostimuloi fotosynteesiä ja kasvien kasvua, ja sillä on potentiaalisia etuja viljakasvien tuottavuudelle, joka on maailman ensisijainen elintarvikkeiden lähde ihmisille ja tuotantoeläimille. Hiili, joka on otettu hiilidioksidi ilmassa autotrofisia kasvien kautta fotosynteesissä, tai otetaan maaperästä hiili, on todellakin yksi tärkeimmistä ravinteiden ruoka rainan . Biomassan kasvu on yksi simuloitujen kokeiden vaikutus, jossa ennustetaan sadon 5-20% kasvua 550 ppm CO 2: lla. Lehtien fotosynteesin on osoitettu kasvavan 30-50% C3-kasveissa ja 10-25% C4-kasveissa alle CO 2 -tason kaksinkertaistui.
Vuodesta 2010 lähtien muodostuu täydellisempi kuva, jossa eri kasvilajeissa, veden saatavuudessa ja otsonipitoisuuksissa havaittu vaste on merkittävä . Esimerkiksi Horshamin vapaiden ilmojen väkevöinti ( FACE) 2007-2010 -hankkeessa (jossa käytettiin vehnänkasveja) Victoriassa, Australiassa, havaittiin, että "hiilidioksidin vaikutuksen oli lisättävä sadon biomassaa. Kypsyydessä 20% ja juuren biomassaa. anteesi 49% ". On havaittu, että ilmakehän hiilidioksidin lisääntyminen vähentää kasvien vedenkulutusta ja siten typen imeytymistä , mikä hyödyttää erityisesti sadon satoa kuivilla alueilla.
Vaikutukset kasvien ravintoarvoon
Kuitenkin, jos CO 2 -pitoisuuden nousuIlmakehä lisää tehokkaasti ( esimerkiksi viljakasvien ) kasvua , syistä, jotka ovat edelleen huonosti ymmärrettyjä, se vähentää sitten tärkeimpien peruskasvien (erityisesti riisin , vehnän ja perunoiden ) ravintoarvoa vähentämällä niiden proteiinipitoisuutta , hivenaineita ja B -vitamiinit . Koeolosuhteissa CO 2 -tasolisääntynyt (jopa ilman lämpötilan nousua) johtaa korkeampaan sokeripitoisuuteen viljellyissä kasveissa ( yhä voimakkaampien alkoholien lähde viinirypäleille), mutta myös proteiini- ja kivennäisainepuutoksista. Riisillä on myös usein korkeita arseenipitoisuuksia , mikä väliaineen happamoituminen voi pahentaa. Lopuksi, suuremmat pitoisuudet CO 2pahentaa happamoituminen makean veden ja valtamerten happamoitumisen seurauksena , jotka voivat vaikuttaa tuottavuuteen levien (ja siksi levät kulttuuri ).
Tästä syystä, mukaan tuoreessa tutkimuksessa (2018), 2015-2050, on epätavallisen korkea CO 2ilmakehän ilmakehä voi maailmassa ennen vuotta 2050 johtaa ihmisten ja tiettyjen tuotantoeläinten (siat, lehmät, siipikarja) ravitsemuksellisten puutteiden aiheuttamiin sairauksiin. PLOS Medicine -lehden ilmastonmuutosta ja terveyttä käsittelevässä erikoisnumerossa julkaistussa tutkimuksessa Christopher Weyant ja hänen kollegansa Stanfordin yliopistossa keskittyivät kahteen olennaiseen hivenaineeseen , sinkkiin ja rautaan. Ilmastonmuutos ja ruokailutottumukset huomioon ottaen ne osoittavat, että tautiriski muuttuu 137 maassa. Jos mitään ei tehdä, kasvu CO 2 nopeusvähentää sinkki- ja rautapitoisuuksia elintarvikkeissa, ja se maksaa maailmanlaajuisesti arviolta 125,8 miljoonaa vammaisuuteen mukautettua elinaikaa (95%: n luottamusväli [CrI] 113,6–138,9) vuosina 2015–2050 tartuntatautien , ripulin ja tapausten lisääntymisen vuoksi ja anemiaa , erityisesti Kaakkois-Aasiassa ja Afrikassa , missä väestö jo kärsineet sinkin ja raudan puutteita. Lapset kärsivät erityisesti näistä puutteista johtuvien peruuttamattomien kehityshäiriöiden riskistä, joka voi levitä useiden sukupolvien ajan ainakin epigeneettisistä syistä .
Weyantin tutkimus osoittaisi myös, että ravitsemuksellinen eriarvoisuus voisi lisääntyä, ja se osoittaisi, että perinteiset kansanterveysreaktiot (mukaan lukien mineraalien ja vitamiinien lisäykset sekä ihmisten ja eläinten sairauksien tehokkaampi hallinta) eivät välttämättä riitä taudin torjumiseksi. Tällaiset vastaukset vähentäisivät vain 26,6% (95% CI: stä 23,8–29,6) tästä terveys-, ihmis- ja taloudellisesta taakasta, kun taas Pariisin ilmastosopimuksessa ehdotettu tehokas kasvihuonekaasupäästöjen vähentämisstrategia estäisi jopa 48,2% (95% CIF-indeksistä 47,8–48,5) tästä kuormituksesta.
Vaikka CO 2ravitsee kasvien kasvua, sen ylimäärä aiheuttaa niiden ruoka-arvon heikkenemisen, jolla on maailmanlaajuiset seuraukset kaikille kasveja kuluttaville eläville olennoille, myös ihmisille. Kirjoittajat kannustavat paremmin tutkimaan lisääntyneen CO 2: n vaikutuksiailmakehässä muilla kasviperäisillä yhdisteillä, joilla on vaikutuksia ihmisten terveyteen (esim. rasvahapot, vitamiinit, farmakologiset yhdisteet, varsinkin kun tässä tutkimuksessa ei otettu huomioon muita CO 2: n lisääntymisen seurauksia, elintarviketurvaan, elintarvikkeiden saatavuuteen, sen käyttöön ja hintavakauteen liittyvistä meteorologisista ja biologisista vaaroista (lisääntynyt köyhtyminen jne.) eikä avaruudessa ja ajassa viivästyneiden seurausten ketjuista (erityisesti aliravitsemuksen pitkän aikavälin vaikutukset).
Maataloustuotot ovat pysähtyneet tai heikkenevät yhdessä osassa maailmaa, mikä johtuu erityisesti lämpenemisestä (lämpöaallot jne.) Ja muuttuneista sateista. Elintärkeisiin viljelykasveihin (erityisesti vehnään ja riisiin) vaikuttaa jo trooppisilla ja lauhkeilla alueilla, ja tulevien tutkimusten mukaan riisi- ja maissikasvit voivat vähentyä 20–40% pelkästään vyöhykkeen odotetun lämpötilan nousun vuoksi. Trooppinen ja subtrooppinen vuoteen 2100 mennessä, jopa äärimmäisten sääilmiöiden vaikutukset huomioon ottaen. Tässä yhteydessä voi johtaa elintarvikkeiden hintojen nousuun, mikä tekee niistä liian kalliita köyhimpiä, kun taas tasojen nousu CO 2 ilmassavoisi myös heikentää erityisesti ihmisten ja mahdollisesti eläinten terveydelle tärkeiden viljojen ravitsemuksellista laatua (myös maidon ja lihan (ja siten proteiinien) lähteet , kun taas merellä myös kalojen biomassa vähenee.
"Vielä ei ole selvää, onko CO 2: n aiheuttama ruokakasvien ravintoarvon laskuon lineaarinen ja jos ravitsemuksellinen laatu on jo heikentynyt hiilidioksidin lisääntymisen vuoksi teollisen vallankumouksen jälkeen. "
Lisäksi ilmastonmuutokseen sopeutumisen edellyttämiä toimenpiteitä, joilla pyritään vähentämään CO 2 päästöjäja biologinen talteenotto CO 2tarvitaan kiireellisesti. Jotkut lajikkeet, jotka ovat vähemmän alttiita ravitsemuksellisille alijäämille lämpenevässä ilmastossa, etsivät Weyantin ja hänen kollegoidensa työtä.
Kasvun vaikutukset CO 2kasveja aiheuttavat enemmän huolta kuin mitä 1990-luvun ja 2000-luvun alun ensimmäiset mallit ennustivat. Morgan et ai. , laboratorio- ja in situ -kokeiden perusteella , vahvisti jo vuonna 2004, että kehittyvissä ekosysteemeissä CO 2Jopa silloin, kun se parantaa tuottavuutta kannalta biomassan, voi kuitenkin olla kielteisiä vaikutuksia muokkaamalla koostumus lajien ja vähentämällä sulavuus on lyhyt heinäkasvien esimerkiksi aro kasvillisuuden ).
Kasvihuonekaasu ja happamoittaja
CO 2on toiseksi tärkein kasvihuonekaasu ilmakehässä vesihöyryn jälkeen , ja sen osuus ilmiöstä on 26% ja 60%. Viime vuosisadan jälkeen planeetan mittakaavassa havaittua ilmaston lämpenemisen todellisuutta ei enää kiistetä tieteelliseltä kannalta, mutta hiilidioksidin vastuun tarkka osuus tässä prosessissa ( erityisesti metaaniin verrattuna ) on vielä selvitettävä, erityisesti paleoklimaattien fossiilisten tallenteiden ansiosta.
Lisäksi happamoitumisen johtuvat liukeneminen ilmakehän hiilidioksidia voi vaaranna monien merieliöiden ennen XXI th -luvulla, varsinkin ne, tukiranka calcified kuten koralleja ja äyriäisiä , mutta myös kalaa.
Väheneminen ihmisen toiminnan aiheuttamien päästöjen on saavuttamista Kioton pöytäkirjan sekä mukaan direktiivin 2003/87 / EY ; sen pitkäaikainen geologinen sitomisen on tutkimuskohde, mutta on kiistanalainen ratkaisu, kun se tulee yksinkertaisesti pistämällä CO 2 geologisissa kerroksissa.
Ekosysteemin lisääntyneen CO 2 tasossa vedessä ja ilmassa
VedessäCO 2on tietty rehevöityneiksi vaikutus (se on perus ravintoaine , joka on välttämätön kasvien), mutta se on myös tekijä happamoitumista valtamerten ja tiettyjen elinten makean veden , joka voi negatiivisesti vaikuttaa monia lajeja (mukaan lukien tietyt mikrolevistä ja muut vedessä kalkkirakenteilla suojattuja mikro -organismeja, joita hiilihappo voi liuottaa). Happamoituminen edistää myös useimpien raskasmetallien , metalloidien tai radionuklidien (luonnollisesti sedimenteissä tai antropogeenistä alkuperää erityisesti teollisen vallankumouksen jälkeen) vapautumista ja verenkiertoa .
IlmassaKasvu CO 2 ilmakehästäniillä voi myös olla erilaistuneita tai jopa antagonistisia vaikutuksia sen nopeudesta, ympäristö- ja luonnonmaantieteellisestä tilanteesta riippuen ja tuoreempien tietojen mukaan vuodenajasta ja vuodenaikojen vaihteluista sateissa (erityisesti metsien yläpuolella)
Ilmastonmuutoksen vaikutusten tutkimiseen liittyy ekologien keskuudessa yksimielisyys siitä, että yli 2 ° C : n nousun vuosisadan aikana maa- ja meriekosysteemeihin kohdistuu vakavia kielteisiä vaikutuksia.
Vuonna 2013 , todellinen vaste ekosysteemin CO 2ja sen biogeografisia modulaatioita pidetään edelleen monimutkaisina ja ymmärrettävinä lukuisien " biogeokemiallisten palautteiden " vuoksi . Se on kuitenkin selvitettävä, jos haluamme arvioida tai jopa ennustaa ekosysteemien planeetta- tai paikalliskapasiteettia luonnollisen hiilivarastoinnin ja ihmisten aiheuttamien ilmastonmuutoksen vaikutusten vaimentamisen kannalta .
Palaute välittämä veden kiertokulun ovat erityisen tärkeitä, ja sademäärä on merkittävä rooli. Fysiologia kasvien on ainakin eräs tunnettu rooli; tiettyyn vaiheeseen (jonka jälkeen kasvi kuolee), kasvu tason CO 2Ilman käyttö vähentää stomaattista johtavuutta ja lisää kasvien vedenkäytön tehokkuutta ( kuiva- aineyksikön tuottamiseen tarvittavan veden määrä ), veden käytön väheneminen johtaa maaperän kosteuden parempaan saatavuuteen. Se arvioitiin vuonna 2008, että kasvun vaikutukset CO 2ekosysteemin ilmassa pitäisi pahentua, kun vesi on rajoittava tekijä (mutta myös typen saanti on otettava huomioon); tämä on osoitettu joissakin kokeissa, mutta se on tekijä, joka on "unohdettu" monissa tutkimuksissa.
Tämä suhde vaikuttaa niin vahva, että se tekee mahdolliseksi - in lauhkean vyöhykkeen - ennustaa tarkasti vuosittain vaihtelut stimulaatio antenni biomassan nousun jälkeen CO 2 tasolla.on sekoitettu nurmi sisältää kasveja tyypin C3 ja C4 , joka perustuu koko kausiluonteinen saostuminen ; sateinen kesä on myönteinen vaikutus, kun taas syksyllä ja keväällä on kielteisiä vaikutuksia vasteena CO 2. CO 2 -tasojen nousun vaikutus riippuu siten pääasiassa uusista tasapainoista tai epätasapainoista, jotka syntyvät kesän ja syksyn / kevään sateiden välillä.
Yhteys typpiin (toinen tekijä, jota ihmisen toiminta, mukaan lukien teollisuusmaatalouden, teollisuuden ja autoliikenteen päästöt, häiritsevät ) löytyy täältä: voimakkaat sateet kylminä ja märkinä vuodenaikoina rajoittavat ajoneuvojen pääsyä maahan. stimulaatio biomassan taso CO 2kasvatettu. Todettiin myös, että tämän ennusteen järjestetään myös koealojen "lämmitettiin" mukaan 2 ° C: ssa tai lämmittämätön, ja se oli samanlainen kasvien C3 ja biomassan, joka näyttää jotta ennustajat tehdä vankka ennusteita. Vastauksista korkeat CO 2 pitoisuuksinan ekosysteemin . Tämä on arvokas voimavara, koska korkean resoluution mallien ilmastoennusteet vahvistavat erittäin suuren todennäköisyyden suurista muutoksista vuotuisessa sademääräjakaumassa, vaikka maaperään sattuva vuotuinen kokonaismäärä ei muuttuisi. Näiden tieteellisesti vahvistettujen tietojen (vuonna 2013) pitäisi auttaa selittämään joitain eroja, jotka ilmenivät kokeiden tuloksissa, jotka perustuivat kasvien altistumiseen lisääntyneelle CO 2 -tasolle.Ja parantaa mahdollinen tehokkuutta malleja, jotka eivät ota riittävästi huomioon ajankohdan sateen annetun biologisen monimuotoisuuden vastauksia CO 2 14, erityisesti metsäympäristöissä.
CO 2 -vähennys ilmassa
Useita tapoja tutkitaan tai toteutettu kumuloituminen CO 2ilmassa. Ne voivat liittyä luonnollisiin prosesseihin, kuten fotosynteesiin tai teollisiin prosesseihin. On myös tehtävä ero sieppauksen lähteellä ja sieppauksen välillä ilmakehässä.
Käynnistys Intian Carbon Clean Solutions (CCSL) on julkistanut ensimmäisen laitokseen, joka kaappaa ja uudelleenkäyttö 100% CO 2(60000 tonnia vuodessa) pienestä hiilivoimalasta Intiassa Chennaissa (Madras); tämä CO 2puhdistetaan, sitten myydään paikalliselle teollisuusyrittäjälle, joka käyttää sitä soodan valmistamiseen. CCSL -tekniikka vähentää CO 2 -kustannuksiamyydään 30 dollarilla tonnilta Intiassa ja 40 dollarilla Euroopassa tai Yhdysvalloissa, mikä on selvästi alle markkinahinnan: 70–150 dollaria tonnilta. Veolia on allekirjoittanut sopimuksen CCSL: n kanssa tämän prosessin markkinoimiseksi kansainvälisesti. Samaan aikaan Climeworks yhtiö pyrkii kaapata CO 2 suodattamalla ympäröivä ilma.
Kanadalainen yhtiö Carbon Engineering perustaman insinööri David Keith ja rahoittavat Bill Gates ja useita öljy- ja kaivosyhtiöiden on kehittänyt reaktorin otteita CO 2ilmakehää edullisemmin kuin nykyiset sieppaustekniikat. Sijoittajien tarjoamia varoja käytetään tämän suoran talteenottoprosessin yhdistämiseen "Ilma polttoaineisiin" -prosessiin, jonka avulla ilmakehässä talteenotettu hiili voidaan muuntaa bensiinin kaltaiseksi polttoaineeksi. Se aikoo rakentaa suuren tehtaan Houstoniin yhteistyössä Occidental Petroleumin kanssa . Kuitenkin CO 2 -anturireaktoritovat erittäin energiaintensiivisiä, ja siksi niiden on saatava uusiutuvia energialähteitä; tiedeneuvoston akatemioiden Euroopan Sciences (EASAC) suhtautuu varauksella: sen mukaan poistamaan CO 2 ilmassa ei estä ilmastonmuutosta eikä ole toistaiseksi IPCC: n suositusten mukainen.
Kohti "aurinkometaanin" tuotantoa CO 2: sta ? .
Teoriassa CO 2: n muuntaminenpolttoaineen tai kemiallisten raaka-aineiden vähentäisi fossiilisten polttoaineiden käyttöä ja vähentää CO 2 -päästöjä.
Sähkökemiallista muuntamista uusiutuvista sähkönlähteistä on tutkittu paljon 2010 -luvulta lähtien.
Yksi fotokemiaan perustuva toivo on, että voimme käyttää vain auringonvaloa ja pilaantumattomia katalyyttejä, jotka ovat halpoja ja runsaita maapallolla. Niistä photocatalysts ja molekyylitason sähkökatalyytit mainittu tieteellisessä kirjallisuudessa 2010-luvun, vain harvat ovat stabiileja ja selektiivisiä vähentää CO 2 ; Lisäksi ne tuottavat pääasiassa CO: ta tai HCOO: ta, ja katalyytit, jotka pystyvät tuottamaan jopa pieniä tai kohtalaisia saantoja huomattavasti vähentyneistä hiilivedyistä, ovat edelleen harvinaisia.
Neljä tutkijaa, mukaan lukien kaksi ranskalaista (Julien Bonin & Marc Robert), tuottivat katalyytin, joka on rauta -tetrafenyyliporfyriinikompleksi, joka on funktionalisoitu trimetyyliammoniumryhmillä ja jonka he esittävät olevan (julkaisuajankohtana) tehokkain ja valikoivin CO 2: n muuntamiseenCO: ssa, koska se voi katalysoida kahdeksan CO 2 -elektronin pelkistymistämetaanissa yksinkertaisessa valossa, ympäristön lämpötilassa ja paineessa. Katalyyttiä on kuitenkin käytettävä asetonitriililiuoksessa , joka sisältää valoherkistimen ja uhrautuvan elektronin luovuttajan; se toimii sitten vakaasti muutaman päivän ajan. CO 2muunnetaan ensin pääasiassa CO: ksi fotoreduktion avulla ja jos on kaksi reaktoria, CO tuottaa sitten metaania, jonka selektiivisyys on enintään 82% ja kvanttisaanto , ts. valotehokkuus, 0, 18%). Kirjoittajat uskovat, että se voisi inspiroida muita molekyylikatalyyttejä.
Suunnitellaan myös "katalyysijärjestelmiä", molekyylikatalyyttejä, samoin kuin järjestelmiä, jotka perustuvat perovskiittiin tai siirtymämetallikomplekseihin .
Huomautuksia ja viitteitä
- HIILIDIOKSIDI , kansainvälisen kemikaaliturvallisuusohjelman käyttöturvallisuustiedote (t) , kuultu 9. toukokuuta 2009
- laskettu molekyylimassa välillä " Atomic painot Elements 2007 " on www.chem.qmul.ac.uk .
- " Hiilidioksidi " , vaarallisten aineiden tietopankissa (käytetty 8. maaliskuuta 2010 )
- Bernard M. ja Busnot F. (1996), Usuel of general and mineral chemistry , Dunod, Paris, s. 229 .
- (EN) Robert H. Perry ja Donald W. Green , Perryn Chemical Engineers' Handbook , Yhdysvallat, McGraw-Hill,1997, 7 th ed. , 2400 Sivumäärä ( ISBN 0-07-049841-5 ) , s. 2-50
- (in) WM Haynes, Handbook of Chemistry and Physics , CRC, 2010-2011 91 th ed. , 2610 Sivumäärä ( ISBN 978-1-4398-2077-3 ) , s. 14–40
- (in) Irvin Glassman ja Richard A. Yetter, Combustion , Amsterdam / Boston, Elsevier,2008, 4 th ed. , 773 Sivumäärä ( ISBN 978-0-12-088573-2 ) , s. 6
- (in) Carl L. leuat, Handbook of termodynaamiset kaaviot , Voi. 1-3, Huston, Texas, Persianlahden pubi,1996( ISBN 0-88415-857-8 , 978-0-88415-858-5 ja 978-0-88415-859-2 )
- (in) David R. LiDE, Handbook of Chemistry and Physics , CRC,2008, 89 th ed. , 2736 Sivumäärä ( ISBN 978-1-4200-6679-1 ) , s. 10-205
- “ Hiilidioksidi ” , osoitteessa www.reciprocalnet.org (käytetty 12. joulukuuta 2009 )
- CAS-numeron "124-38-9" merkitseminen kemikaalitietokantaan GESTIS of the IFA (saksalainen elin, joka vastaa työturvallisuudesta ja -terveydestä) ( saksa , englanti ), saatavana 6. joulukuuta 2008 (vaaditaan JavaScript)
- SIGMA-ALDRICH
- " Hiilidioksidi " kemiallisten tuotteiden tietokannassa Reptox of the CSST (Quebec-organisaatio, joka vastaa työturvallisuudesta ja työturvallisuudesta), käyty 25. huhtikuuta 2009
- (in) David R. LiDE, CRC Handbook of Chemistry and Physics , CRC Press,2009, 90 th ed. , 2804 Sivumäärä , kovakantinen ( ISBN 978-1-4200-9084-0 ) , s. 6-107
- Frédéric Datchi, " CO 2 -molekyylikestää painetta odotettua paremmin. » , Tiivistetyn median mineralogian ja fysiikan instituutista (IMPMC, Pariisi) ,huhtikuu 2010(käytetty 28. tammikuuta 2016 ) .
- T. Uchida, S. Mae, J. Kawabata ja T. Hondoh, “CO 2: n fyysiset tiedotHydraatti ” , julkaisussa N. Handa ja T. Ohsumi (ohjaaja), Direct Ocean Disposal of Carbon Dioxide , Terra Scientific Publishing Company (TERRAPUB),1995, 45-61 Sivumäärä ( lue verkossa ).
- HS Chen, Hiilidioksidihydraattien termodynamiikka ja koostumus , MS-tutkielma, Syracuse University, New York, 1972.
- H. Lee, C.-S. Lee, W.-M. Laulanut ja S.-P. Kang, Hydrata faasitasapainot vieraseoksissa, jotka sisältävät CO 2: ta, N2 ja tetrahydrofuraani , nestefaasin tasapaino. , 2001, 185, 101
- P. Englezos, R. Kumar ja J. Ripmeester, kaasu hydraatti erotusprosessista CO 2polttokaasuseoksesta: makro- ja molekyylitasotutkimukset , Proceedings of the 6th International Conference on Gas Hydrates (ICGH) , 2008
- P. Linga, R. Kumar ja P. Englezos, Klatraattihydraattiprosessi hiilidioksidin talteenoton jälkeiseen ja polttamista edeltävään talteenottoon , J. Hazard. Mater. , 2007a, 149 (3), 625–629.
- NH Duc, F.Chauvy ja J.-M. Herri, CO 2sieppaus hydraattikiteyttämällä - potentiaalinen ratkaisu terästeollisuuden kaasupäästöille , energia. Tulos Manag. , 2007, 48, 1313-1322.
- Wassila Bouchafaa, Stabiloitujen kaasun hydraattien dissosiaatio -olosuhteiden mittaus ja mallinnus käytettäväksi CO 2: n talteenotossa (väitöskirja École Polytechnique), 22. marraskuuta 2011
- YD Kim, HJ Lee, YS Kim ja JD Lee, tutkimus suolanpoiston purkamisesta CO 2hydraattitekniikka , Proceedings of the 6th International Conference on Gas Hydrates (ICGH) , 2008
- MD Max, K. Sheps, SR Tatro ja LB Osegovic, Meriveden suolanpoistolaitoksissa hyödyllinen tekijä CO 2sitomista , Proceedings of the 6th International Conference on kaasuhydraatteja (ICGH) , 2008
- luku. I-4.3. Samanaikaisesti metaanin talteenotto ja CO 2 varastoinnin, s. 61 (tai s. 67 [PDF] -versiosta ) Nadia Mayoufin opinnäytetyöstä, Characterization of hydrate coulis, joka sisältää CO 2sovellettu jäähdytysjärjestelmiin , väitöskirja, École Polytechnique, 8. joulukuuta 2010
- (in) " Hiilidioksidi: Sylvester Spiritus " Ebbe Almqvist, Teollisuuskaasujen historia , Springer,2003, 472 Sivumäärä ( ISBN 978-0-306-47277-0 , lue verkossa ), s.
- Sigaud de La Fond, essee kiinteän ilman tai kaasun eri lajeista… , Pariisi, Chez P.Fr.Geeffier,1785( lue verkossa )
- (sisään) Joseph Priestley , " Havaintoja erilaisista ilmalajeista " , Phil. Trans. , Voi. 62,1772, s. 147–264 ( ISSN 0260-7085 , DOI 10.1098 / rstl.1772.0021 , lue verkossa )
- (in) Humphry Davy , " On the soveltaminen Nesteet Muodostuu tiivistämällä kaasujen Mekaaninen Agents " , Phil. Trans. , Voi. 113,1823, s. 199–205 ( ISSN 0261-0523 , DOI 10.1098 / rstl.1823.0020 , lue verkossa [PDF] )
- (en) Charles Thilorier, " Hiilihapon jähmettyminen " , CR Hebd. Acad-istunnot. Sei. , Voi. 1,1835, s. 194-196 ( lukea verkossa )
- (in) HD Roller Duane , " Thilorier First and the solidification of a Permanent Gas (1835) " , Isis , voi. 43, n ° 21952, s. 109-113 ( ISSN 0021-1753 , DOI 10,1086 / 349402 )
- Dominique Pialot, " CO2, uudet markkinat? » , Osoitteessa latribune.fr ,17. kesäkuuta 2019(käytetty 6. elokuuta 2019 ) .
- (in) " Hiilidioksidi Elintarvikkeiden ja juomien laatu lähde pätevyys, laatuvaatimukset ja todentaminen: Eiga Doc 70/17 " päälle eiga.eu ,2016(käytetty 12. heinäkuuta 2019 ) .
- (en) CO2: n käyttöönotto - arvon luominen päästöistä , Kansainvälinen energiajärjestö , syyskuussa 2019.
- Neil A. Campbell ja Jane B. Reece , biologia , Erpi,2007, 1400 Sivumäärä
- Carboglace on tavaramerkki rekisteröity Ranskassa Air Liquide
- von Baczko, K., toim. Gmelins Handbuch der Anorganischen Chemie: Kohlenstoff , 8 th ed. , Chemie GMBH, Weinheim / Bergstr., 1970, osa C. Osa 1, s. 413–416 .
- Phillips, RJ, Davis, BJ, Tanaka, KL, Byrne, S., Mellon, MT, Putzig, NE, ... & Smith, IB (2011) Massiiviset CO2-jääkerrokset erotettiin Marsin eteläpolaarisissa kerrostumissa . Science, 332 (6031), 838-841.
- (in) " Reaktioverkko propaanin hapetusvaiheessa puhtaan MoVTeNb M1 Oxide Catalystsin yli " , Journal of Catalysis , Voi. 311,2014, s. 369-385 ( lue verkossa )
- (in) " Puhtaan oksidifaasin pintakemia M1 MoVTeNb käytön aikana propaanin selektiivisessä hapetuksessa akryylihapoksi " , Journal of Catalysis , Voi. 285,2012, s. 48-60 ( lukea verkossa )
- (in) Propaanihapetuksen kineettiset tutkimukset ovat Mo- ja V-sekoitetut katalyytit ,2011( lue verkossa )
- (in) " kiteisten MoV (NBPT) M1-oksidikatalyyttien monitoiminto propaani- ja bentsyylialkoholin selektiivisessä hapetuksessa 3 (6) " , ACS Catalysis , voi. 3, n o 6,2013, s. 1103-1113 ( lukea verkossa )
- (in) Colin Finn , Sorcha Schnittger Lesley J. Yellowlees ja Jason B. Love , " Molecular lähestymistavat hiilidioksidin sähkökemialliseen pelkistykseen " , Chemical Communications , voi. 48, n ° 10,2012, s. 1392-1399 ( PMID 22116300 , DOI 10.1039 / c1cc15393e ).
- (en) CO2.earth CO 2 -pitoisuus maan ilmakehässä.
- Myrkytys hengittämällä hiilidioksidia , lääketieteellinen asiakirja 79, INRS, 1999.
- CO 2 -pitoisuudet sisäilmassa ja vaikutukset terveyteen, ANSES-lausunto, kollektiivinen asiantuntijaraportti, ANSES, 2013/07, 294 Sivumäärä
- Sisäilman laadun seurantakeskus (Oqai), ekologian ministeriö, Ademe, CSTB, AirParif, ...
- (in) Chatzidiakou, L. Mumovic, D., & Summerfield, A. (2015). Onko CO 2hyvä sisäilman laadun edustaja luokkahuoneissa? Osa 1: Lämpöolosuhteiden, CO2 -tason, ilmanvaihdon ja valittujen sisäsaasteiden väliset suhteet. Talotekniikan tekniikan tutkimus ja tekniikka, 36 (2), 129-161 ( tiivistelmä ).
- (in) Cetin Sevik M & H (2016), Indoor laadun analyysi CO2 Kastamonu yliopisto . In Conference of the International Journal of Arts & Sciences (Vuosikerta 9, nro 3, s.71).
- (in) Jaber AR Dejan Marcella M & U (2017) Sisälämpötilan ja CO2-tasojen vaikutus on aikuisten naisten kognitiivinen suorituskyky yliopistorakennuksessa Saudi-Arabiassa , Energy Procedia , 122, 451-456.
- (in) Myhrvold AN, Olsen S & Lauridsen O Sisäympäristö kouluissa, oppilaat ja terveydentila hiilidioksidipitoisuuksien suhteen , sisäilma , 96 (4), 369-371, 1996
- (en) Prestmo LS (2018) Sisäilman parametrien mittaukset jääkiekkohallin harjoitusvyöhykkeellä (pro gradu, NTNU).
- (in) Prestmo LS (2018) Sisäilmastoparametrien mittaukset jääkiekkohallin harjoitusalueella (Pro gradu, NTNU) (ks. Kohta 7.2 Lisääntynyt CO 2 keskittyminen ottelun aikana)
- (in) Esim: Kenneth W. Rundell (2004) "Keuhkojen toiminta rappeutuminen naisilla jääkiekkoilijoita: Onko suhde jäähalli ilmanlaatua? " Hengitysteiden toksikologia , 16 (3): 117–123
- Myrkytys hengittämällä hiilidioksidia , lääketieteellinen tekninen tiedosto 79 TC 74, INRS
- D Tri Pieter ruskettuu (3 toukokuu 2008) Annual CO 2moolijakeen kasvu (ppm) vuosina 1959–2007 , National Oceanic and Atmospheric Administration , Earth System Research Laboratory , Global Monitoring Division ( lisätietoja ).
- NOAA / Law Dome
- NOAA / Mauna Loa
- Ilmastotutkimusyksikkö (Univ. East Anglia)
- Solar Influences Data Analysis Center (SIDC)
- http://advances.sciencemag.org/content/3/1/e1601207
- Trends in Atmospheric Carbon Dioxide - Global Monthly Mean CO2 , National Oceanic & Atmospheric Administration (NOAA) - Earth System Research Laboratories (ESRL), käytetty 25. huhtikuuta 2021.
- (in) hiilidioksidissa Analysis Centre, kesäkuussa 1998 , " Historiallinen CO 2ennätys, joka on johdettu Law Dome DE08- ja DE08-2-jään ytimien spline-sovituksesta (20 vuoden katkaisu) ", DM Etheridge, LP Steele, RL Langenfelds, RJ Francey (ilmakehän tutkimuksen osasto, CSIRO, Aspendale, Victoria, Australia) J.-M.Barnola ( Glaciologian ja ympäristögeofysiikan laboratorio , Saint-Martin-d'Hères , Ranska) ja VI Morgan (Antarktiksen CRC ja Australian Antarctic Division, Hobart, Tasmania, Australia)
- (in) Yhdistyneiden Kansakuntien ympäristöohjelma (UNEP) - Kolmas arviointiraportti Climate Change 2001 , " Climate Change 2001: Working Group I: The Scientific Basis - Chapter 3. The Carbon Cycle and Atmospheric Carbon Dioxide " Tiivistelmä
- Planeetatiedot, CO 2 -pitoisuuskasvoi voimakkaasti vuodesta 1990 vuoteen 2004 (käytetty 31. maaliskuuta 2012)
- ESRL: n maailmanlaajuinen seurantaryhmä
- Tutkimusryhmän hiilen kierron kasvihuonekaasut
- Atmosphere Dossier , Pour la science , kesäkuu 1996
- Earth Guide / UCSD, ilmasto ja CO 2in the Atmosphere (käytetty 10. lokakuuta 2007)
- Robert A.Berner ja Zavareth Kothavala, GEOCARB III: Tarkistettu malli ilmakehän CO 2: staPhanerozoic over [PDF] , American Journal of Science , voi. 301, 2001, c. 2, s. 182-204, DOI : 10.2475 / ajs.301.2.182 (käytetty 15. helmikuuta 2008)
- Sigurdsson, Haraldur ja Houghton, BF, Tulivuoren tietosanakirja , 2000, Academic Press, San Diego ( ISBN 0-12-643140-X )
- van Gardingen, PR; Grace, J .; Jeffree, CE; Byari, SH; Miglietta, F. Raschi, A.; Bettarini, I., luku. Pitkän aikavälin vaikutukset parannettu CO 2pitoisuudet lehtiä kaasu vaihto: mahdollisuuksia tutkimukseen käyttämällä CO 2jouset , toimittaja: Raschi, A .; Miglietta, F.; Tognetti, R.; van Gardingen, PR (toim.), 1997, Cambridge University Press, Cambridge ( ISBN 0-521-58203-2 ) , s. 69-86
- Martini M., luku. CO 2päästöt tulivuorialueilla: tapaustiedot ja vaarat , laitoksen reaktioissa kohonneeseen CO 2: een: Todisteita luonnollisista lähteistä , toimittaja: Raschi, A.; Miglietta, F. Tognetti, R.; van Gardingen, PR (toim.), 1997, Cambridge University Press, Cambridge ( ISBN 0-521-58203-2 ) , s. 69-86
- Tulivuoren kaasut ja niiden vaikutukset (in) , tarkastettu 2007-09-07
- Martin Wolf, " Ilmastonmuutoksen skeptikot ovat menettämässä maata " , The New Economist ,17. heinäkuuta 2014(käytetty 26. heinäkuuta 2014 ) .
- " aina lisää CO 2ilmakehässä ”, La Croix ,30. lokakuuta 2017( ISSN 0242-6056 , luettu verkossa , käytetty 31. lokakuuta 2017 )
- Gamilloaug E., Ilmakehän hiili saavutti viime vuonna tason, jota ei ole nähty 800000 vuodessa , Science News , 2. elokuuta 2018
- " Globaalit CO 2 -päästöt”Livahtaa” vuonna 2018, on + 2,7% ” , on Liberation.fr (kuullaan päivänä joulukuuta 6, 2018 )
- " CO2 " .
- Lobell DB & Field CB (2008) Arvio hiilidioksidista (CO 2) Lannoitus vaikutus käyttäen kasvu poikkeavuuksien CO 2ja sadonkorjuu vuodesta 1961 . Glob Chang Biol. ; 14 (1): 39–45.
- FN Tubiello , JF Soussana ja SM Howden , " Kasvien ja laidunten vastaus ilmastonmuutokseen ",2007( PMID 18077401 , PMCID 2148358 , DOI 10,1073 / pnas.0701728104 , Bibcode 2007PNAS..10419686T ) ,s. 19686–19690
- (in) Rob Norton et ai. Kohonneen hiilidioksidin vaikutus vehnän kasvuun ja saantoon Australian Grains Free Air Carbon Dioxide Enrichment (AGFACE) -kokeessa , regional.org.au 2008
- (in) Daniel R. taub, vaikutukset Rising Ilmakehän hiilidioksidipitoisuuden yhden Kasvit , luonto , koulutus tieto 3 (10): 21, 2010
- (in) Taub DR, Miller B, Allen H. vaikutukset kohonnut CO2 proteiinipitoisuudesta elintarviketuotannon: meta-analyysi , Global Change Biology 1 maaliskuuhun ja 14 (3): 565-75 27. marraskuuta 2007
- (en) Myers SS Zanobetti A, Kloog I, P Huybers, Leakey AD, Bloom AJ et ai. (2014), CO2: n lisääntyminen uhkaa ihmisten ravitsemusta. Luonto . Kesäkuu; 510 (7503): 139.
- (sisään) Zhu C, Kobayashi K, Loladze I, Zhu J, Jiang Q, Xu et ai. (2018), hiilidioksidin (CO2) tasot tällä vuosisadalla muuttavat riisinjyvien proteiini-, hivenaine- ja vitamiinipitoisuutta, mikä saattaa aiheuttaa terveysvaikutuksia köyhimmille riisiriippuvaisille maille , Sci Adv. 2018: 4: eaaq1012.
- (in) Loladze I (2014 ) Kasvien ionomin piilotettu muutos, joka altistuu kohonneille hiilidioksidipäästöistä kärsiville mineraaleille ihmisten ravinnon perusteella , Elifa . ; 3: e02245.
- (in) Andrew A.Meharg, Jeanette Hartley-Whitaker (2002) Arseenin otto ja aineenvaihdunta arseeniresistentteissä ja ei-vastustuskykyisissä kasvilajeissa, julkaistu 4. huhtikuuta 2002 DOI: 10.1046 / j.1469-8137.2002.00363.x Issue New Phytologist , Osa 154, numero 1, sivut 29–43, huhtikuu 2002
- (en) Ebi KL, Ziska LH (2018) Ilmakehän hiilidioksidin lisääntyminen: Odotetut kielteiset vaikutukset elintarvikkeiden laatuun. PLoS Med 15 (7): e1002600. https://doi.org/10.1371/journal.pmed.1002600 ; Tutkimus julkaistu Creative Commons CC0: n julkisella lisenssillä
- (in) Helena Bottemiller evich, " suuri ravintoaine romahtaa " , poliittis ,13. syyskuuta 2017( lue verkossa , kuultu 13. syyskuuta 2017 ).
- (in) Weyant C Brandeau ML, Burke M, DB Lobell, Bendavid S & S Basu (2018), Ennakoitu taakka ja hiilidioksidin aiheuttamien ravitsemuksellisten puutteiden ja niihin liittyvien sairauksien lieventäminen: simulointimallinnustutkimus, PLoS Med. ; 15 (7): e1002586
- Vickers MH (2014) Varhaisen elämän ravitsemus, epigenetiikka ja myöhemmän elämän sairauden ohjelmointi . Ravinteet. 2. kesäkuuta; 6 (6): 2165–78.
- Zhu C, Zeng Q, McMichael A, Ebi KL, Ni K, Khan AS et ai. (2015) Historialliset ja kokeelliset todisteet artemesiniinin, globaalin malarialääkehoidon, lisääntyneestä konsentraatiosta, jossa ilmakehän hiilidioksidin viimeaikainen ja ennustettu kasvu . Ilmastonmuutos. 1. syyskuuta; 132 (2): 295–306
- Porter JR, Xie L, Challinor AJ, Cochrane K, Howden SM, Iqbal MM et ai. (2014) Elintarviketurva ja elintarviketuotantojärjestelmät . Julkaisussa: Ilmastonmuutos 2014: Vaikutukset, sopeutuminen ja heikkous. Osa A: Globaalit ja alakohtaiset näkökohdat. Työryhmän II panos hallitustenvälisen ilmastonmuutospaneelin viidenteen arviointiraporttiin [Field CB, Barros VR, Dokken DJ, Mach KJ, Mastrandrea MD, et ai. (toim.)]. Cambridge University Press, Cambridge, Iso-Britannia ja New York, NY, USA, s. 485–533
- Battisti DS & Naylor RL (2009) Historialliset varoitukset tulevasta elintarviketurvasta ennennäkemättömällä kausiluonteisella lämmöllä . Tiede 323, 240–244.
- (in) Nowak RS, SD Ellsworth DS ja Smith (2004), Kasvien toiminnalliset reaktiot kohonneeseen ilmakehän CO 2: een- tukevatko FACE-kokeiden fotosynteettiset ja tuottavuustiedot varhaisia ennusteita? , Uusi fytoli. , 162, 253–280 ( tiivistelmä )
- (sisään) Morgan JA et ai. (2004), CO 2parantaa tuottavuutta, muuttaa lajien koostumusta ja vähentää lyhytheinän arojen kasvillisuuden sulavuutta , Ecol. Appl. , 14, 208–219
- (in) JT Kiehl ja Kevin E. Trenberth, " Maan vuotuinen keskimääräinen energiabudjetti " , Bulletin of the American Meteorological Society , voi. 78, n ° 2Helmikuu 1997, s. 197-208 ( DOI 10.1175 / 2008BAMS2634.1 , luettavissa verkossa )
- (in) Ilmastonmuutos: Mistä tiedämme? , NASA, päivämäärätön
- (en) Emmanuel Quiroz, lämpötila ja CO 2Ice Core -tietueista löytyi korrelaatioita , päivämäärättömiä
- (in) Bärbel Hönisch Andy Ridgwe Daniela N.Schmidt, Ellen Thomas, Samantha J.Gibbs, Appy Sluijs, Richard Zeebe, Lee Kump, Rowan C.Martindale, Sarah E.Greene, Wolfgang Kiessling, Justin Ries, James C.Zachos , Dana L.Royer, Stephen Barker, Thomas M. Marchitto Jr. , Ryan Moyer, Carles Pelejero Patrizia Ziveri, Gavin L.Foster ja Branwen Williams, " The Geological Record of Ocean Acidification " , Science , voi. 335, n o 6072, 2. maaliskuuta 2012, s. 1058-1063 ( DOI 10.1126 / science.1208277 , lukea verkossa )
- (in) Joe Romm, Geological Society: Acidifying oceans spell meren biologinen sulaminen "vuosisadan loppuun mennessä" , Climate Progress , 31. elokuuta 2010
- (en) C. Langdon ja J. Atkinson, " Kohonneen p CO 2: n vaikutuskorallien fotosynteesistä ja kalkkeutumisesta sekä vuorovaikutuksista lämpötilan / säteilyn kausivaihtelun ja ravinteiden rikastumisen kanssa " , Journal of Geophysical Research , voi. 110,7. syyskuuta 2005, C09S07 ( DOI 10.1029 / 2004JC002576 , lue verkossa )
- (in) Katharina E.Fabricius, Chris Langdon, Sven Uthicke Craig Humphrey, Sam Noonan, Glenn De'ath, Remy Okazaki, Nancy Muehllehner, Martin S.Glas ja Janice M.Lough, " Häviäjät ja voittajat koralliriutoilla sopeutuneet kohonneet hiilidioksidipitoisuudet ” , Nature Climate Change , voi. 1,29. toukokuuta 2011, s. 165-169 ( DOI 10.1038 / nclimate1122 , luettavissa verkossa )
- (in) Joe Romm, Hiilidioksidi ajaa kalaa hulluksi ja uhkaa niiden selviytymistä, tutkimustulokset , ilmastonmuutos , 23. tammikuuta 2012.
- Sebastian Leuzinger ja Christian Korner ” sadannan jakautuminen on tärkein valunnan tulevissa CO 2keskittyminen lauhkeaan lehtipuumetsään ”, Glob. Vaihda Biol. , Voi. 16,2010, s. 246–254 ( yhteenveto )
- Peters, GP et ai. , Haaste pitää ilmaston lämpeneminen alle 2 ° C , Nature Clim. Muutos , 3, 4–6, 2013
- Reich PB ja Hobbien SE (2013), vuosikymmenen pitkä orgaanisen typen rajoittaa CO 2kasvien biomassan lannoitus , Nature Clim. Muutos , 3, 278-282 ( yhteenveto )
- Mark J. Hovenden, Paul CD Newton ja Karen E. Wills, " Kausittaiset, ei vuosittaiset sademäärät määrittävät nurmen biomassavasteen hiilidioksidille ", Nature , voi. 511,2014( DOI 10.1038 / nature13281 , yhteenveto )
- Sokolov AP et ai. (2008), hiili-typpi-vuorovaikutusten huomioon ottamisen vaikutukset ilmaston ja maanpäällisen hiilen kierron väliseen palautteeseen , J. Clim. , 21, 3776–3796 ( yhteenveto ja lähdeluettelo )
- Morgan J. et ai. (2011), C4-ruohot menestyvät, kun hiilidioksidi poistaa kuivumisen lämmitetyillä puolikuivilla niityillä , Nature , 476, 202–205 ( tiivistelmä )
- (en) Leakey A. et ai. (2009), kohonnut CO 2vaikutukset kasvien hiili-, typpi- ja vesisuhteisiin: kuusi tärkeää opetusta FACE: lta , J. Exp. Bot. , 60, 2859–2876 ( tiivistelmä )
- (in) McMurtrie, RE , et ai. (2008), Miksi kasvien kasvuvaste reagoi kohonneeseen CO 2: eenmonistuu, kun vesi on rajoittavaa, mutta vähennetään, kun typpi on rajoittava? Kasvun optimointihypoteesi , Funct. Plant Biol. , 35, 521–534
- PB Reich, SE Hobbie, T. Lee et ai. , " Typenrajoitus rajoittaa ekosysteemin kestävyyttä CO 2: een », Nature , voi. 440,2006, s. 922–925 ( yhteenveto )
- PB Reich, BA Hungate ja Y. Luo, “ Hiili-typpi-vuorovaikutukset maan ekosysteemeissä vasteena ilmakehän hiilidioksidin nousulle ”, Annu. Rev. Koulu. Evol. Syst. , Voi. 37,2006, s. 611-636 ( yhteenveto )
- J.A. Morgan, DE Pataki, C. Körner et ai. " Vesi suhteet nurmi ja desert ekosysteemin altistettiin koholla ilmakehän CO 2 », Oecologia , voi. 140,2004, s. 11–25 ( lue verkossa [PDF] )
- (en) Derner JD et ai. , C3- C4 -lajiseosten reaktiot maanpinnan ylä- ja alapuolella kohonneeseen CO 2: eenja maaperän veden saatavuus , Glob. Vaihda Biol. , 9, 452–460, 2003
- (en) Dukes JS et ai. (2005), Nurmen tuotannon vastaukset yksittäisiin ja moniin maailmanlaajuisiin ympäristömuutoksiin , PLoS Biol. , 3, 1829–1837 ( tiivistelmä
- Grunzweig JM ja Korner C. (2001), Kasvu-, vesi- ja typpisuhteet Israelin puolikuivan Negevin nurmikentän ekosysteemeissä, jotka ovat alttiina korkealle CO 2: lle, Oecologia , 128, 251–262 ( tiivistelmä )
- (en) Marissink M., Pettersson A. ja Sindhoj E. (2002) Maanpäällinen kasvien tuotanto kohonneessa hiilidioksidissa ruotsalaisessa puoliluonnollisessa nurmessa , Agric. Ekosysteemi. Noin. , 93, 107–120 ( tiivistelmä )
- (in) Singh D., Tsiang M. B. ja Rajaratnam Diffenbaugh NS (2013) Sateen ääripäitä yli Manner Yhdysvallat on ohimenevä, korkearesoluutioinen, koko ilmastomallien kokeilu , J. Geophys. Res. , D 118, 7063–7086 ( tiivistelmä )
- (sisään) Piao S. et ai. (2013), arviointi maanpäällisten hiilen kiertomalleista niiden reaktiona ilmaston vaihteluun ja CO 2: eentrendit , Glob. Vaihda Biol. , 19, 2117–2132 ( tiivistelmä )
- (in) De Kauwe MG et ai. (2013), Metsän vedenkäyttö ja vedenkäytön tehokkuus korkealla CO 2: lla: mallin ja datan vertailu kahdessa vastakkaisessa lauhkean metsän FACE-paikassa , Glob. Vaihda Biol. , 19, 1759–1779 ( tiivistelmä )
- " käynnistyminen CCSL ja Veolia poimii ja myydä CO 2suuressa mittakaavassa " ,30. maaliskuuta 2017.
- Kanadalainen tukena Bill Gates haluaa kaapata CO 2ilmassa , Le Figaro , 29. kesäkuuta 2019.
- (in) Richard Littlemore: "Voiko tämä yritys olla osallisena ilmastonmuutosratkaisussa?" , The Globe and Mail , raportti yrityslehdestä , lokakuu 2019
- Bonin J, Maurin A & Robert M (2017) Molecular katalyysin sähkökemiallisen ja fotokemiallinen vähentäminen CO 2Fe- ja Co -metallipohjaisilla komplekseilla. Viimeaikaiset edistysaskeleet . Coord. Chem. Ilm. 334, 184-198 | URL: https://www.researchgate.net/profile/Julien_Bonin/publication/308271980_Molecular_Catalysis_of_the_Electrochemical_and_Photochemical_Reduction_of_CO2_with_Fe_and_Co_Metal_Based_Complexes_Recent_Advances/links/5c0639fb299bf169ae3078e9/Molecular-Catalysis-of-the-Electrochemical-and-Photochemical-Reduction-of-CO2- kanssa-Fe-ja-Co-Metal-Based-Complexes-Recent-Advances.pdf
- Jhong HR.M, Ma S & Kenis PJA (2013) CO 2: n sähkökemiallinen konversiohyödyllisiä kemikaaleja: nykytila, jäljellä olevat haasteet ja tulevaisuuden mahdollisuudet . Curr. Opin. Chem. Eng. 2, 191–199 ( yhteenveto )
- Aresta M, Dibenedetto A & Angelini A (2014) Catalysis varten valorization pakokaasun hiiltä: CO 2kemikaaleihin, materiaaleihin ja polttoaineisiin . Hiilidioksidin tekninen käyttö. Chem. Rev. 114, 1709–1742 ( yhteenveto )
- Qiao J, Liu Y, Hong F & Zhang J (2014) Katsaus katalyytteihin hiilidioksidin sähkön vähentämiseksi vähähiilisten polttoaineiden tuottamiseksi . Chem. Soc. Ilm. 43, 631–675
- Parajuli R et ai. (2015) Maan runsaiden materiaalien anodisten ja katodisten katalyyttien integrointi tehokkaaseen, skaalautuvaan CO 2: eenvähennys . Alkuun. Catal. 58, 57–66
- Tatin A et ai. (2016) Tehokas elektrolysaattori CO 2: llehalkaisu neutraaliin veteen runsaalla maapallolla . Proc. Natl Acad. Sei. USA 113, 5526–5529 | URL: https://www.pnas.org/content/pnas/113/20/5526.full.pdf
- Sahara G & Ishitani O (2015) Tehokkaat valokatalyytit CO 2: llevähennys . Inorg. Chem. 54, 5096–5104 | URL: https://pubs.acs.org/doi/full/10.1021/ic502675a
- Takeda H, Cometto C, Ishitani O & Robert M (2017) Elektronit, fotonit, protonit ja maa-runsas metallikompleksien molekyyli- katalyysiin CO 2vähentäminen . ACS-katalysaattori. 7, 70–88 ( yhteenveto )
- Shen, J. et ai. (2015) Hiilidioksidin elektrokatalyyttinen pelkistys hiilimonoksidiksi ja metaaniksi immobilisoidussa kobolttiprotoporfyriinissä . Nat. Yleinen. 6, 8177 | URL: https://www.nature.com/articles/ncomms9177
- Weng Z et ai. (2016) Sähkökemiallinen CO 2pelkistäminen hiilivedyiksi heterogeenisellä molekyylipitoisella Cu-katalyytillä vesiliuoksessa . J. Am. Chem. Soc. 138, 8076–8079 | URL: https://pdfs.semanticscholar.org/a69e/11c9a8e97716bdbd4a24aa5e687f447616fa.pdf .
- Manthiram K, Beberwyck BJ & Alivisatos AP (2014) Hiilidioksidin tehostettu sähkökemiallinen metanointi dispergoituvan nanomittakaavan kuparikatalysaattorin avulla . J. Am. Chem. Soc. 136, 13319–13325
- Xie MS et ai. (URL: https://cloudfront.escholarship.org/dist/prd/content/qt4882v99t/qt4882v99t.pdf ) Aminohapolla modifioidut kuparielektrodit hiilidioksidin tehostetulle selektiiviselle sähköreduktiolle hiilivetyihin . Energia noin Sei. 9, 1687–1695 (2016)
- Wu T et ai. (2014) Hiilipohjainen valokatalyytti muuntaa tehokkaasti CO 2: nCH4: ään ja C2H2: een näkyvässä valossa . Green Chem. 16, 2142–2146
- AlOtaibi B, Fan S, Wang D, Ye J & Mi Z (2016) Kiekkojen tason keinotekoinen fotosynteesi CO 2: llevähentäminen CH4: ksi ja CO: ksi käyttämällä GaN -nanolankoja . ACS Catal. 5, 5342–5348 ( yhteenveto )
- Liu X, Inagaki S & Gong J (2016) Heterogeeniset molekyylijärjestelmät fotokatalyyttistä CO 2: ta vartenpelkistys veden hapettumisella . Angew. Chem. Int. Toim. 55, 14924–14950 ( abstrakti )
- Wang Y et ai. (2016) Helppo yksivaiheinen synteesi hybridigrafiittisesta hiilimonitridista ja hiilikomposiiteista korkean suorituskyvyn katalyytteinä CO 2: llefotokatalyyttinen muunnos . ACS Appl. Mater. Interf. 8, 17212–17219 ( yhteenveto )
- Zhu, S. et ai. (2016) CO 2: n fotokatalyyttinen pelkistysH2O: sta CH4: ään erittäin ohuilla SnNb2O6 2D -arkkeilla näkyvän valon säteilytyksessä . Green Chem. 18, 1355–1363 | URL: https://www.researchgate.net/profile/Ling_Wu10/publication/283244219_Photocatalytic_reduction_of_CO_2_with_H_2_O_to_CH_4_over_ultrathin_SnNb_2_O_6_2D_nanosheets_under_visible_light_irradiation/links/569dcad408ae950bd7a6b275.pdf )
- Yu L et ai. (2016) Hiilellä koristeltujen kuparioksidin mesohuokoisten nanorodien tehostettu aktiivisuus ja vakaus CO 2: llekeinotekoisen fotosynteesin väheneminen . ACS-katalysaattori. 6, 6444–6454 ( yhteenveto )
- Azcarate I, Costentin C, Robert M & Savéant J.-M (2016) Tutkimus avaruusvarauksen vuorovaikutusvaikutuksista molekyylikatalyysissä, mikä johti tehokkaimman CO2-CO-sähkökemiallisen konversion katalyytin suunnitteluun . J. Am. Chem. Soc. 138, 16639–16644
- Costentin C, Robert M, Savéant JM. & Tatin A (2015) Tehokas ja selektiivinen molekyylikatalyytti hiilidioksidi-CO-sähkökemialliseen muuntumiseen vedessä . Proc. Natl Acad. Sei. USA 112, 6882–6886
- Heng Rao, Luciana C. Schmidt, Julien Bonin ja Marc Robert (2018) ” Näkyvän valon ajettu metaanin muodostuminen CO 2molekyylirautakatalyytin kanssa "; Kirje | 17. heinäkuuta 2017 Luonto-osa 548, sivut 74–77 (3. elokuuta 2017) | URL: https://www.nature.com/articles/nature23016#ref2
- Li, X., Yu, J., Jaroniec, M., & Chen, X. (2019). Katalysaattorit CO 2 : n selektiiviseen valonsiirtoonaurinkopolttoaineiksi. Kemialliset arvostelut, 119 (6), 3962-4179. ( yhteenveto )
- Zhang, B., & Sun, L. (2019). Keinotekoinen fotosynteesi: molekyylikatalyyttien mahdollisuudet ja haasteet . Chemical Society Reviews, 48 (7), 2216-2264.
- Andrei V, Reuillard B & Reisner E (2019) Bias-free solar syngas tuotanto integroimalla molekyylikobolttikatalyytti perovskiitin - BiVO 4 tandemien kanssa . Luontomateriaalit, 1-6 ( yhteenveto )
- Dalle KE, Warnan J, Leung JJ, Reuillard B, Karmel IS & Reisner E (2019) Sähkö- ja aurinkoenergiainen polttoainesynteesi ensimmäisen rivin siirtymämetallikomplekseilla . Kemialliset arvostelut, 119 (4), 2752-2875 | URL: https://pubs.acs.org/doi/full/10.1021/acs.chemrev.8b00392 ( PDF-versio )
Katso myös
Bibliografia
- Gérard Borvon, Hiilen ja CO 2: n historia. Elämän alkuperästä ilmastonmuutokseen , Vuibert, 2013, 256 Sivumäärä