Dioxygen
| Dioxygen | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dioksidihapon edustukset. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Henkilöllisyystodistus | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| IUPAC-nimi | happi | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synonyymit |
molekyylihappi |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100,029,051 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O EY | 231-956-9 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ATC-koodi | V03 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o E | E948 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hymyilee |
O = O , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1 / O2 / c1-2 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ulkomuoto | väritön kaasu ympäristön lämpötilassa ja paineessa; nesteytetty kaasu : väritön tai sininen neste | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kemialliset ominaisuudet | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kaava |
O 2 [isomeerit] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Moolimassa | 31,9988 ± 0,0006 g / mol O 100%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molekyylihalkaisija | 0,292 nm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fyysiset ominaisuudet | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fuusio | -219 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° kiehuu | -183 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Liukoisuus | on veteen on 20 ° C : 3,1 ml / 100 ml, 14,6 mg l −1 (vesi 0 ° C: ssa ), |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tilavuusmassa |
yhtälö:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
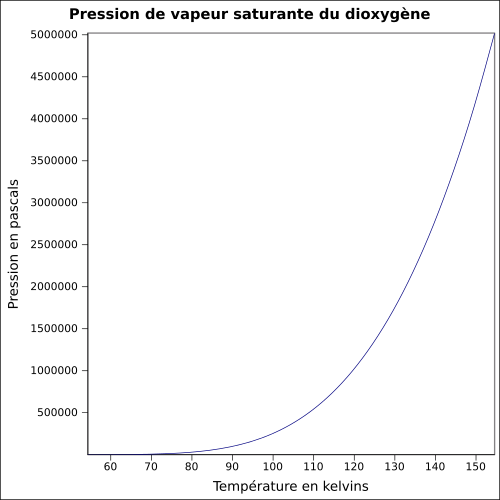
| Kyllästävä höyrynpaine | lämpötilassa -118 ° C : 5080 kPa
yhtälö:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kriittinen piste |
−118,67 ° C 50,422 bar 0,636 1 kg l −1 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kolmoispiste |
-218,7916 ° C 0,00149 bar |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Äänen nopeus | 330 m s −1 ( 27 ° C , 1 atm ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lämpökemia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| A fus H ° | 213 kJ / kg | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ vap H ° | 6,82 kJ mol −1 ( 1 atm , −182,95 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C s |
yhtälö:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Varotoimenpiteet | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Vaara H270, H270 : Voi aiheuttaa tai voimistaa tulipaloa; hapetin |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  A, C, : Puristettu kaasu kriittinen lämpötila = -118,57 ° C C : Hapettavat materiaali aiheuttaa tai edistää toisen materiaalin palamisen Disclosure 1,0% mukaan luokitteluperusteista |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 0 3 0 HÄRKÄ | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kuljetus | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
25 : hapettava kaasu (edistää tulipaloa) YK-numero : 1072 : PURISTETTU HAPEN LUOKKA: 2 Merkinnät: 2.2 : Palamattomat, myrkyttömät kaasut (vastaa A: n tai ison O: n osoittamia ryhmiä); 5.1 : Hapettavat aineet  
225 : jäähdytetty nesteytetty kaasu, hapetin (edistää tulipaloa) YK-numero : 1073 : JÄÄHDYTETTÄVÄ NESTEHAPEN LUOKKA: 2 Tarrat: 2.2 : Palamattomat, myrkyttömät kaasut (vastaa isoja A tai O: n osoittamia ryhmiä); 5.1 : Hapettavat aineet   |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SI- ja STP- yksiköt, ellei toisin mainita. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Dihappea , jota yleisesti kutsutaan happi on aine , joka koostuu molekyyleistä O 2 (joka koostuu kahdesta atomien ja happea ). Kaasu on vakio-olosuhteet lämpötilan ja paineen , väritön, hajuton ja mauton, se osallistuu hapetus-pelkistys-reaktioita , pääasiassa polttava , korroosiota ja hengitystä . Dioxygen on yksi hapen allotrooppisista muodoista .
Nimitys " happi " ilman tarkkuutta on epäselvä, koska tämä termi voi osoittaa alkuaineen happea (O) tai happikaasua (O 2). Vaikka otsoni O 3 on myös suurimolekyylistä yhdistettä elementin happea, se on yleensä dihappili-, joka on tarkoitettu, kun termejä "molekulaarisen hapen" ja "happi-molekyyli" käytetään.
Löysi itsenäisesti vuonna 1772, jonka ruotsalainen Carl Wilhelm Scheele vuonna Uppsalassa , ja vuonna 1774 vuoteen britti Joseph Priestley vuonna Wiltshire , happi nimettiin niin vuonna 1777, jonka ranskalainen Antoine Lavoisier ja hänen vaimonsa Pariisiin päässä antiikin Kreikan ὀξύς / oxús ( "akuutti", joka on sanoa tässä "happo") ja γενής / genếs ("generaattori"), koska Lavoisier ajatteli virheellisesti - hapettuminen ja happamoituminen liittyvät toisiinsa - että:
"Olemme antaneet pohjan hengittävä osan ilman nimen happea, johtuvat sen kahdesta kreikan sanoista ὀξύς , hapan ja γείνομαι , minä tuottaa , koska todellakin yksi yleinen ominaisuuksia tämän perusteella [Lavoisier puhuu hapen] on muodostamaan happoja yhdistämällä useimpiin aineisiin. Siksi kutsumme happikaasua tämän emäksen liitokseksi kalorien kanssa. "
Diokseni muodostaa 20,95 tilavuusprosenttia maapallon ilmakehästä (23,2 painoprosenttia), ja se on välttämätön kaasu useimmille nykyisille elämänmuodoille, jolle se toimittaa solujen toiminnalle ( soluhengitys ) tarvittavan hapettimen . Vesiympäristössä liuennutta happea tarvitaan myös monien lajien elämään. Vain arkeus ja vähemmistöosa bakteereista (kutsutaan anaerobeiksi ) voivat toimia ilman happea. Ne tuottavat anaerobisia happibakteereja, jotka ovat hapettaneet alkukehän alun perin pelkistämällä ja sitten rikastaneet happea: sitä on ilmassa runsaasti suuren hapetuksen jälkeen , on noin 2,4 miljardia vuotta.
Hapen alkuperä ja kehitys maan ilmakehässä
Hypoteesin ilmakehässä selittämiseksi on esitetty monia hypoteeseja:
- yleisimmin käytetty on, että se on kaasu aikana tuotettu toimivuuteen syanobakteerien , ja yleisemmin chlorophyllian kasvien , talteen hiili päässä hiilidioksidia (muodossa orgaaniset yhdisteet) ja hylättiin happi (muodossa dihappi) mekanismilla fotosynteesi ;
- toisen vetoaa hajoaminen, ylemmässä ilmakehässä , on vesimolekyylien osaksi dihappi ja vety , vaikutuksesta auringon ja kosmisen säteilyn. Kun divety poistuu lopulta avaruuteen (tällä hetkellä noin 3 kg / s ), happi kerääntyy ilmakehään.
Kaksi olemassa olevaa ilmiötä, todellisuus, voivat olla kahden prosessin yhdistelmä.
Syanobakteerit
4 miljardia vuotta sitten maapallo oli melkein kokonaan peitetty valtamerillä, ja sen ilmakehä koostui metaanista, ammoniakista ja hiilidioksidista. Ensimmäiset meressä olevat bakteerit käyttävät fermentointia yksinomaan energialähteenä. Vähitellen kehittyessään he voivat käyttää auringonvaloa energialähteenä , hiilidioksidina .hiilenlähteenä ja H 2 Otai H 2 Svedyn lähteenä. Se on fotosynteesin ulkonäkö . Nämä autotrofiset , toisin sanoen kykenevät luomaan omat ravintoaineet, organisaatiot kehittyvät, leviävät ja mutatoituvat syanobakteereiksi, joita on 3,2 miljardia vuotta.
Nämä syanobakteerit käyttävät vettä vedyn lähteenä ja vapauttavat dioksihappoa ympäristöönsä, joka on tappava myrkky kaikille muille anaerobisille bakteereille . Tämä hapen kilpailu bakteerien välillä on ratkaiseva käännekohta elämän kehityksessä. Syanobakteerien lisääntyminen muuttaa täysin ilmakehän ja valtamerien koostumusta rikastamalla niitä hapella. Samanaikaisesti bakteerit kehittyvät voidakseen käyttää tätä dioksidia aineenvaihdunnassa fermentaation sijasta. Ne ovat ensimmäisiä organismeja, jotka suorittavat soluhengityksen . Hengityksen energiantuotot ovat todellakin paljon korkeammat kuin käyminen, mikä antaa näille eläville olennoille tärkeimmän evoluutioedun.
Noin 2 miljardia vuotta sitten primitiivinen eukaryoottinen (anaerobinen) solu nieli bakteerin, joka kykenee suorittamaan hengityksen. Tästä fagosytoosin sisäistämästä bakteerista tulee mitokondrioita , joita on tällä hetkellä kaikissa aerobisissa soluissa. Voidaan myös huomata, että mitokondrioilla on oma DNA , jolla on kaikki bakteeri- DNA: n ( pyöreä DNA ) ominaisuudet.
Happitason kehitys maapallon ilmakehässä
Dioksidia ei ollut melkein ollenkaan maapallon ilmakehässä ennen arkkien ja bakteerien kehittymistä, todennäköisesti noin 3,5 miljardia vuotta sitten. Vapaassa tilassa olevaa dioksidihappoa esiintyi ensimmäisen kerran merkittävissä määrissä paleoproterotsooosin aikana (noin 2,5 - 1,6 miljardia vuotta sitten). Ensimmäisten miljardin vuoden aikana kaikki näiden organismien tuottama happi yhdistyy liuenneen raudan kanssa valtamerissä muodostaen raidoitettuja rautamuodostumia . Kun nämä hapen nielut ovat kyllästettyjä, vapaata happea alkaa vapautua valtameristä 2,7 miljardia vuotta sitten. Sen pitoisuus saavutti 10% nykyisestä tasostaan noin 1,7 miljardia vuotta sitten.
Suuren määrän liuenneen hapen esiintyminen valtamerissä ja ilmakehässä on saattanut johtaa sittemmin elävien anaerobisten organismien sukupuuttoon noin 2,4 miljardia vuotta sitten suureksi hapetukseksi kutsutun ekologisen kriisin aikana. Happea käyttävä soluhengitys antaa kuitenkin aerobisille organismeille mahdollisuuden tuottaa paljon enemmän ATP: tä kuin anaerobiset organismit, mikä auttaa heitä hallitsemaan maapallon biosfääriä .
Kambriumian 540 miljoonan vuoden takaisesta alusta lähtien hapen pitoisuus ilmakehässä on kehittynyt, mikä on ajan mittaan 15-30% sen tilavuudesta. Kohti loppua hiilikaudella noin 300 miljoonaa vuotta sitten, ilmakehän happipitoisuus saavutti huippunsa: se sitten oli 35% tilavuudesta ilmakehän, jotka olisivat voineet osaltaan suuren koon hyönteisten ja sammakkoeläinten ajasta. Tämä huippu sen osuus maapallon ilmakehään tällä hetkellä johtuu massiivinen laajentuminen on valtava saniainen metsien päälle Pangea , ja vähitellen hautaaminen orgaanisten tuotteiden tuli hiili talletukset . Ihmisen toiminnalla, mukaan lukien 7 miljardin tonnin fossiilisten polttoaineiden polttaminen vuosittain, on hyvin vähän vaikutuksia vapaan hapen määrään ilmakehässä. Nykyisellä fotosynteesinopeudella kaiken ilmakehässä olevan hapen tuottaminen vie noin 2000 vuotta.
Biologiset roolit
Fotosynteesi
Luonnossa, vapaata happea tuotetaan fotolyysin on veden kautta fotosynteesin . Joidenkin arvioiden mukaan viherlevän ja syanobakteerien löytyy meriympäristön noin 70%: n vapaata happea tuotetaan maapallolla, loput on tuotettu maanpäällisten kasvien . Muiden arvioiden mukaan valtamerien osuus ilmakehän hapen saannista on suurempi, toiset taas päinvastoin, mikä viittaa siihen, että valtameret tuottavat noin 45% ilmakehän hapesta vuosittain.
Kirjoitetaan maailmanlaajuinen ja yksinkertaistettu kaava, joka kääntää fotosynteesiä:6 CO 2+ 6 H 2 O+ Fotonit → C 6 H 12 O 6+ 6 O 2
tai yksinkertaisesti: hiilidioksidi + vesi + auringonvalo → glukoosi + happi.
Dioksibin fotolyyttinen evoluutio tapahtuu fotosynteettisten organismien tyliakoidissa ja vaatii neljän fotonin energiaa . Monet vaiheet ovat monimutkaisia, mutta tulos on muodostumista sähkökemiallisen gradientin koko thilakoid, jota käytetään syntetisoimaan adenosiinitrifosfaatin (ATP) kautta prosessin photophosphorylation . Vesimolekyylin hapettumisen jälkeen jäljellä oleva dioksihappo vapautuu ilmakehään.
Hengitys
Happihappo on välttämätöntä soluhengityksessä kaikissa aerobisissa organismeissa . Mitokondriot käyttää sitä auttaa ATP: n tuotannon prosessissa oksidatiivisen fosforylaation . Reaktiomallinnus aerobista hengitystä on yleensä päinvastoin kuin mallinnus fotosynteesi ja se kirjoitetaan yksinkertaistetulla tavalla ja glukoosin hapettumisen saannon ollessa 100%: n saanto:C 6 H 12 O 6+ 6 O 2→ 6 CO 2+ 6 H 2 O+ 2880 kJ mol −1 .Itse asiassa energiaa käytetään ADP: n muodostamisen aikana (molekyyli, joka sallii energian varastoinnin soluun) ADP: stä, samoin kuin mahdollistamaan reaktiolle tarvittavien molekyylien kuljettaminen solun sisällä. Täten ATP: n muodossa tosiasiallisesti varastoitu ja elimistön käyttämä energia on siis pikemminkin 1162,8 kJ yhdelle moolille kulutettua glukoosia, toisin sanoen:C 6 H 12 O 6+ 6 O 2→ 6 CO 2+ 6 H 2 O+ 1162,8 kJ mol -1 .Vuonna selkärankaisia , happi leviää kalvojen läpi solujen keuhkoihin ja punasoluja . Hemoglobiini sitoo happea ja aiheuttaa värin muutoksen proteiinin kulkee sinertävän punainen kirkkaan punainen. Muut eläimet eivät käytä hemoglobiinia hapen kuljettamiseen: nilviäiset ja jotkut niveljalkaiset käyttävät hemosyaniinia, kun taas hämähäkit ja hummerit käyttävät hemerythriiniä . Yksi litra verta voi liuottaa 200 cm 3 happea.
Reaktiiviset johdannaiset happea , kuten ioni superoksidin O 2- ja vetyperoksidi H 2 O 2ovat myrkyllisiä sivutuotteita, joita organismit käyttävät. Osa kehittyneiden organismien immuunijärjestelmästä tuottaa kuitenkin peroksidia, superoksidia ja singletti-happea tunkeutuvien mikro-organismien tappamiseksi . Reaktiivisilla dioksidihappojohdannaisilla on myös tärkeä rooli kasvien yliherkässä reaktiossa patogeenisiä hyökkäyksiä vastaan.
Lepoinen aikuinen hengittää 1,8 - 2,4 grammaa happea minuutissa. Tämä vastaa yli kuutta miljardia tonnia ihmiskunnan hengittämää happea vuodessa.
Aerobinen hengitys on absorboida happea tarpeen katabolian oksidatiivisen ja osuus energian soluihin. Organismeilla on rajoittava imeytymiskyky , nimeltään suurin hapenottokyky .
Hapen kulutus on soluaktiivisuuden indeksi. Tämä huomautus on peräisin vesinäytteen biologisesti hajoavasta pilaantumisesta, biologisesta hapenkulutuksesta .
Läsnäolo selkärankaisten kehossa
Se on hengityselimissä kuin hapen osapaine elävän selkärankaisen kehossa on korkein. Se on heikointa valtimoissa , sitten ääreiskudoksissa ja vielä enemmän suonissa . Dioksidin osapaine on paine, joka dioksiinilla olisi, jos se yksin vie tarkasteltavan tilavuuden.
| Yksikkö | Kaasun paine keuhkojen alveoleissa |
Valtimon verikaasu | Verikaasu suonissa |
|---|---|---|---|
| kPa | 14.2 | 11–13 | 4.0–5.3 |
| mmHg | 107 | 75–100 | 30-40 |
Rakenne
Geometrinen rakenne
Molekyyli on piimaa ja keskimääräinen etäisyys kahden atomin välillä on perustilassa 120,74 um .
Kahdessa ensimmäisessä viritetyssä tilassa (katso alla oleva spektroskooppiosa) tämä etäisyys kasvaa 121,55 μm : iin ensimmäisessä tilassa ja 122,77 μm : iin toisessa tilassa.
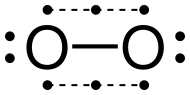
Lewisin edustus
Lewisin nykyinen hapen esitys siten, että sen kaksi atomia seuraavat tavusääntöä , on kaksoissidos , jolloin kukin atomi kantaa lisäksi kahta jakamatonta elektronidublettia . Tämä rakenne ei kuitenkaan ota huomioon tämän molekyylin paramagnetismia . On mahdollista ehdottaa Lewis-kaaviota, joka kunnioittaa tätä kokeellista havaintoa yhdellä sidoksella (eikä kaksoissidoksella) ja yhdellä elektronilla happiatomia kohden.
Epätavanomaisella esityksellä yhdellä sidoksella on haittana se, että ei oteta huomioon lyhyttä sidosetäisyyttä ( d = 120,74 pm ), joka on paljon lyhyempi kuin yksittäinen OO-sidos, kuten vetyperoksidissa. HOOH, jonka sidoksen pituus on 145,7 pm . Tämä selittää erityisesti, miksi tätä rakennetta käytetään käytännössä vain koulutustarkoituksiin korostaakseen molekyylin Diradical- luonteen . Tehokkaampi kuvaus saadaan molekyylipyörillä .
Molekyylirata-kaavio
Teoreettisessa viitekehyksessä ( CLOA-menetelmä ) kahden happiatomin välinen vuorovaikutus molekyylin muodostamiseksi heijastuu vastakkaisessa kaaviossa.
Kahden happiatomin kaksi 2s-orbitaalia, jotka ovat alun perin saman energian omaavia, rappeutuvat muodostaen sitovan σ 2s- ja σ-kiertoradan*
2s antiliantti, molemmat täysin miehitettyinä, jolloin näiden kahden atomin välillä ei ole sidosta. Kuusi 2p-orbitaalien kahden atomin läpikäydä myös rappeutumista, jotka muodostavat kolme σ 2px , σ 2PY ja σ 2PZ orbitaalien ja kolme σ orbitaalien* 2
kuvapistettä , σ*
2py ja σ*
2pz liima-aineet. Kahdeksan (2 × 4) 2p-elektronia jakautuu seuraavasti:
- kuusi elektronia vievät kolme vähän energiaa sitovaa orbitaalia;
- loput kaksi elektronia kumpikin vievät antiliaatin kiertoradan.
Tämä 2p-orbitaalien yhdistelmä johtaa siis kolmeen sitoutuvaan molekyyliorbitaaliin ja yhteen antilianttiin, toisin sanoen sitoutumisindeksiin 2. Kahden elektronin jakautuminen kahdelle antiliaatiosta selittää myös dioksidin diradiaalisen luonteen. Tämä ominaisuus olla radikaali, kun taas elektronien määrä molekyyleissä on tasainen, on ainutlaatuinen piimaamolekyylien keskuudessa. Tämä jakauma selittää myös dioksidin paramagneettisen luonteen, jota ei voida ennustaa sen "klassisesta" Lewis-esityksestä.
Tämä triplettitilan tila antaa molekyylille magneettiset ominaisuudet (katso alla) ja voidaan saattaa sen kemiallisesta inertiteetistä huoneenlämpötilassa. Todellakin, reaktio O 2toisen molekyylin (H 2, orgaaniset molekyylit), joka on melkein aina singlettitilassa muodostaakseen molekyylin singlettitilassa, etenee ilman kokonais spinin säilymistä; tämä on syy happeen liittyvien kemiallisten reaktioiden suurelle hitaudelle normaalissa lämpötilassa ja paineessa.
Spektroskopia
Kaksi ensimmäistä viritettyä happitasoa ovat kaksi singlettitilaa 15 800 cm- 1: ssä ( 94,72 kJ mol- 1 ) ja 21 100 cm -1: ssä ( 157,85 kJ mol- 1 ) (katso kaavio). Nämä siirtymät ovat spin-kiellettyjä, mikä johtaa hapen värittömyyteen. Näin on kaasufaasissa, jossa ilmakehän sininen väri johtuu Rayleigh-sironnasta .
Sininen väri nestemäisessä tilassa (katso alla) johtuu kahden fotonin absorptiosta 7 918 cm- 1 : ssä kahden dioksigeenimolekyylin ( O 4- dimeeri ) yhdistelmällä.
Magnetismi
Happihappo on paramagneettista . Faraday havaitsi tämän ominaisuuden jo vuonna 1848. CLOA-menetelmällä jäljitetty happimolekyylinen kiertoradakaavio heijastaa tätä. Elektroninen konfiguraatio sisältää todellakin kaksi yksittäistä elektronia kahdella Π * orbitaalilla ( triplettitila ).
In -ydinmagneettinen resonanssi (NMR), hienoksi mittauksia, on tärkeää kaasun poistamiseksi näyte poistaa molekulaarista happea, joka on paramagneettinen ja häiritsevät havaitseminen aiheuttaa piikit laajenevat. Tämä kaasunpoisto toteutetaan yleensä kuplittamalla liuoksessa inerttiä kaasua (typpeä tai argonia) tämän inertin ja ei-magneettisen kaasun liuenneiden kaasujen korvaamiseksi.
Tuotanto
Teollisuustuotanto
Dioksihappo saadaan teollisesti pääasiassa (95%: lla) erottamalla yhdisteet kryogeenisesti ilmasta , toisin sanoen ilman nesteytyksellä ja sen jälkeen jakotislauksella .
Kriittinen lämpötila on typpi N 2( T c = -146,9 ° C ) ja happi O 2( T c = −118,4 ° C ) eivät salli ilman nesteytystä yksinkertaisesti puristamalla . Ilma on näin ollen puristaa välillä 5 ja 7 bar, sitten suodatetaan, kuivataan, hiilihappo jonka adsorptio on molekyyliseulan ja lopuksi jäähdytetään lämmönvaihto tulevan kaasun ja nesteytetyt kaasut. Jäähdytyshäviöt kompensoidaan laajennuksella 5-10% käsitellystä kaasuvirrasta turbiinissa, jonka ulkopuolinen työ on palautettavissa.
Tislaus suoritetaan yleisimmin käytetyssä prosessissa kaksoispylväässä, mikä mahdollistaa jatkuvasti puhtaiden kaasujen saamisen. Ensimmäisessä pylväässä (keskipaine, 5 bar) ilma erotetaan ensimmäisen kerran puhtaaksi kaasumaiseksi typpikaasuksi (99,999%) yläosassa ja happipitoiseen nesteeseen (noin 40%) pohjassa. Tämä neste lähetetään sitten toisen tislauskolonnin puoliväliin (matala paine, 1,3 bar). Happi O 299,5% - 99,7% saadaan talteen tämän toisen kolonnin pohjalta. Se sisältää vähemmän kuin 1 ppm typpeä, pääasiallinen epäpuhtaus on argoni .
Tislauspylväiden halkaisija on 1-6 m ja niiden korkeus on 15-25 m . Ne on valmistettu ruostumattomasta teräksestä tai alumiinista ja niissä on noin sata tarjotinta. Lämmöneristys suoritetaan perliitillä (paisutetulla piihiekalla). Pylväiden lämpötilan ylläpitäminen kuluttaa vain 6-7% kokonaismenotuksesta.
Energiankulutus on 0,4 kWh m −3 kaasumaista happea eli 50-60% omakustannushinnasta.
Noin 5% teollisesta hapesta tuotetaan toisella ei-kryogeenisellä prosessilla, jota kutsutaan VPSA: ksi ( tyhjiö-paine-swing-adsorptio ) tai adsorptioksi vaihtamalla paine ja tyhjiö.
Ympäristön ilma kuivattiin ja puhdistettiin suodattamalla, sitten se kulkee pylvään läpi zeoliitteja , jotka adsorboivat typen N 2 nopeammin.kuin happi O 2. Zeoliitit voivat kiinnittää 10 litraa typpeä kilogrammaa kohden. Kun ne ovat tyydyttyneitä, ilma lähetetään toiseen kolonniin, kun taas ensimmäisestä kolonnista peräisin oleva typpi desorboituu tyhjössä. Täten poistamalla typpi ilmasta saadun dioksidin puhtaus voi olla 90 - 95%. Tämä dioksihappo sisältää edelleen 4,5% argonia, jota dioksibin tapaan ei adsorboida. Energiankulutus on 0,4-0,5 kWh m −3 happea. Tätä menetelmää käytetään yhä enemmän teollisissa prosesseissa, joiden tarve on alle 100 tonnia päivässä, sekä kotona käytetyissä hengityssuojaimissa. Katso myös happikonsentraattori .
Tuotettu happi kuljetetaan:
- nestemäisessä tai kaasumaisessa muodossa putkistojen kautta, joita kutsutaan oksideiksi tai happiputkiksi ;
- kaasumaisessa muodossa puristettuna terässylintereihin tai säiliöihin 200 baarin paineella;
- nestemäisessä muodossa, säiliöautoissa .
Vuonna 1995 kahdeksan yritystä ympäri maailmaa valmisti melkein kaiken teollisen hapen:
- Air Liquide (Ranska): 17%;
- BOC (Yhdistynyt kuningaskunta): 14% (Linde osti vuonna 2006);
- Praxair (Yhdysvallat): 14%;
- Air Products (Yhdysvallat): 8%;
- Nippon Sanso (Japani): 7%;
- AGA (Ruotsi): 7% (Linde osti vuonna 2000);
- Messer (Saksa): 6%;
- Linde (Saksa): 6%.
Tärkeimmät tuottajamaat vuonna 1996 olivat:
- Yhdysvallat: 27 miljoonaa tonnia;
- Japani: 12,7 miljoonaa tonnia;
- Ranska: 3,23 miljoonaa tonnia.
Maailmanlaajuisesti kokonaistuotanto oli noin 100 miljoonaa tonnia vuonna 1996, tai 1 / 10 miljoonasosaa happea ilmakehään.
Laboratoriossa
Dioksidia on jo pitkään valmistettu laboratoriossa pieninä määrinä oksyyli- Na 2 O 2 : n reaktiolla vedellä.
Se voidaan tuotetaan katalyyttisen hajoamisen ja vetyperoksidin läsnä ollessa mangaanin ( IV ) oksidi MnO 2.
Nämä kaksi tuotantomenetelmää käyttävät yleensä vedensiirtokokoonpanoa tuotetun hapen keräämiseksi.
Se voidaan valmistaa myös veden elektrolyysillä opetusnäytöksiä varten, mutta tämä tekniikka on hidasta ja kallista energiaa.
Reaktiivisuus
Dioxygen on termodynaamisesti hyvin reaktiivinen, ja suurin osa sen reaktioista on voimakkaasti eksotermisiä. Tämä suuri reaktiivisuus ei yleensä tapahdu huoneen lämpötilassa. Kineettiset syyt on kuvattu edellä.
Yksinkertaisilla rungoilla
Harvat yksinkertaiset kappaleet eivät yhdisty suoraan hapen kanssa: volframi W, platina Pt, kulta Au ja jalokaasut . On huomattava, että hapetetut yhdisteet jalokaasujen olemassa kuitenkin (Xeo 3), mutta niitä ei koskaan voitu saada suoralla toiminnalla O 2: n kanssa.
Se, että oksideja on melkein kaikille kemiallisille alkuaineille, auttoi suurelta osin Mendelejevia luokittelemaan alkuaineet ( 1869 ). Lisäksi se seikka, että tietyt osat on useita eri oksideja (esimerkiksi typpi ) oli alkuperä syntyminen käsitteen atomin mukaan Dalton ( 1800 ).
-Ioneja O 2
Monet O 2: n ionit tunnetaan:
- dioxygenyl ioni , O 2+ , harvinaisissa yhdisteissä;
- superoksidi -ioni , O 2- , usein anioni biologisissa järjestelmissä, joissa redox on usein monoelektroninen; se on epävakaa kokonaisuus;
- peroksidi -ionin O 22- , anioni yhteinen metallin peroksidit, kuten bariumperoksidi BaO 2 ; dioksidilla on sama hapettumisaste kuin vetyperoksidissa H 2 O 2.
Reaktio singlettihappea 1 O 2
Yksittäinen dioksibigeeni tuotetaan triplettidioksidin (sen perustila ) 3 O 2 : n kevyellä säteilytyksellävaloherkistimellä. Tätä varten jälkimmäisen viritetyn tilan on oltava suurempi kuin 94,7 kJ mol -1 (katso yllä oleva spektroskooppiosa ).3 O 2+ 1 herkistin - hν → 1 O 2+ 3 herkistin.
Yksittäistä dioksidihappea voidaan tuottaa myös kemiallisesti, esimerkiksi alkoholiliuoksessa, vetyperoksidin ja valkaisuaineen seoksella :H 2 O 2+ CIO - → Cl - + H 2 O+ 1 O 2.
Singletidiokseni on erittäin reaktiivinen sekä kemiallisesti että biologisesti.
Käyttää
Ilmassa olevaa dioksidia käytetään polttamiseen (lämmitys, kuljetus).
Erotettuna typestä, sen pääasiallinen käyttö on terästeollisuudessa . Rauta jättäen masuuneissa on muodossa Fe 3 C karbidi, käyttökelvoton, koska se sisältää yli 4 painoprosenttia hiiltä. Tämä hiili poltetaan ruiskuttamalla happea suoraan sulaan rautaan. Tämä on muuntimien periaate . 60 m 3 CNTP O 2 tarvitaantonnia rautaa. Terästehtaan kulutus on tuhansia tonneja O 2: ta päivässä.
Petrokemian on myös tärkeä kuluttajan, kun se tulee tuottaa etyleenioksidia , ja propyleenioksidin , ja vinyylikloridin mukaan oksiklooraus , jalostuksen öljytuotteiden, regeneroimiseksi katalyyttejä, jne.
Muut prosessit vaativat myös suuria happimääriä:
- synteesi titaanidioksidin , että klooria prosessia ;
- valkaistaan ja massan , joka rajoittaa kulutusta klooria Cl 2 , joka on edelleen tärkein valkaisuaine;
- tiettyjen kemiallisten jätteiden, esimerkiksi metyylimetakrylaatin tuotannossa syntyvää rikkipitoista jätettä, jälleenkäsittely , mikä johtaa H 2 SO 4: n talteenottoon.
Muita satunnaisia käyttötarkoituksia ovat esimerkiksi:
- liekkien tuottaminen korkeassa lämpötilassa, kuten oksi- vetypoltin ;
- lääketieteellisenä kaasuna :
- Normobaarinen happihoito (ilmakehän paineessa): hengitysvaikeuksien omaavien ihmisten hengitystukessa (sairaudet, kuten astma tai krooninen hengitysvajaus tai anestesian aikana ), keinotekoiseen tuuletukseen ( hengityksen lopettaminen ),
- hyperbarinen happiterapia (korkea paine): tiettyjen kaasumyrkytysten (erityisesti hiilimonoksidin ), sukelluksen paineonnettomuuksien tai tiettyjen palovammojen, tiettyjen valtimoiden patologioiden hoitoon .
-
Kaavio muuntimesta, jossa happea syötetään suoraan sulaan metalliin.
-
Muunnin toiminnassa; sulan raudan reaktio hapen kanssa tuottaa valosuihkuja.
-
Pullotettu lääketieteellinen happi.
Eri
Dioksihappo on osa Maailman terveysjärjestön välttämättömien lääkkeiden malliluetteloa (luettelo päivitetty vuonna 2007)Huhtikuu 2013).
Huomautuksia ja viitteitä
Huomautuksia
- Sama epäselvyys koskee monia muita elementtejä ( vety , typpi , kloori , jne. ).
- Hiilidioksidi vapautuu toisesta osasta hemoglobiinin kautta Bohrin ilmiö .
- (1,8 grammaa / minuutti per henkilö) × (60 minuuttia / tunti) × (24 tuntia päivässä) × (365 päivää / vuosi ) × (6,6 miljardia ihmistä) ÷ (1 000 000 grammaa tonnilta) = 6,24 miljardia tonnia.
Viitteet
- OXYGENE et OXYGENE (LIQUEFIED) , kemiallisten aineiden turvallisuuden kansainvälisen ohjelman käyttöturvallisuustiedotteet, joita on käyty 9. toukokuuta 2009.
- laskettu molekyylimassa välillä " Atomic painot Elements 2007 " on www.chem.qmul.ac.uk .
- CAS-numeron "7782-44-7" merkitseminen IFA: n (saksalainen työturvallisuudesta ja -terveydestä vastaavan elimen) kemikaalitietokantaan GESTIS ( saksa , englanti ), pääsy 28. tammikuuta 2009 (vaaditaan JavaScriptiä) .
- (en) Robert H. Perry ja Donald W. Green , Perry's Chemical Engineers 'Handbook , Yhdysvallat, McGraw-Hill,1997, 7 th ed. , 2400 Sivumäärä ( ISBN 0-07-049841-5 ) , s. 2-50.
- pöytäkirja kansainvälisen komitean painoista ja mitoista , 78 th istunto, 1989, s. T1-T21 (ja s. T23-T42, englanninkielinen versio).
- (in) WM Haynes, Handbook of Chemistry and Physics , CRC, 2010-2011 91 th ed. , 2610 Sivumäärä ( ISBN 978-1-4398-2077-3 ) , s. 14–40.
- (in) David R. LiDE, CRC Handbook of Chemistry and Physics , CRC Press,2009, 90 th ed. , 2804 Sivumäärä , Kovakantinen ( ISBN 978-1-4200-9084-0 ).
- Indeksinumero taulukossa 3.1 liitteen VI : n asetuksen N o 1272/2008 (16 joulukuu 2008).
- " Happi " kemiallisten tuotteiden tietokannassa Reptox of CSST (Quebecin organisaatio, joka vastaa työturvallisuudesta ja työturvallisuudesta), käyty 25. huhtikuuta 2009.
- Lavoisier A. (1789). Kemian perustutkielma , 1864, s. 48 .
- (in) University of Wisconsin. (2006), Liuennut happi: vesiympäristö riippuu siitä , Water Action Volunteers-Volunteer Stream Monitoring Factsheet Series , luettu verkossa ( luettu 25. helmikuuta 2010).
- " Mikä oli maapallon ilmakehään kuin 4000000000vuosi sitten?" - notre-planete.info ” , osoitteessa our-planete.info (kuultu 15. helmikuuta 2018 ) .
- (in) Heinrich D. Holland, "hapetus ilmakehän ja valtamerten" , Phil. Trans. R. Soc. B , 361, 903–915, 19. toukokuuta 2006, DOI : 10.1098 / rstb.2006.1838 .
- Archean .
- Varhainen proterotsooinen .
- Suurin osa proteroosista .
- Myöhäinen proterotsooinen .
- Phanerozoic .
- (in) Neil A. Campbell ja Jane B. Reece , Biology , San Francisco, Pearson-Benjamin Cummings2005, 7 th ed. , 1231 Sivumäärä ( ISBN 0-8053-7171-0 ) , s. 522-23.
- (in) Scott Freeman , biologian, 2. , Upper Saddle River, NJ, Pearson-Prentice Hall,2005( ISBN 0-13-140941-7 ) , s. 214, 586.
- (en) Robert A. Berner , “ Atmospheric oxigen over Phanerozoic time ” , Proceedings of the National Academy of Sciences of USA , voi. 96, n ° 20,1999, s. 10955–57 ( PMID 10500106 , DOI 10.1073 / pnas.96.20.10955 , lue verkossa ).
-
DOI : 10.1111 / j.1472-4669.2009.00188.x
Tämä tarjous luodaan muutamassa minuutissa. Voit ohittaa hännän tai täydentää sen käsin . - (en) John Emsley , Nature's Building Blocks: AZ Guide to the Elements , Oxford, Englanti, Oxford University Press ,2001, 538 Sivumäärä ( ISBN 0-19-850340-7 , lue verkossa ) , s. 297-304.
- (in) Malcolm Dole , " The Natural History of Oxygen " , The Journal of General Physiology , vol. 49, n o 1,1965, s. 5–27 ( PMID 5859927 , DOI 10.1085 / jp.49.1.5 , lue verkossa ).
- (in) William Fenical , "Marine Kasvit: ainutlaatuinen ja tutkimaton Resource" in kasvit: mahdollisuudet talteen proteiinia, lääkkeitä, ja muuta hyödyllistä Chemicals (työpaja menettely) Diane Publishing,Syyskuu 1983( ISBN 1-4289-2397-7 , luettu verkossa ) , s. 147.
- (in) JCG Walker , happisykli luonnossa ja biogeokemialliset syklit , Springer-Verlag ,1980.
- (in) Theodore L. Brown ja Burslen LeMay , Kemia: Central Science , Prentice Hall / Pearson Education,2003( ISBN 0-13-048450-4 ) , s. 958.
- (en) Peter H.Raven , Ray F.Evert ja Susan E.Eichhorn , Kasvien biologia, 7. painos , New York, WH Freeman and Company Publishers,2005( ISBN 0-7167-1007-2 ) , s. 115-27.
- “ The Ingredients of Life in Earth and Space ” , Euroopan avaruusjärjestö (käytetty 28. kesäkuuta 2013 ) , s. 3.
- (in) Albert Stwertka , elementteihin Guide , Oxford University Press ,1998, 240 Sivumäärä ( ISBN 0-19-508083-1 ) , s. 48-49.
- Charles A. Janeway ja Paul Travers ( trans. Vuodesta Englanti) Immunobiologian: perus- ja patologinen immuunijärjestelmän , Pariisi / Bryssel, De Boeck,2003, 784 Sivumäärä ( ISBN 2-7445-0150-6 ) , s. 41.
- (in) " Virtauksenrajoitin hengitysparametrien mittaamiseen " , Patenstorm (tarkastettu 28. kesäkuuta 2013 ) : " Ihmisille normaali tilavuus on 6-8 litraa minuutissa. " .
- (in) Charles Henricksonin , kemia Cliffs Notes2005, 440 Sivumäärä ( ISBN 0-7645-7419-1 ).
- Tulos, joka saadaan arvoista mmHg käyttäen muunnosta 0,133 322 kPa / mmHg .
- (in) ' Normal Reference Range Table ' , The University of Texas Southwestern Medical Center, Dallas (käytetty 28. kesäkuuta 2013 ) .
- (in) " The Medical Education Division of the Brookside Associates → ABG (Arterial Blood Gas) " (käytetty 28. kesäkuuta 2013 ) .
- Elementtien kemia , s. 606.
- (in) NN Greenwood ja A. Earnshaw, kemian elementit , Boston Oxford, Butterworth-Heinemann,1997, 2 nd ed. ( 1 st ed. 1984), 1341 s. ( ISBN 978-0-7506-3365-9 , OCLC 804401792 ) , s. 615.
- Vigne J.-L., Teollisuustiedot .
- (in) WHO: n tärkeiden lääkkeiden malliluettelo , 18. luettelo , huhtikuu 2013.
Katso myös
Aiheeseen liittyvät artikkelit
Bibliografia
- Davis JC (1975), Vesipohjainen liuenneen hapen tarve ja kriteerit painottaen erityisesti Kanadan ympäristöä , Associate Committee on Scientific Criteria for Quality , National