Tetrametyylisilaani
| Tetrametyylisilaani | |||
|
|||
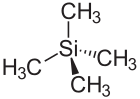
| Tetrametyylisilaanin rakenne | |||
| Henkilöllisyystodistus | |||
|---|---|---|---|
| IUPAC-nimi | Tetrametyylisilaani | ||
| Synonyymit |
TMS |
||
| N o CAS | |||
| N o ECHA | 100 000 818 | ||
| N O EY | 200-899-1 | ||
| N o RTECS | VV5706000 | ||
| PubChem | 6396 | ||
| ChEBI | 85361 | ||
| Hymyilee |
C [Si] (C) (C) C , |
||
| InChI |
Std. InChI: InChI = 1S / C4H12Si / c1-5 (2,3) 4 / h1-4H3 Vakio. InChIKey: CZDYPVPMEAXLPK-UHFFFAOYSA-N |
||
| Ulkomuoto | Väritön, helposti syttyvä neste, joka muodostaa räjähtäviä seoksia ilman kanssa | ||
| Kemialliset ominaisuudet | |||
| Raaka kaava |
C 4 H 12 Si [Isomeerit] |
||
| Moolimassa | 88,2236 ± 0,0043 g / mol C 54,46%, H 13,71%, Si 31,83%, |
||
| Molekyylihalkaisija | 0,596 nm | ||
| Fyysiset ominaisuudet | |||
| T ° fuusio | -102 ° C | ||
| T ° kiehuu | 26 ° C | ||
| Liukoisuus | 0,02 g · L -1 - 25 ° C | ||
| Liukoisuusparametri δ | 12,6 J 1/2 · cm -3/2 ( 25 ° C ) | ||
| Tilavuusmassa | 0,65 g · cm -3 kohteeseen 20 ° C: ssa | ||
| Itsesyttymislämpötila lämpötilan | 330 ° C | ||
| Leimahduspiste | -20 ° C | ||
| Räjähdysrajat ilmassa | 1 tilavuusprosenttia (36 g / m 3 ) 37,9 tilavuusprosentissa. (1385 g / m 3 ) | ||
| Kyllästävä höyrynpaine | 75 kPa ajan 20 ° C: ssa | ||
| Sähköiset ominaisuudet | |||
| 1 re ionisaatioenergia | 9,80 ± 0,04 eV | ||
| Varotoimenpiteet | |||
| SGH | |||
 Vaara H224, P210, P240, P243, P403 + P235, H224 : Erittäin helposti syttyvä neste ja höyry P210 : Suojaa lämmöltä / kipinöiltä / avotulelta / kuumilta pinnoilta. - Tupakointi kielletty. P240 : Astian ja vastaanottolaitteiden maadoitus / potentiaalintasaus. P243 : Suojaa staattisen sähkön purkautumiselta. P403 + P235 : Varastoi paikassa, jossa on hyvä ilmanvaihto. Pysyä rauhallisena. |
|||
| NFPA 704 | |||
| 4 1 1 | |||
| Kuljetus | |||
33 : erittäin helposti syttyvä neste materiaali (leimahduspiste on alle 21 ° C: ssa ) YK-numero : 2749 : tetrametyylisilaani Luokka: 3 Levy: 3 : Palavat nesteet Pakkaus: Pakkaus ryhmä I : erittäin vaarallisia aineita;  |
|||
| SI- ja STP- yksiköt, ellei toisin mainita. | |||
Tetrametyylisilaania , tai TMS , on kemiallinen yhdiste on kaava Si (CH 3 ) 4. Tämä orgaaninen piiyhdiste on erittäin haihtuvan värittömän nesteen muodossa - sen kiehumispiste on vain 26 ° C - erittäin helposti syttyvä ja kykenevä muodostamaan räjähtäviä seoksia ilman kanssa. Se on kemiallisesti suhteellisen inertti. Toiminta n- butyylilitiumia LiCH 2 CH 2 CH 2 CH 3tetrametyylisilaanilla johtaa sen deprotonointiin ja antaa trimetyylisilyylimetyylilitium Si (CH 3 ) 3 CH 2 Li, joka on suhteellisen yleinen alkylointiaine . Tetrametyylisilaania on myös esiaste on piidioksidin ja piikarbidin tekniikoissa on CVD ( CVD ).
Valmistautuminen
Tetrametyylisilaani on sivutuote metyylikloorisilaanien synteesissä SiCl n (CH 3 ) 4– nreaktiolla kloorimetaani CH 3 : llaon pii . Hyödyllisimmät tuotteet tässä synteesissä ovat tuotteet, joissa n = 1, 2 tai 3 , vastaavasti trimetyylisilyylikloridi SiCl (CH 3 ) 3, Dimetyylidikloorisilaania SiCl 2 (CH 3 ) 2ja metyylitrikloorisilaanin SiCl 3 CH 3 ; ja n = 4 , se on piitetrakloridia SiCl 4ja, sillä n = 0 , tetrametyylisilaania Si (CH 3 ) 4.
Tetrametyylisilaania voidaan valmistaa piitetrakloridista SiCl 4ja metyylimagnesiumkloridi CH 3 MgBrjonka Grignard-reaktiossa . Se voidaan myös valmistaa saattamalla trimetyylisilyylikloridi SiCl (CH 3 ) 3natrium- metyylialumiiniseskvikloridi kloridi nach 3 AICI 3 :
3 NaCI + AICI 3+ 2 AI + 3 CH 3 : lla⟶ 3 nach 3 AICI 3 ; Nach 3 AICI 3+ SiCl (CH 3 ) 3⟶ Si (CH 3 ) 4+ NaAlCl 4 (sisään) .Vuonna 1865 yksi ensimmäisistä trimetyylisilaanin synteeseistä Charles Friedel ja James Mason Crafts käsitteli piitetrakloridia SiCl 4kanssa dimetyylisinkki Zn (CH 3 ) 2 :
SiCl 4+ 2 Zn (CH 3 ) 2⟶ Si (CH 3 ) 4+ 2 ZnCI 2.Sovellukset
Tetrametyylisilaania käytetään kalibrointiin sisäisesti kemialliset siirtymät ja NMR-spektroskopia on 1 H , 13 C ja 29 Jos on orgaanisia liuottimia , joissa TMS on liukeneva - δ ( 1 H TMS) = 0,0 ppm määritelmän mukaan. On vesi , jossa TMS ei ole liukoinen, natrium trimethylsilylproprionate (de) (TPS) (CH 3 ) 3 SiCH 2 CH 2 COO käytetään- Na + tai natrium- suoloja ja DSS (CH 3 ) 3 SiCH 2 CH 2 CH 2 SO 3 - Na + . TMS: n haihtuvuus antaa sen haihtua helposti, mikä helpottaa NMR-spektroskopialla analysoitujen näytteiden talteenottoa.
Vaikka tetrametyylisilaania on kemiallisesti melko inertti, se on käytetty menestyksellisesti metyloimalla aineena on transmetallointi reaktiot :
Si (CH 3 ) 4+ GaCl 3 (en) ⟶ SiCl (CH 3 ) 3+ GaCl 2 CH 3.Huomautuksia ja viitteitä
- Merkintä "Tetrametyylisilaani" IFA: n (saksalainen työturvallisuudesta ja -terveydestä vastaavan elimen) kemikaalitietokantaan GESTIS ( saksa , englanti ), pääsy 30. tammikuuta 2021 (vaaditaan JavaScriptiä)
- (sisään) Yitzhak Marcus, The Properties of Solvents , voi. 4, John Wiley & Sons Ltd, 1999, 239 Sivumäärä ( ISBN 0-471-98369-1 )
- laskettu molekyylimassa välillä " Atomic painot Elements 2007 " on www.chem.qmul.ac.uk .
- (in) David R. LiDE, Handbook of Chemistry and Physics , 89 th painos., CRC Press, 2008, s. 10-205 . ( ISBN 978-1420066791 )
- " Tetrametyylisilaania yhdiste arkki, 99,9% " , on Alfa Aesar (näytetty päivänä tammikuuta 30, 2021 ) .
- (de) Georg Brauer, yhdessä Marianne Baudler, Handbuch der Chemie Präparativen Anorganischen , 3 e toim. tarkistettu, voi. Minä, Ferdinand Enke, Stuttgart 1975, s. 705 . ( ISBN 3-432-02328-6 )
- (de) JM Crasts ja C. Friedel , " Ueber das Siliciummethyl und die Kieselsäure-Methylather " , Justus Liebigs Annalen der Chemie , voi. 136, n o 2 1865, s. 203-212 ( DOI 10.1002 / jlac.18651360217 , lue verkossa )
- (in) Jerry R. Mohrig Christina Noring Hammond, Paul F. Schatz, tekniikoita Organic Chemistry , WH Freeman, 2006, s. 273–274 . ( ISBN 978-0-7167-6935-4 )
- (in) H. ja W. Schmidbaur Findeiss , " Yksinkertainen Reitti organogallium yhdisteet " , Angewandte Chemie International Edition , Vol. 3, n o 10, Lokakuu 1964, s. 696-696 ( DOI 10.1002 / anie.196406961 , lue verkossa )
