Butaanihappo
| Butaanihappo | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Henkilöllisyystodistus | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| IUPAC-nimi | Butaanihappo | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synonyymit |
voihappo |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100,003,212 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O EY | 203-532-3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Huumeiden pankki | DB03568 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| FEMA | 2221 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hymyilee |
CCCC (= O) O , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1 / C4H8O2 / c1-2-3-4 (5) 6 / h2-3H2,1H3, (H, 5,6) / f / h5H |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ulkomuoto | väritön, öljyinen neste, jolla on tyypillinen haju. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kemialliset ominaisuudet | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Raaka kaava |
C 4 H 8 O 2 [Isomeerit] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Moolimassa | 88,1051 ± 0,0044 g / mol C 54,53%, H 9,15%, O 36,32%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molekyylihalkaisija | 0,560 nm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fyysiset ominaisuudet | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fuusio | -7,9 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° kiehuu | 164 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Liukoisuus | veteen: sekoittuu, Sekoittuu etanolilla , eetterillä |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Liukoisuusparametri δ |
21,5 MPa 1/2 ( 25 ° C ); 25,1 J 1/2 · cm -3/2 ( 25 ° C ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tilavuusmassa |
0,959 g · ml -1 - 20 ° C 0,964 g · ml -1 - 25 ° C yhtälö:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Itsesyttymislämpötila lämpötilan | 452 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Leimahduspiste | 72 ° C (suljettu kuppi) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Räjähdysrajat ilmassa | 2 - 10 til-% | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kyllästävä höyrynpaine | ajan 20 ° C : 57 Pa
yhtälö:

|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kriittinen piste | 52,7 bar , 354,85 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lämpökemia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
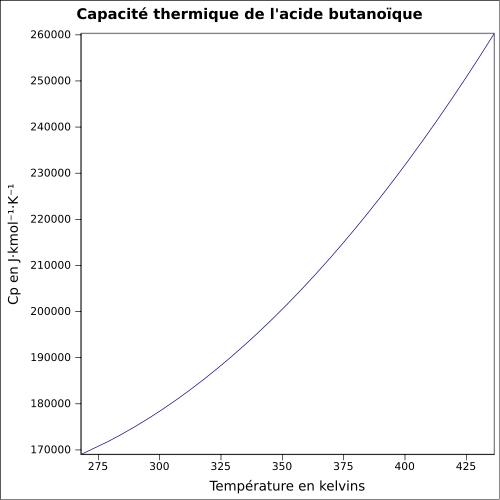
| C s |
yhtälö:
yhtälö:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sähköiset ominaisuudet | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 re ionisaatioenergia | 10,17 ± 0,05 eV (kaasu) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Optiset ominaisuudet | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Taitekerroin | 1.398 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Varotoimenpiteet | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Vaara H314, H314 : Voimakkaasti ihoa syövyttävää ja silmiä vaurioittavaa |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
Luokittelematon tuoteTämän tuotteen luokitusta ei ole vielä vahvistettu myrkyllisyyshakemistopalvelun ilmoituksessa (1,0%) ainesosaluettelon mukaan |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2 3 0 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kuljetus | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
2820 : VoiHappo |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ekotoksikologia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| DL 50 | 8,79 g · kg -1 (rotat, suun kautta) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LogP | 0,79 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SI- ja STP- yksiköt, ellei toisin mainita. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Butaanihappo , jota kutsutaan myös voihappo Kreikka βουτυρος ( voi ) on karboksyylihappo , joka oli kyllästetty kaava CH 3 CH 2 CH 2 -COOH
Sitä löytyy esimerkiksi röyhkeästä voista , parmesaanista ja mahalaukun sisällöstä , josta se antaa voimakkaan ja epämiellyttävän hajun. Voihappoa voidaan nähdä noin 5 - 40 ug / m 3 lähteestä riippuen.
Alle vakio-olosuhteet lämpötilan ja paineen , butaanihappo on hieman öljyinen neste, joka kiinteytyy -8 ° C: ssa ja jonka kiehumispiste on 164 ° C . Se liukenee helposti veteen , etanoliin ja eetteriin ja irtoaa liuottimestaan lisäämällä kalsiumkloridia . Kaliumdikromaatti ja rikkihapon hapettua osaksi hiilidioksidia ja etikkahappoa , ja kaliumpermanganaatin alkalioksidimoolia vain hiilidioksidia . Lisäksi, sen isomeeri rakenne 2-metyylipropanoiinihappo , joka on velkaa sen toinen nimi isovoihappoa.
Se on myös lyhytketjuinen rasvahappo, jota löytyy kasviöljyistä ja eläinrasvoista. Glyseridi ( esteri on glyseroli ) voihapon käsittää 3%: sta 4% voita. Kun voi rikkoutuu, glyseridit hydrolysoituvat vapauttaen epämiellyttävän hajuista voihappoa. Normaali voihappo tai käymisen voihappo myös löydetä heksyyli esterin , että öljy Heracleum giganteum ja oktyyli- esteri että palsternakka ( Pastinaca sativa ); sitä esiintyy myös hikoilussa .
Se on yleensä tuotettu fermentoimalla ja sokeria tai tärkkelystä , aiheuttama lisäämällä mätäneminen juustoa , jonka kalsiumkarbonaattia lisätään happojen neutraloimiseksi on muodostettu prosessissa. Tärkkelyksen voihappokäymistä helpottaa Bacillus subtiliksen suora lisääminen .
Erilaisia estereitä saadaan voihaposta. Näitä estereitä kutsutaan butyraatiksi tai oikeammin butanoaatiksi . Niillä, joilla on pieni moolimassa, kuten metyylibutanoaatilla , on enimmäkseen miellyttäviä aromeja. Niitä käytetään siten elintarvikelisäaineina tai hajusteissa.
Sen raaka kaava on sama kuin propyyliformiaatin .
Käyttää
Butaanihappo käytetään valmistuksessa eri makuja ( butanoaatti esterit ), alhaisen molekyylipainon voihapon esterit, kuten metyyli butanoaattia, on, että suurin osa, miellyttävä tuoksu tai maku. Siksi niitä käytetään elintarvikkeiden ja hajusteiden lisäaineina.
Vahvan tuoksunsa ansiosta sitä käytetään myös lisäaineena syöttiä varten. Monissa markkinoilla olevissa tavallisen karpin ( Cyprinus carpio ) syötteissä käytettävissä aromeissa esteripohjana käytetään voihappoa, mutta ei ole selvää, houkuttelevatko kalat itse voihappo vai muut lisäaineet. Voihappo on kuitenkin yksi harvoista orgaanisista hapoista, jotka osoittautuvat maukkaiksi sekä siipille että kovakuoriaiselle .
Anekdotisesti tätä ainetta on käytetty myös myrkyttömänä, pahoinvointia aiheuttavana, lihaa pilaavana valaan hylkivänä aineena Sea Shepherd -ryhmässä japanilaisten valaanpyytäjien tehdasalusta ja abortin vastaisia aktivisteja vastaan; jotkut poliisivoimat harkitsevat myös sen käyttämistä ei-tappavana aseena .
Butyraattien valmistus
Klassinen käyminen
Butyaanihapon esterit, butyraatit tai oikein butanoaatit, ovat peräisin fermentaatioista, joihin liittyy anaerobisia bakteereja . Tämän prosessin löysi Louis Pasteur vuonna 1861 . Tärkeimmät butyraatteja tuottavat bakteerit ovat:
- Clostridium butyricum ;
- Clostridium kluyveri ;
- Clostridium pasteurianum ;
- Fusobacterium nucleatum ;
- Butyrivibrio fibrisolvens ;
- Eubacterium limosum ;
- Clostridium tyrobutyricum .
Reaktion tulokset ovat seuraavat:
C 6 H 12 O 6 → C 4 H 8 O 2 + 2 CO 2 + 2 H 2Ensimmäinen vaihe tuotannon butanoates seuraa metabolisen ketju on glykolyysin , mikä johtaa siihen, että muodostuu kaksi molekyylien ja pyruvaattia molekyyliä kohti glukoosia . Pyruvaatti jälkeen saatu hapetetaan ja etanoaatti ( asetaatti muodossa etanoyyli-koentsyymi A ), jonka ainutlaatuinen entsymaattinen prosessi , johon liittyy sarja entsyymejä, joita kutsutaan pyruvaattidehydrogenaasin monimutkainen , kanssa rinnakkain muodostumista hiilidioksidia (CO 2), joka sitten poistuu solusta diffuusiolla ja pelkistämällä NAD + NADH: ksi.
- Etanoyyli-koentsyymi A muuttuu asetoasetyyli-koentsyymiksi A. Vastuussa oleva entsyymi on asetyyli-CoA-asetyylitransferaasi.
- Asetoasetyyli-koentsyymi A muuttuu P-hydroksibutyryyli-CoA: ksi. vastuussa oleva entsyymi on β-ketoasyyli-CoA-reduktaasi (koentsyymi: NADH).
- Β-hydroksibutyryyli-CoA muuntuu krotonyyli-CoA: ksi. vastuussa oleva entsyymi on β-hydroksiasyylidehydraasi.
- Krotonyyli-CoA muuttuu butyyli-CoA (CH 3 CH 2 CH 2). vastuussa oleva entsyymi on enoyyli-CoA-reduktaasi (koentsyymi: NADH).
- Fosfaatti ryhmä korvaa CoA muodostamiseksi butyylifosfaattia. Vastuussa oleva entsyymi on fosfobutyrylaasi.
- Fosfaattiryhmä liittyy ADP : hen muodostaen ATP: n ja butyraatit; aikaansaava entsyymi on butyraattia kinaasi .
Asetoni ja butyraattien käyminen
Jotkut bakteerit tuottavat asetonia ja butanolia toisella prosessilla, joka alkaa butyraattien käymisestä, kuten:
- Clostridium acetobutylicum : (tärkein, käytetty kemianteollisuudessa)
- Clostridium beijerinckii
- Clostridium tetanomorphum
- Clostridium aurantibutyricum
Nämä bakteerit seuraavat edellä kuvattua käymisprosessia, mutta kun pH on alle 5, ne siirtyvät butanolin ja asetonin tuotantoon estääkseen edelleen heille kohtalokkaan pH-arvon laskun. Yhdelle asetonimolekyylille tuotetaan kaksi butanolimolekyyliä. Modifikaatio tapahtuu asetoasetyyli-CoA: n muodostumisen jälkeen. Tämä välittäjä voi näissä olosuhteissa toimia kahdella uudella tavalla:
- Asetoasetyyli CoA → asetoasetaatti → asetoni
- Asetoasetyyli CoA → butyryyli CoA → butanaali → butanoli.
Butaanihapon fysiologinen aktiivisuus
Voihappo voi estää toiminnan histoni -deasetylaasin, mikä lisää osuus asetyloitua histonien, joilla on pienempi affiniteetti DNA: ta kuin ei-asetyloitu muodossa (johtuen sähköstaattisten hylkivä syistä). On yleisesti hyväksyttyä, että transkriptiotekijöiden sitoutuminen DNA: han on haitaksi asetyloimattomien histonien läsnäololla (joilla on pieni affiniteetti DNA: ta kohtaan). Siksi on mahdollista päätellä, että voihappo lisää solun transkriptionaalista aktiivisuutta histonideasetylaasien säätelemien promoottorien tasolla.
Voihappoa tuottaa nisäkkäiden suoliston mikrobiota . Sen tuotantoa vahvistavat prebioottiset aineet ( liukoiset kuidut ). Se toimii polttoaineena suoliston limakalvolle ja paikallisena ja systeemisenä immunostimulaattorina. Se antaisi immuunijärjestelmälle mahdollisuuden erottaa symbioottisten bakteerien aiheuttama kolonisointi ja patogeenit , kuten kolera .
Voihapolla on kationi- tai esterimuodossa virus-, sieni- ja antibakteerisia ominaisuuksia. Sen kiinnostus tähän muotoon on ennen kaikkea sen kyvyssä säätää syöpäsoluja ja indusoida solujen erilaistumista.
Lähde
- ( fr ) Tämä artikkeli on osittain tai kokonaan otettu Wikipedian englanninkielisestä artikkelista " Butyric acid " ( katso kirjoittajaluettelo ) .
- VUTARIHAPPO , kemikaaliturvallisuusohjelman käyttöturvallisuustiedote (t) , kuultu 9. toukokuuta 2009
- (sisään) Yitzhak Marcus, The Properties of Solvents , voi. 4, Englanti, John Wiley & Sons Ltd,1999, 239 Sivumäärä ( ISBN 0-471-98369-1 )
- laskettu molekyylimassa välillä " Atomic painot Elements 2007 " on www.chem.qmul.ac.uk .
- (in) James E. Mark, Physical Properties of Polymer Handbook , Springer,2007, 2 nd ed. , 1076 Sivumäärä ( ISBN 0387690026 , lue verkossa ) , s. 294
- (en) Robert H. Perry ja Donald W. Green , Perry's Chemical Engineers 'Handbook , USA, McGraw-Hill,1997, 7 th ed. , 2400 Sivumäärä ( ISBN 0-07-049841-5 ) , s. 2-50
- " Eri kaasujen ominaisuudet ", osoitteessa flexwareinc.com (käytetty 12. huhtikuuta 2010 )
- (in) Carl L. leuat, Handbook of termodynaamiset kaaviot , Voi. 1, Huston, Texas, Persianlahden pubi. Co,1996( ISBN 0-88415-857-8 )
- (in) David R. LiDE, Handbook of Chemistry and Physics , CRC,2008, 89 th ed. , 2736 Sivumäärä ( ISBN 978-1-4200-6679-1 ) , s. 10-205
- Indeksinumero EY-asetuksen N: o 1272/2008 liitteen VI taulukossa 3.1 (16. joulukuuta 2008)
- " Voihappoa " tietokannassa kemiallisten tuotteiden Reptox n CSST (Quebec organisaatio, joka vastaa työsuojelun), pääsee 25 huhtikuu 2009
- " Luku 4, Akuutit riskit, lisääntymiselle vaaralliset vaikutukset ja hajujen havaitseminen " osoitteessa invs.sante.fr
- (in) " Pakastinsyötit " , Nutrabaits
- AO Kasumyan ja KB Døving , “ Taste preferences in fishes ”, Fish and Fisheries , voi. 4,2003, s. 289–347 ( DOI 10.1046 / j.1467-2979.2003.00121.x )
- (in) " happoja polttavien aktivistien vahingoittamat japanilaiset valaanpyytäjät " , newser.com,2010
- (in) " Väkivallan historia: voihappohyökkäykset " , National Abort Federation, 1998
- PR Pouillart , " Voihapon ja sen johdannaisten rooli paksusuolen syövän ja hemoglobinopatioiden hoidossa ", Life Sciences , voi. 63,1. st tammikuu 1998, s. 1739-1760 ( ISSN 0024-3205 , PMID 9820119 , luettu verkossa , käytetty 29. joulukuuta 2015 )
- (fi-FI) “ Prebiootit: sisäpuutarhamme hoitaminen | NutritionFacts.org ” (käytetty 24. helmikuuta 2019 )
- Philippe R. Pouillart , Flore Dépeint , Afif Abdelnour ja Laetitia Deremaux , ” Nutriose Prebiootti alhainen sulavia hiilihydraatteja, stimuloi suoliston limakalvon immuniteetin ja estää TNBS-indusoidun paksusuolentulehduksen porsaiden ”, tulehduksellisten suolistosairauksien , voi. 16,1. st toukokuu 2010, s. 783-794 ( ISSN 1536-4844 , PMID 19998458 , DOI 10.1002 / ibd.21130 , luettu verkossa , käytetty 29. joulukuuta 2015 )
Bibliografia
Voet & Voet; John Wiley & Sons, 1995