Atominen kiertorata
In kvanttimekaniikan , atomiorbitaali on matemaattinen funktio , joka kuvaa aallon käyttäytyminen olevan elektronin tai pari elektronit atomin . Tämä toiminto antaa todennäköisyyden atomin elektronin läsnäololle tietyllä tämän atomin alueella. Siten sitä edustetaan usein isosurfacien avulla , jotka rajaavat alueen, jonka sisällä elektronin läsnäolon todennäköisyys on suurempi kuin annettu kynnys, esimerkiksi 90%. Tällaiset alueet eivät välttämättä ole yhteydessä toisiinsa ja voivat muodostaa pallomaisista yliaaltoista johtuvia monimutkaisia muotoja .
Jokainen atomirata on määritelty ainutlaatuisella kvanttilukujen tripletillä ( n , ℓ , m ℓ ) , jotka edustavat vastaavasti elektronin energiaa , sen kulmamomenttia ja tämän kulmamomentin projektiota tietyllä akselilla. Kukin näistä orbitaalien voi täyttyä enintään kaksi elektronia eroavat toisistaan niiden magneettinen kvanttiluku spin m s . Puhumme s , p , d ja f orbitaaleja tarkoittamaan orbitaalit määritelty kulma vauhtia ℓ yhtä suuri kuin 0, 1, 2 ja 3, vastaavasti. Nämä nimet tulevat vanhasta nimet spektriviivojen , että alkalimetallien kuvattu terävä , pää- , haja- ja hieno tai perustavanlaatuinen ; orbitaalit vastaa ℓ > 3 on sitten nimetty aakkosjärjestyksessä g , h , i , k , jne. , j-kirjain jätetään pois, koska jotkut kielet eivät erota sitä i-kirjaimesta.
Atomiradat ovat elektronipilven alkuaineosia, mikä tekee mahdolliseksi mallintaa elektronien käyttäytymistä aineessa. Tässä mallissa monielektroniatomin elektronipilvi voidaan arvioida elektronikonfiguraatioksi, joka muodostuu useiden hydrogeenisten orbitaalien tuotteesta . Rakenne jaksollisen elementtien sisään lohkojen käsittää kullakin ajan , yhteensä 2, 6, 10 tai 14 elementtiä , on suora seuraus enimmäismäärä elektroneja, jotka voivat viedä atomiorbitaali s , p , d ja f .
Elektronin ominaisuudet
Kvanttiluonto
Kehittäminen kvanttimekaniikan ja kokeellisia havaintoja, kuten diffraktion olevan elektronin palkin kautta Youngin rakojen perustettu Aaltohiukkasdualismi kuvaamaan alkeishiukkasten . Siten elektronit eivät kiertävät Atomiydinten vuonna määritelty kiertoradat kuin planeetat ympärille Auringon tehdä . Itse asiassa niitä ei voida kuvata pieninä kiinteinä palloina, jotka määritellään sijainnin ja nopeuden avulla ytimen ympärillä. Sen sijaan niitä tulisi nähdä seisovina aaltoina, jotka vievät tilavuuden, jossa niillä on määritetyt kvanttiominaisuudet ja jotka kykenevät vuorovaikutukseen muiden hiukkasten kanssa.
- Korpuskulaarinen luonne :
- atomissa voi olla vain kokonaismäärä elektroneja;
- energianvaihto tulevan hiukkasen, esimerkiksi fotonin , ja atomin elektronien välillä koskee aina vain yhtä elektronia kaikkien muiden poissulkemiseksi, vaikka usealla elektronilla on nollasta poikkeava todennäköisyys olla samanaikaisesti paikka, jossa yksi heistä on vuorovaikutuksessa tämän fotonin kanssa;
- elektronilla on selkeä ja vakio sähkövaraus , ja se esittää spinin, jonka projektio kvantisointiakselilla voi olla yhtä suuri kuin +12(pyöritä ylös ) tai -12(pyöritä alas ).
- Aaltoluonne :
- vähintään elektronin energia vastaa valtion verrattavissa perustaajuus värähtelyn merkkijonon, joka tunnetaan nimellä perustila ; korkeamman energian tasoja elektronin voidaan nähdään harmonisten tämän perustaajuus;
- elektronit eivät koskaan sijaitse tarkassa avaruuspisteessä, mutta ne ilmenevät tilavuudessa, jonka todennäköisyys vuorovaikutuksessa heidän kanssaan tietyssä pisteessä määräytyy niiden aaltofunktion avulla .
Matemaattinen ilmaisu
Atomiradat voidaan määritellä tarkemmin kvanttimekaniikan matemaattisen formalismin avulla . Tässä yhteydessä kvanttitilassa elektronin on aalto toiminto Ψ joka täyttää ominaisarvo yhtälö on Hamiltonin H , jota kutsutaan myös "ajasta riippumaton Schrödingerin yhtälön" , tai jopa "yhtälö tiloja. Paikallaan”: H Ψ = E Ψ , missä E on tähän aaltofunktioon liittyvä energia. Elektroninen kokoonpano usean sähköisen atomi on approksimoida lineaarisella yhdistelmä ( konfiguraatio vuorovaikutus , emäkset ) tuotteiden mono-elektronisia toimintoja ( Slater determinantteja ). Spatiaalinen osa näistä mono-elektronisia toimintoja ovat atomiorbitaali, ja huomioon ottaminen spin komponentin määrittelee spinorbitals .
Atomirata on elektronin läsnäolon todennäköisyysamplitudi eristetyn atomin ytimen ympärillä . Tämän todennäköisyyden tiheys riippuu neliön ja moduuli on aallon funktion Ψ . Tämä määritetään Schrödingerin yhtälöllä käyttäen kiertoradan approksimaatiota , johon kuuluu elektronien välisten korrelaatioiden huomiotta jättäminen ja atomin elektronisen konfiguraation laskeminen monoelektronisten aaltofunktioiden tuotteina. Tämä on kuitenkin likimääräinen, koska eri elektronien jakautuminen kiertoradoillaan on oikeastaan korreloiva, kun Lontoon voimat ovat osoitus tästä korrelaatiosta.
Orbitaalilaskenta
Atomiorbitaali voi olla monoelectron orbitaaleja, jotka ovat tarkkoja ratkaisut Schrödingerin yhtälön varten hydrogenoid (eli yhden elektronin) atomi . Ne voivat myös olla perusta laskettaessa aaltofunktioita, jotka kuvaavat atomin tai molekyylin eri elektroneja. Valittu koordinaatisto on yleensä, että on pallokoordinaateissa (r, θ, φ) atomeissa ja suorakulmaisessa koordinaatistossa (x, y, z) on moniatomiseen molekyylejä. Pallomaisten koordinaattien etuna on, että kiertoradan aaltofunktio on kolmen funktion tulo, joista kukin riippuu vain yhdestä kolmesta koordinaatista: ψ (r, θ, φ) = R (r) Θ (θ) Φ (φ) .
Radiaalifunktio R (r) voidaan yleensä mallintaa kolmen yleisesti käytetyn matemaattisen muodon avulla:
- Hydrogenoidiset atomi-orbitaalit ovat peräisin Schrödingerin yhtälön tarkoista ratkaisuista elektroneille ja atomiytimille. Osa toiminto, joka riippuu säteen suuntainen etäisyys on säteittäinen solmut ja laskee pitkin e - r , ollessa vakio.
- Slater-tyyppi orbital ( STO ) on muodoltaan kiertoradan vailla säteen solmujen mutta pienenee pitkin r kuin hydrogenoid kiertoradan.
- Gaussin Orbital ( GTO ) on vailla säteittäinen solmujen ja laskee pitkin e - r 2 .
Hydrogenoid orbitaalien käytetään opetusvälineiksi mutta se on Slater tyyppi orbitaaleja, jotka edullisesti käytetään mallin atomia ja kaksiatomiseksi molekyylejä on digitaalinen kemia . Polyatomiset molekyylit, joissa on kolme tai useampia atomeja, mallinnetaan yleensä käyttämällä Gaussin orbitaaleja, jotka ovat vähemmän tarkkoja kuin Slaterin orbitaalit, mutta joiden yhdistelmä suurina määrinä tekee mahdolliseksi lähestyä hydrogenoidisten orbitaalien tarkkuutta.
Kulmakerroin Θ (θ) Φ (φ) tuottaa funktioita, jotka ovat pallomaisen yliaallon todellisia lineaarisia yhdistelmiä Y m
ℓ(θ, φ) , missä ℓ ja m ovat vastaavasti atsimutaalinen kvanttiluku ja magneettinen kvanttiluku .
Vetyatomin kiertoradat
Orbitaalit lasketaan kompleksilukuina , niin että puhumme monimutkaisista orbitaaleista , mutta useimmiten käytämme valittujen pallomaisten harmonisten lineaarisia yhdistelmiä , jotta kuvitteelliset osat kumoavat toisensa: kiertoradoista tulee siten reaalilukuja , ja puhumme todellisista orbitaaleista .
Monimutkaiset kiertoradat
Kukin atomiorbitaali on määritetty tripletti on kvanttiluvut ( n , ℓ , m ℓ ) ja voi sisältää korkeintaan kaksi elektronia kukin eroavat niiden magneettinen spinkvanttiluku , joka voi olla vain ylös tai alas ; Paulin kieltosääntö itse asiassa estää kaksi elektronia samasta atomi jakavat saman kvanttitilassa :
- pääkvanttiluku n on ei-nolla luonnollinen numero : n ≥ 1 ;
- toissijainen kvantti numero (tai sivukvanttiluku) l: on positiivinen tai nolla kokonaisluku tarkastaa 0 ≤ l: ≤ n - 1 ja liittyvät kvantisointi on impulssimomentti silmäkuopan;
- magneettinen kvanttiluku m l: on täyttävä kokonaisluku - l: ≤ m l: ≤ l: ja liittyy kvantisointi projektio kulma vauhtia annetulle akselille;
- magneettinen kvanttiluku spin m s on yhtä suuri ja -12tai +12jolloin vastaavat elektronit ovat yleisesti symboleilla ↓ ja ↑; se on elektronin luontainen ominaisuus, riippumaton kolmesta muusta kvanttiluvusta.
Pääkvanttiluku n määrittävästä sähköisen kuori , kun sivukvanttiluku ℓ määrittää tyypin sähköisen subshell elektronin. Riippuen siitä, onko ℓ on 0, 1, 2, 3, 4, 5, 6 tai enemmän, tyyppi näiden alikerroksista on merkitty kirjaimilla s , p , d , f , g , h , i , jne.
Alikerroksia itse merkitään yhdistämällä kvanttiluku n kvanttilukua representing edustavaan kirjaimeen ; täten ( n , ℓ ) = (2, 1) vastaavaa alikerrosta merkitään 2p: llä.
Elektroninen kokoonpano atomien on huomattava luettelemalla sähköisen alikerroksista kanssa, kuin eksponentti , elektronien lukumäärä tässä alikerros. Rakenteellisesti alikerrosten lukumäärä elektronista kerrosta kohden on yhtä suuri kuin n , kun taas kiertoradojen lukumäärä elektronista alikerrosta s , p , d , f on 1, 3, 5, 7 jne. Kukin näistä kiertoradoista voi sisältää korkeintaan kaksi elektronia, elektronien enimmäismäärä alikuoren tyyppiä s , p , d , f on 2, 6, 10, 14.
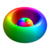
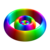
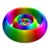
Taulukko ensimmäisen monimutkainen orbitaaleja on vety atomi| Kvanttiluvut | Pohjavilla | Magneettinen kvanttiluku m ℓ | |||||||
|---|---|---|---|---|---|---|---|---|---|
| Main | Azimuthal | -3 | -2 | -1 | 0 | 1 | 2 | 3 | |
| n = 1 | ℓ = 0 | 1 s |

|
||||||
| n = 2 | ℓ = 0 | 2 sekuntia |

|
||||||
| ℓ = 1 | 2 Sivumäärä |

|

|

|
|||||
| n = 3 | ℓ = 0 | 3 sekuntia |

|
||||||
| ℓ = 1 | 3 Sivumäärä |

|

|
|
|||||
| ℓ = 2 | 3 d |

|

|

|

|

|
|||
| n = 4 | ℓ = 0 | 4 sekuntia |

|
||||||
| ℓ = 1 | 4 Sivumäärä |

|

|

|
|||||
| ℓ = 2 | 4 d |

|

|

|

|

|
|||
| ℓ = 3 | 4 f |

|

|

|

|

|

|

|
|
| n = 5 | ℓ = 0 | 5 s |

|
||||||
| ℓ = 1 | 5 Sivumäärä |

|

|

|
|||||
| ℓ = 2 | 5 d |

|

|

|

|
|
|||
| n = 6 | ℓ = 0 | 6 s |

|
||||||
| ℓ = 1 | 6 Sivumäärä |

|

|

|
|||||
| ℓ = 2 | 6 d |
|

|

|

|

|
|||
Yllä esitetyt pintojen värit osoittavat aaltofunktion todellisten ja kuvitteellisten osien merkkiä (nämä värit ovat mielivaltaisia eivätkä heijasta sopimusta):
| Aaltotoiminto | Todellinen osa | Kuvitteellinen osa |
|---|---|---|
| Positiivinen arvo | Sininen | Punainen |
| Negatiivinen arvo | Keltainen | Vihreä |
Nämä laskelmat merkitse valinta etuoikeutettu akselin - esimerkiksi z- akselin sisään suorakulmaisten koordinaattien - ja etuoikeutetun suuntaan tämän akselin: tämä on mitä tekee mahdolliseksi määritellä merkki on magneettinen kvanttiluku m ℓ . Tämä malli on siksi käyttökelpoinen järjestelmissä, jotka jakavat tämän symmetria, kuten tapauksessa Stern ja Gerlach koe , jossa hopea atomit altistetaan pystysuuntaisen epäyhtenäinen magneettikentän .
Todelliset kiertoradat
Kiteisessä kiinteässä aineessa sijaitsevaan atomiin kohdistuu useita etuakseleita, mutta ei etusijaa näillä akseleilla. Näissä olosuhteissa sen sijaan, että rakennettaisiin tällaisen atomin atomiorbitaalit säteittäisistä funktioista ja yhdestä pallomaisesta harmonisesta , käytämme yleensä lineaarisia yhdistelmiä pallomaisista harmonisista, jotka on valittu siten, että niiden kuvitteellinen osa poistuu., Mikä antaa todelliset harmoniset . Juuri näitä todellisia orbitaaleja käytetään yleensä atomien orbitaalien visualisointiin.
Esimerkiksi todellisissa hydrogenoidisissa orbitaaleissa n: llä ja ℓ: llä on sama merkitys kompleksisella vastineellaan , mutta m ℓ ei ole enää kelvollinen kvanttiluku , vaikka sen moduuli onkin. Todellinen vety p orbitaalit , esimerkiksi, annetaan:
missä , ja .
P x- ja p y- orbitaalien yhtälöt riippuvat palloharmonikoille valitusta vaihekäytännöstä. Aikaisemmissa yhtälöissä oletetaan, että pallomaiset yliaallot on määritelty Y: lläm
ℓ(θ, φ) = N e i m φ Pm
ℓ(cosθ) . Kuitenkin joskus vaiheen tekijä (-1) m on mukana , jolla on vaikutus, jolloin p x silmäkuopan vastaavaterosta harmonisten ja p y silmäkuopansummaan harmonisten.
| Kvanttiluvut | Pohjavilla | Moduuli | m ℓ | että magneettinen kvanttiluku | |||||||
|---|---|---|---|---|---|---|---|---|---|
| Main | Azimuthal | 0 | 1 | 2 | 3 | ||||
| n = 1 | ℓ = 0 | 1 s |
 1s |
||||||
| n = 2 | ℓ = 0 | 2 sekuntia |
 2s |
||||||
| ℓ = 1 | 2 Sivumäärä |
 2p z |
 2p x |
 2p y |
|||||
| n = 3 | ℓ = 0 | 3 sekuntia |
 3s |
||||||
| ℓ = 1 | 3 Sivumäärä |
 3p z |
 3p x |
 3p y |
|||||
| ℓ = 2 | 3 d |
 3d z 2 |
 3d xz |
 3d yz |
 3d xy |
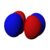 3d x 2 –y 2 |
|||
| n = 4 | ℓ = 0 | 4 sekuntia |
 4s |
||||||
| ℓ = 1 | 4 Sivumäärä |
 4p z |
 4p x |
 4p y |
|||||
| ℓ = 2 | 4 d |
 4d z 2 |
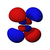 4d xz |
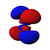 4d yz |
 4d xy |
 4d x 2 –y 2 |
|||
| ℓ = 3 | 4 f |
 4f z 3 |
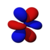 4f xz 2 |
 4f yz 2 |
 4f xyz |
 4f z (x 2 –y 2 ) |
 4f x (x 2 –3y 2 ) |
 4f y (3x 2 –y 2 ) |
|
| n = 5 | ℓ = 0 | 5 s |
 5s |
||||||
| ℓ = 1 | 5 Sivumäärä |
 5p z |
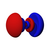 5p x |
 5p y |
|||||
| ℓ = 2 | 5 d |
 5d z 2 |
 5d xz |
 5d yz |
 5d xy |
 5d x 2 –y 2 |
|||
| n = 6 | ℓ = 0 | 6 s |
 6s |
||||||
| ℓ = 1 | 6 Sivumäärä |
 6p z |
 6p x |
 6p y |
|||||
| ℓ = 2 | 6 d |
 6d z 2 |
 6d xz |
 6d yz |
 6d xy |
 6d x 2 –y 2 |
|||
| n = 7 | ℓ = 0 | 7 s |
 7s |
||||||
Yllä olevassa esityksessä väri osoittaa aaltofunktion merkin, joka on positiivinen punaisella ja negatiivinen sinisellä.
Atomiorbitaalien geometria
Orbitaalien graafisten esitysten tarkoituksena on näyttää avaruusalueet, jotka atomirataalisen elektronilla on tietty todennäköisyys miehittää. Nämä mallit eivät voi edustaa koko aluetta, jolla elektroni todennäköisesti sijaitsee, koska elektronin kvanttiominaisuuksien perusteella on todennäköisyys , että nolla ei ole nolla, melkein mistä tahansa elektronin avaruudesta atomin ympärillä. Siksi nämä esitykset koostuvat isopinnoista , joiden todennäköisyystiheys | ψ (r, θ, φ) | 2 on vakio ja jossa elektronin läsnäolon todennäköisyys on yhtä suuri kuin annettu arvo, esimerkiksi 90%. Vaikka | ψ | 2 ei ole koskaan negatiivisia , me yleensä osoittaa merkki on aaltofunktion ψ (r, θ, φ) .
On myös mahdollista esittää funktio ψ ja sen vaihe sen sijaan, että ψ 2 ilmaisee todennäköisyystiheyden, mutta ei vaihetta. Esitykset | ψ (r, θ, φ) | Kuviossa 2 on yleensä vähemmän pallomaisia ja kapeampia lohkoja kuin ψ: n (r, θ, those) lohkoissa , mutta kahdella esityksellä on sama määrä lohkoja samalla alueellisella järjestelyllä ja ne voidaan tunnistaa toisistaan.
Kvanttilukujen tulkinta
Yleisesti ottaen pääkvanttiluku n määrittää kiertoradan koon ja energian tietylle atomituumalle : mitä enemmän n kasvaa, sitä enemmän kiertoradan koko kasvaa. Verrattaessa kuitenkin useiden kemiallisten alkuaineiden orbitaaleja , mitä suurempi atomiluku Z kasvaa, sitä enemmän atomirataita supistuu, koska myös sähkövarauksen kokonaisydin kasvaa Z: n kanssa . Tämän seurauksena atomien koko pysyy suhteellisen vakiona elektronisten kerrosten kertymisestä huolimatta .
Silti yleensä atsimutaalinen kvanttiluku ℓ määrää kiertoradan muodon, kun taas magneettinen kvanttiluku m ℓ määrää sen orientaation avaruudessa. Kuitenkin, määrä m ℓ myös määrittää muodon joitakin monimutkaisia orbitaalien . Annettua paria ( n , ℓ ) vastaava kiertoratajoukko täyttää tilan mahdollisimman symmetrisesti kasvavalla määrällä lohkoja ja solmuja.
S kiertoradat
S- orbitaalit , jotka on identifioitu ℓ = 0 , on esitetty palloilla. Kun n = 1 , todennäköisyystiheys on suurempi keskellä ja pienenee ulospäin, mutta kun n = 2 tai enemmän, todennäköisyystiheys jokaisen s orbitaalin sisällä muodostaa radiaalisen aaltorakenteen, jossa vuorotellen samankeskiset kerrokset, joilla on suuri todennäköisyys ja pienempi todennäköisyys.
S- orbitaalit ovat ainoat, jotka esittävät antisolmun, toisin sanoen alueen, jossa aaltofunktiolla on korkea moduuli, ytimen keskellä. P- , d- , f- ja sitä seuraavilla kiertoradoilla on kulmamomentti ja ne välttävät ydintä, jossa ne muodostavat solmun.
P-, d- ja f-orbitaalit
Kolme p- orbitaalia, kun n = 2, on kahden ellipsoidin muotoinen, jotka jakavat tangenttipisteen ytimen tasolla . Tämä muoto on joskus kutsutaan kuten käsipainot . Ne on suunnattu ortogonaalisesti toisiinsa nähden funktiona niiden magneettinen kvanttiluku m ℓ .
Neljä viidestä d orbitaalien ja n = 3 muodot ovat samanlaiset, joissa jokaisessa on neljä päärynä-muotoinen lohkoa, nämä liuskat ovat kohtisuoraan tangentti kaksittain, keskukset nämä neljä lohkoa ovat samassa tasossa . Kolme näistä orbitaaleista, nimeltään d xy , d yz ja d xz , ovat linjassa xy- , yz- ja xz- tasojen kanssa - lohkot sijaitsevat kunkin kolmen koordinaattiakseliparin välissä - kun taas neljäs, nimeltään d x 2 - y 2 , on linjassa itse x- ja y- akselien kanssa .
Viides kiertorata d , nimeltään d z 2 ja vastaa m ℓ = 0 , muodostetaan kolmesta alueesta, joilla todennäköisyystiheys on suuri: kahdesta päärynän muotoisesta alueesta ytimen molemmin puolin akselia z pitkin ja toruksesta ytimen ympärillä xy- tasossa .
-
Orbitaalinen d xy
-
Kiertorata d yz
-
Orbitaali d xz
-
Kiertorata d x 2 - y 2
-
D z kiertorata 2
On olemassa seitsemän f orbitaalit ja ovat monimutkaisempia muotoja kuin d orbitaalien .
Vetyatomien atomiorbitaalien muoto on johdettu pallomaisista yliaaltoista . Nämä muodot eivät ole ainutlaatuisia, ja monet lineaariset yhdistelmät ovat kelvollisia, kuten muunnos kuutioharmonikoiksi (in) . On myös mahdollista tuottaa funktiosarjoja, jotka tuottavat d orbitaalia, joilla kaikilla on sama muoto, kuten p orbitaaleja .
On pidettävä mielessä, että kaikki nämä orbitaalit, jotka esitetään erikseen osana vetyatomien malleja, esiintyvät samanaikaisesti todellisissa atomeissa.
Analogia kalvon värähtelyn kanssa
On mahdollista esittää kahdessa ulottuvuudessa atomirataalien erilaisten kolmiulotteisten muotojen merkitys pyöreän kalvon, esimerkiksi rummun ihon, värähtelymoodien avulla . Tässä esityksessä etäisyys keskustasta kalvon vastaa etäisyyttä elektronin välillä atomin ydin , ja suuruus poikkeama tasapainosta kalvon tasossa edustaa tiheys läsnäolo elektroni. Atomissa . Tämä analogia ei ole täydellinen etenkään siksi, että fyysisen kalvon kuten rummun ihon jännitys pyöristää sen läpi kulkevat aallot, mutta sillä on useita atomirataalien laadullisia ominaisuuksia, esimerkiksi se, että vain s- orbitaaleilla on keskellä antisolmu (suurin amplitudi), kun taas kaikilla muilla on solmu (nollamplitudi) tässä paikassa tai Student-tason orbitaalien lohkojen geometrisen jakauman visualisoimiseksi:
- Ensimmäiset 9 rummun ihon värähtelytapaa
-
Tila u 01 , samanlainen kuin 1s
-
Tila u 02 , analoginen 2 sekunnin kanssa
-
Tila u 03 , samanlainen kuin 3s
-
Tila u 11 , analoginen 2p: n kanssa
-
Tila u 12 , analoginen 3p: n kanssa
-
Tila u 13 , analoginen 4p: n kanssa
-
U 21 -tila , analoginen 3d: n kanssa
-
Tila u 22 , analoginen 4d: n kanssa
-
Tila u 23 , analoginen 5d: n kanssa
Todellinen osa on aaltofunktio n ja p atomiorbitaali edustaa samalla tavoin eri arvoilla n ja ainsi on siten analoginen eri värähtelymoodia rumpukalvon:
- Reaaliosa n aaltofunktio s ja p orbitaalien
-
1s kiertorata
-
2s kiertorata
-
kiertorata 3s
-
2p kiertorata
-
kiertorata 3p
-
kiertorata 4p
Sovellukset
In atomifysiikan , spektriviivat vastaavat elektroniset siirtymät johtuvat siirtyminen yhdestä kvanttitilan on atomin toiseen. Nämä tilat määrittelee kvanttilukujen joukko, joka yleensä liittyy elektroniseen kokoonpanoon , toisin sanoen elektronien jakautumiseen eri atomirataalien välillä. Näin ollen elektroninen kokoonpano neon on perustilassa on 1s 2 2s 2 2p 6 , yhteenveto termi1S
0.
Atomiorbitaali ovat keskeinen käsite visualisointiin heräte prosessit on peräisin elektronien siirtymisestä . Esimerkiksi, on mahdollista yhdistää tietyn siirtymisen magnetointi elektronin kulkee varatun orbitaali pääkvanttiluku n = n 1 on vapaana kiertoradalla kvantti lukumäärä n = n 2 . Siten energia elektronin on vety atomi on yhtä suuri kuin:
,voimme päätellä Rydbergin kaava antaa aalto numero liittyvät sähköiseen siirtymistä koskevat n = n 1 kiertoradan kohteena on n = n 2 silmäkuopan on hydrogenoid atomi, jossa λ on aallonpituus , R ∞ Rydberg vakio , ja Z eff tehokas ydinpanos (in) :
Sovelletaan vety , kaavan käytetään laskettaessa emissiolinjat n spektrin vety :
On kuitenkin pidettävä mielessä, että orbitaalit Näin määritellyt monoelectronic aalto liittyvät toiminnot vety atomia . Koska atomit eivät yleensä ole hydrogeenisia, ne ovat päinvastoin polyelektronisia, joten tämä likiarvo on tapa yksinkertaistaa atomien elektronisen konfiguraation mallintamista, mutta sillä voi olla rajoituksia erityisesti suurten atomien kuvaamiseen.
Huomautuksia ja viitteitä
- (in) David Griffiths, Introduction to Quantum Mechanics , 1995, Prentice Hall, s. 190–191 . ( ISBN 0-13-124405-1 )
- (en) Ira Levine, (2000). Quantum Chemistry , 5 th painos, 2000, Prentice Hall, s. 144–145 . ( ISBN 0-13-685512-1 )
- (in) Keith J. Laidler, John H. Meiser, Physical Chemistry , 1982, Benjamin / Cummings, s. 488 . ( ISBN 0-8053-5682-7 )
- (in) Peter Atkins, Julio de Paula, Ronald Friedman, Quanta, Matter and Change: molekyyligrafiikkapakka- lähestymistapa Physical Chemistry , 2009, Oxford University Press, s. 106 . ( ISBN 978-0-19-920606-3 )
- Roger Penrose , Universumin lakien löytäminen: matematiikan ja fysiikan ihana historia , 2004.
- (in) Ira Levin, Kvanttikemian , 7 th edition, Pearson Education, 2014, s. 141–142 . ( ISBN 0-321-80345-0 )
- (in) Miguel A. Blanco, herra Flórez ja herra Bermejon , " Evaluation of pyörimisen matriisien perusteella todellinen palloharmonisten " , Journal of Molecular Structure: Theochem , vol. 419, n luut 1-3, 8. joulukuuta 1997, s. 19-27 ( DOI 10.1016 / S0166-1280 (97) 00185-1 , lue verkossa )
- (in) Albert Messias, Kvanttimekaniikka: kaksi tilavuutta sidottu yhdeksi , 1999 Mineola, Dover, New York. ( ISBN 978-0-486-40924-5 )
- Claude Cohen-Tannoudji, Bernard Dui, Franck Laloë, kvanttimekaniikka , tiedekasvatuskokoelma , Herman, Pariisi, 1973. Raamatun koodi : 1973viitekirja ..... C
- (in) Richard E. Powell , " Viisi d orbitaalit vastaavaa " , Journal of Chemical Education , vol. 45, n o 1, Tammikuu 1968, s. 45 ( DOI 10,1021 / ed045p45 , Bibcode 1968JChEd..45 ... 45P , lukea verkossa )
- (in) George E. Kimball , " Ohjaus Valencia " , The Journal of Chemical Physics , vol. 8, n o 2 Helmikuu 1940, s. 188-198 ( DOI 10,1063 / 1,1750628 , Bibcode 1940JChPh ... 8..188K , lukea verkossa )
Katso myös
Aiheeseen liittyvät artikkelit
- Schrödingerin malli
- Vetyatomi
- Pallomainen harmoninen
- Molekyylinen kiertorata
Ulkoinen linkki
- Atomiorbitaaleihin ja kvantifiointiin liittyvä toiminta, sovellukset ja tutkimus (Paris Sud University)







