Typpihappo
| Typpihappo | |
 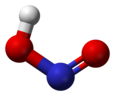  Rakenne cis ja trans- typpihapoke . |
|
| Henkilöllisyystodistus | |
|---|---|
| IUPAC-nimi |
typpihappo vetynitriitti |
| N o CAS | |
| N o ECHA | 100,029,057 |
| N O EY | 231-963-7 |
| PubChem | 24529 |
| ChEBI | 25567 |
| Hymyilee |
N (= O) O , |
| InChI |
InChI: InChI = 1S / HNO2 / c2-1-3 / h (H, 2,3) InChIKey: IOVCWXUNBOPUCH-UHFFFAOYSA-N |
| Ulkomuoto | vaaleansininen liuos |
| Kemialliset ominaisuudet | |
| Kaava |
H N O 2 [isomeerit] |
| Moolimassa | 47,0134 ± 0,0009 g / mol H 2,14%, N 29,79%, O 68,06%, |
| pKa | 3,35 25 ° C: ssa |
| Dipolaarinen hetki |
1,423 ± 0,005 D ( cis ) 1,855 ± 0,016 D ( trans ) |
| Sähköiset ominaisuudet | |
| 1 re ionisaatioenergia | ≤ 11,3 eV (kaasu) |
| SI- ja STP- yksiköt, ellei toisin mainita. | |
Typpihapoke on kemiallinen yhdiste on kaavan HNO 2. Se on heikko monohappo , jonka tiedämme vain liuoksessa, joka ei ole liian hapan (se on suhteeton matalassa pH: ssa) ja kaasufaasissa. Sen suolat ( nitriitit ) ovat stabiileja vesiliuoksessa. Typpihappo on yksi välttämättömiä reagensseja atsoväriaineiden valmistuksessa. Sitten se valmistetaan in situ hapottamalla natriumnitriittiä alhaisessa lämpötilassa (noin 5 ° C: ssa).
HNO 2 -molekyylinhavaittiin tähtienvälisessä väliaineessa binaarijärjestelmän IRAS 16293-2422 (en) B-komponentissa .
Kuvaus
Sen systemaattinen nimi on: dioksonihappo (III) tai typpihappo III . Sen suoloja kutsutaan nitriiteiksi .
Se on erityisen epävakaa ja hajoaa huoneenlämpötilassa typpimonoksidiksi NO ja nitraatti- ioniksi [NO 3 ] -Ja näyttää Frost kaavio on typen alla:

Typpi, joka on + III- hapetustilassa , löytyy suhteettomuuden jälkeen + V- ja + II-tiloissa.
Typpihappoa käytetään atsojohdannaisten ( atsobentseeni C 6 H 5 – N = N - C 6 H 5) valmistamiseen.) Peräisin aromaattisista amiineista , kautta diatsoniumsuolat C 6 H 5 N + ≡N · X -.
Hänen pK a on 3,3.
Se on valmistettu ex tempore, koska se on liian epävakaita varastoitaviksi lisäämällä suolahappoa ja natriumnitriittiä liuoksena:
NO 2 - (vesiliuos)+ H 3 O +→ HNO 2 (vesiliuos)+ H 2 O (neste).Katso myös
Huomautuksia ja viitteitä
- (in) David R. LiDE, Handbook of Chemistry and Physics , CRC,16. kesäkuuta 2008, 89 th ed. , 2736 Sivumäärä ( ISBN 142006679X ja 978-1420066791 ) , s. 9-50
- laskettu molekyylimassa välillä " Atomic painot Elements 2007 " on www.chem.qmul.ac.uk .
- (in) David R. LiDE, Handbook of Chemistry and Physics , CRC,2008, 89 th ed. , 2736 Sivumäärä ( ISBN 978-1-4200-6679-1 ) , s. 10-205
- (in) A. Coutens, NFW Ligterink, BC Loison, V. Wakelam, H. Calcutt, MN Drozdovskaya JK Jørgensen, HSP Muller, EF van Dishoeck ja SF Wampfler , " ALMA PILS kysely: ensimmäisen havaitseminen typpihapokkeen (HONO ) tähtienvälisessä väliaineessa ” , Astronomy & Astrophysics , voi. 623, maaliskuu 2019, Artikkeli n o L13 ( DOI 10,1051 / 0004-6361 / 201935040 , Bibcode 2019A & A ... 623L..13C , arXiv +1903,03378 , lukea verkossa )