Kysteiini
| Kysteiini | |
 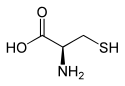 L tai R (+) - kysteiini ja D tai S (-) - kysteiini |
|
| Henkilöllisyystodistus | |
|---|---|
| IUPAC-nimi | 2-amino-3-merkapto-propaanihappo |
| Synonyymit |
C, Cys |
| N o CAS |
(raseeminen) L taiR(+) D taiS(-) |
| N o ECHA | 100 000 145 |
| N O EY | 200-158-2 L 213-062-0 D |
| N o E | E920 L |
| FEMA | 3263 L |
| Kemialliset ominaisuudet | |
| Kaava |
C 3 H 7 N O 2 S [Isomeerit] |
| Moolimassa | 121,158 ± 0,009 g / mol C 29,74%, H 5,82%, N 11,56%, O 26,41%, S 26,47%, |
| pKa | 1,91 8,14 10,28 |
| Fyysiset ominaisuudet | |
| T ° fuusio | 240 ° C |
| Liukoisuus | 280 g · L -1 vedessä ( 25 ° C ) |
| Biokemialliset ominaisuudet | |
| Codons | UGU , UGC |
| isoelektrinen pH | 5.07 |
| Välttämätön aminohappo | Tapaus mukaan |
| Esiintyminen selkärankaisilla | 3,3% |
| Varotoimenpiteet | |
| WHMIS | |
|
Hallitsematon tuoteTätä tuotetta ei valvota WHMIS-luokituskriteerien mukaan. |
|
| Direktiivi 67/548 / ETY | |
 Xn Symbolit : Xn : Haitallista R-lausekkeet : R22 : Haitallista nieltynä. R-lausekkeet : 22, |
|
| SI- ja STP- yksiköt, ellei toisin mainita. | |
Kysteiini (Lyhenteet IUPAC - IUBMB : Cys ja C ) sekä vanha Kreikka κύστις ( " rakko ") on hapan α-aminohappo , jonka enantiomeeri L on yksi 22 proteinogeenisiä aminohapot , koodaa on lähetti-RNA , jonka UGU ja UGC kodonit . Sitä ei pidetä olennaisia varten ihmiselle , mutta voidaan tuotetaan riittäviä määriä kehon riippuen terveydentilasta yksilöiden - etenkin, kun on kyse tiettyjen aineenvaihdunnan sairauksiin ja imeytymishäiriö - sekä potilaille. Lapsille ja vanhuksille.
Se on luonnollinen a-aminohappo, jolle on tunnusomaista tioli muodostavan sulfhydryyli- SH- ryhmän läsnäolo ; selenokysteiini ja tellurocystéine ovat kuten joiden atomi rikki on korvattu vastaavasti atomilla seleenin ja telluurin .
Kysteiiniä on läsnä pieninä määrinä useimmissa proteiineissa . Sen läsnäolo proteiineissa on erittäin tärkeää erityisesti siksi, että se sallii disulfidisiltojen muodostumisen . Tioliryhmä on hyvin herkkä, koska se hapettuu helposti. Sen hapettuminen johtaa kystiiniin , joka koostuu kahdesta kysteiinimolekyylistä, jotka on liitetty disulfidisillalla. Vahvempi hapetin voi hapettaa kysteiini sen rikki, jolloin saatiin kysteiinihappo HO 3 S - CH 2 -CH (NH 2 ) COOH, tauriinin , sappeen läsnä olevan dekarboksylointituotteen taurokolaatin muodossa .
Tiolien "suojaamiseksi" kysteiiniltä tai disulfidisiltojen vähentämiseksi käytetään erilaisia reaktioita, erityisesti:
- Vapaiden tiolien suuri ylimäärä:
- R-SH-tyyppisten monotiolien avulla. Yleisimmin käytetty on 2-merkaptoetanolia : HS H 2 C - CH 2 OH,
- syklisoitavilla ditioleilla, esimerkiksi ditiotreitolilla : HS H 2 C - CHOH - CHOH - CH 2 SH ;
- Vapaiden tiolien alkylointi .
Alkyloinnin estoa käytetään yleisesti proteiineja tutkittaessa. Siinä käytetään erityisesti jodiasetamidia, joka johtaa karboksiamidometylaatioon:
Cys - SH + IH 2 C - CONH 2→ Cys - S - CH 2 -CONH 2.Kysteiini voidaan ottaa ravintolisänä N- asetyylikysteiinin (NAC) muodossa.
Hänellä oli tärkeä rooli maan elämän kehityksessä.
Sovellus
Kysteiini on hyväksytty elintarvikelisäaineeksi ja sillä on numero E920 .
Tuotanto
L -cysteic hapon ja L -kysteiini- voidaan valmistaa teollisessa mittakaavassa tietyistä GMO: , erityisesti Escherichia coli päässä glukoosista ja mineraalisuoloja , mistä höyhenet liuotettiin suolahappoon samoin kuin ihmisen hiukset , jotka sisältävät enemmän. Tämä viimeinen tuotantotapa kiellettiin Ranskassa Ranskan julkisen hygienian ylemmän neuvoston lausunnossa 8. kesäkuuta 1999 päivätyllä lausunnolla "ottaen huomioon ihmisruokaa käsittelevän tiedekomitean yleisen suosituksen vastustaa sisäistä kierrätystä. tätä päätöstä on kuitenkin vaikea soveltaa, koska jakautuneen kysteiinin alkuperää ei voida helposti määrittää.
Euroopan elintarviketurvallisuusviranomainen (EFSA) on valtuuttanut, jota direktiivinlokakuu 2010, L- kysteiinin käyttö pikkulasten ja pikkulasten kekseissä tukehtumisen estämiseksi vähärasvaisten rasvojen pirstoutumisella . Yleisemmin kysteiini sallii pastan pidättää paremmin kaasua ja säilyttää suuret muodot pitkällä aikavälillä, mikä edistää näiden tuotteiden virtausta leivonnaisiin .
Ruoat, jotka ovat kysteiinin lähteitä
- Hiiva
- Vehnänalkio
- Valkosipuli
- Sipuli
- Ruusukaali
- Hamppu
- Parsakaali
- Maitotuotteet
- Pähkinät
- Siemenet
- Fonio
- Meren antimia
- Kalastaa
- Munat
- Liha
Toiminta ihmiskehossa
Kysteiini on mukana melaniinin , ihon ja hiusten luonnollisen pigmentin, synteesissä .
Se osallistuu myös koentsyymin A synteesiin, jolla on tärkeä rooli ihmisen aineenvaihdunnassa.
Ja koska sen jäämät korjata metalli- kationeista , se näyttää olevan osallisena tiettyjen prosessien saastumisen , biokertymisen , ja luonnollinen vieroitus rungon ( kelatoituminen on raskasmetallien tai myrkyllisiä metalloidien ).
Huomautuksia ja viitteitä
- laskettu molekyylimassa välillä " Atomic painot Elements 2007 " on www.chem.qmul.ac.uk .
- (in) Francis A. Carey, " taulukossa pK ja pH-arvot " , on kemian laitoksen ja University of Calgary , 2014(käytetty 26. heinäkuuta 2015 )
- (in) Mr. Beals, L. Gross, S. Harrell, " aminohappo Frequency " on Institute for Environmental Modelling (ITSH) on Tennesseen yliopistossa (näytetty 26 heinäkuu 2015 )
- " kysteiini (L-) " tietokannassa kemikaalien Reptox että CSST (Quebec organisaatio, joka vastaa työsuojelun), pääsee 25 huhtikuu 2009
- Tiivistelmä kreikan-ranskan sanakirjasta A. Bailly, s. 520 .
- Georges Dolisin lääketieteellinen terminologia
- (sisään) Yannick Vallee , Ibrahim Shalayel , Dung Kieu- Ly ja K. Raghavendra Rao , " At Very Beginning of Life on Earth: the thiol-rich peptide (TRP) world hypothesis " , International Journal of Developmental Biology , voi. 61, n luu 8-9,8. marraskuuta 2017( ISSN 0214-6282 ja 1696-3547 , luettu verkossa , kuultu 16. huhtikuuta 2018 )
- Kysteiini GMO Compass -sivustolla.
- http://www.economie.gouv.fr/files/files/directions_services/dgccrf/boccrf/00_01/a0010016.htm Ranskan korkeamman julkisen hygienian neuvoston lausunto L-kysteiinin käytön lupahakemuksesta hiuksista ihmisravinnossa].
- Komission direktiivi 2010/69 / EU, annettu 22 päivänä lokakuuta 2010, muista elintarvikelisäaineista kuin väreistä ja makeutusaineista annetun Euroopan parlamentin ja neuvoston direktiivin 95/2 / EY liitteiden muuttamisesta .
- HMCOF SEABIRDS " Merilintujen ja pyöriäisten raskasmetallikontaminaatio Pohjanmerellä ;" Liègen kuninkaallisen tiedeliiton tiedote 61 (1992): 163.)
- MOENNE, Alejandra. "Eukaryoottiset metallotioneiinit: proteiinit, geenien säätely ja kuparin homeostaasi." Meribiologian muistikirjat 42.1-2 (2001): 125-135.
Katso myös
Aiheeseen liittyvät artikkelit
Ulkoiset linkit
- (en) http://www.chemie.fu-berlin.de/chemistry/bio/aminoacid/cystein_en.html
- (ei) kysteiinin hydrofobinen luonne.
- Pilottitutkimus kysteiinipitoisen proteiini-isolaatin (Immunocal) nauttimisen siedettävyydestä autistisilla ihmisillä
Bibliografia
- Brattström, L. et ai. " Homokysteiini ja kysteiini: plasmapitoisuuden tekijät keski - ikäisillä ja vanhuksilla ." Journal of internal medicine 236.6 (1994): 633-641 ( tiivistelmä ).
- Quig, David. "Kysteiinin metabolia ja metallimyrkyllisyys." Vaihtoehtoisen lääketieteen katsaus 3 (1998): 262-270.
- Rhee, Sue Goo et ai. "Vetyperoksidi: avainlähetin, joka moduloi proteiinin fosforylaatiota kysteiinin hapettumisen kautta." Science Signaling 2000.53 (2000): pe1-pe1 ( tiivistelmä ).
- Turk, Vito ja Wolfram Bode. " Kystatiinit: kysteiiniproteinaasien proteiini-inhibiittorit ." FEBS-kirjeet 285.2 (1991): 213-219.
- Turk, Vito, Boris Turk ja Dušan Turk. "Lysosomaaliset kysteiiniproteaasit: tosiasiat ja mahdollisuudet." EMBO-lehti 20.17 (2001): 4629-4633 ( tiivistelmä ).
- Van Wart, Harold E. ja Henning Birkedal-Hansen. " Kysteiinikytkin: metalloproteinaasiaktiivisuuden säätelyn periaate, jota voidaan soveltaa koko matriisimetalloproteinaasigeeniperheeseen. " Proceedings of the National Academy of Sciences 87.14 (1990): 5578-5582 abstrakti .