Karboksyylihappo
Termi karboksyylihappo viittaa molekyyliin, joka käsittää karboksyyliryhmän (–C (O) OH). Ne ovat happoja ja niiden konjugoituja emäksiä kutsutaan karboksylaatti-ioneiksi .
On orgaaninen kemia , joka on karboksyyliryhmä on funktionaalinen ryhmä, joka koostuu atomi on hiili , sitoo kaksoissidos atomiin hapen ja sitoo yksinkertainen sidos ryhmään hydroksyyli -OH.
Kenraali
On kemia , karboksyylihapot R-COOH ovat kanssa sulfonihappojen R-SO 3 H kahdenlaisia happojen ja orgaanisen kemian . Niitä esiintyy luonnossa runsaasti rasvahappona ( lipideinä ) ja ne ovat erittäin tärkeitä teollisessa kemiassa . Esimerkiksi etikkahappo ei ole vain tärkeä rakennuspalikka biologiassa esiintyville monimutkaisille molekyyleille , vaan se on myös teollisesti valmistettu etikka . Yksi tunnetuimmista on asetyylisalisyylihappo tai aspiriini. Proteiinien rakennusosa , aminohapot ovat karboksyylihappoja.
Tyypillinen funktionaalinen ryhmä on karboksyyliryhmä, jossa R on vety tai orgaaninen ryhmä:

Karboksyylihapot on raakaa kaava C n H 2 N O 2 , kun R on alkyyli ryhmä . Laskemalla määrä tyydyttymättömyyttä antaa: . Tämä tyydyttymättömyys heijastaa hiili-happi- kaksoissidosta .
Karboksyyliryhmät kirjoitetaan usein pelkistetyssä muodossa: -COOH (ryhmän ionisoimaton muoto). Ryhmän ionisoitu muoto on: -COO - .
Tämä sijaitsee aina hiiliketjun päässä . Lisäksi on karboksyyliryhmän ryhmän kohteena on orgaaninen yhdiste on karboksylaatio , poistaminen tämän saman ryhmän on dekarboksylaation .
Karboksylaatti-ionit
Nämä ovat konjugaatin emäkset R-COO - karboksyylihapot. Nämä emäkset ovat yleensä melko heikkoja . Molekyylin negatiivinen varaus delokalisoituu karboksyyliryhmän kahteen happiatomiin mesomerismillä, mikä selittää tämän tyyppisten molekyylien suhteellisen stabiilisuuden.

Karboksylaatti-ioni on amfifiilistä pinta-aktiivista ainetta , se on pesuaine laji ja saippua . Itse asiassa _COO-karboksylaattiryhmä on hydrofiilinen, koska se on hyvin polaarinen . Toisaalta hiiliketju R on apolaarinen ja siksi hydrofobinen ja lipofiilinen .
Nimikkeistö
- Systemaattinen: jos karboksyyliryhmän COOH hiiliatomi sisältyy vastaavan hiilivedyn pääketjuun (jossa on sama määrä hiiliatomeja, CH 3: lla COOH: n sijasta), seuraa tämän nimeä. Hiilivety loppuliitteellä " -oic "(dihappo dihapolle), ja edeltää sitä sanalla" happo ". Muussa tapauksessa (esimerkiksi syklisissä sarjoissa) sanan " happo " jälkeen seuraa hiilivedyn nimi, johon lisätään loppuliite "-karboksyylihappo".
| Luokka | Kaavan * on tunnusomainen ryhmä |
Liite |
|---|---|---|
| Karboksyylihapot | - (C) OOH- COOH |
happo-… öljyhappo… -karboksyylihappo |
- heptaanihappo CH 3 (CH 2 ) 5 -COOH, voidaan vaihtoehtoisesti nimetty heksaani-1-karboksyylihappo, jos hiiliatomi -COOH ei sisälly ketjun numerointi;
- HOOC- (CH 2 ) 5 -COOH heptaanidihappo on dikarboksyylihappo . Jälkiliite -oic edeltää multiplikatiivisessa etuliite di- ;
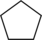
- syklopentaanikarboksyylihappo: -COOH .
- Tavallinen: kuten monilla orgaanisilla yhdisteillä, karboksyylihapoilla on yleisiä nimiä, joita käytetään usein kirjallisuudessa ja jotka muistuttavat lähteen, josta ne ensin eristettiin. IUPAC: n määrittelemä luettelo säätelee kuitenkin systemaattisten nimien rinnalla hyväksyttyjen triviaalien nimien käyttöä.
| Tyyppi | Rakenne | IUPAC-nimi | yleinen nimi | Lähde |
|---|---|---|---|---|
| Alifaattiset yksihapot | H-COOH | metaanihappo | muurahaishappo | erittävät muurahaiset (latinaksi: formica , muurahaiset) |
| CH 3 COOH | etaanihappo | etikkahappo | Latinalainen: acetum , etikka | |
| CH 3 CH 2 -COOH | propaanihappo | propionihappo | Kreikka: sotilas , rasva | |
| CH 3 (CH 2 ) 2 -COOH | butaanihappo | voihappo | Kreikka: bouturos , voi | |
| CH 3 (CH 2 ) 3 -COOH | pentaanihappo | valeriinihappo | valerian | |
| CH 3 (CH 2 ) 4 -COOH | heksaanihappo | kapronihappo | ||
| CH 3 (CH 2 ) 5 -COOH | heptaanihappo | enantihappo | ||
| CH 3 (CH 2 ) 6 -COOH | oktaanihappo | kapryylihappo | kookospähkinä , äidinmaito | |
| CH 3 (CH 2 ) 7 -COOH | nonaanihappo | pelargonihappo | ||
| CH 3 (CH 2 ) 8 -COOH | dekaanihappo | kapriinihappo | ||
| CH 3 (CH 2 ) 9 -COOH | undekaanihappo | undekyylihappo | ||
| CH 3 (CH 2 ) 10 -COOH | dodekaanihappo | lauriinihappo | kookosöljy | |
| CH 3 (CH 2 ) 11 -COOH | tridekaanihappo | tridekyylihappo | ||
| CH 3 (CH 2 ) 12 -COOH | tetradekaanihappo | myristiinihappo | muskottipähkinä | |
| CH 3 (CH 2 ) 13 -COOH | pentadekaanihappo | pentadekyylihappo | ||
| CH 3 (CH 2 ) 14 -COOH | heksadekaanihappo | palmitiinihappo | palmuöljy | |
| CH 3 (CH 2 ) 15 -COOH | heptadekaanihappo | margariinihappo | ||
| CH 3 (CH 2 ) 16 -COOH | oktodekaanihappo | steariinihappo | eläinrasvat | |
| CH 3 (CH 2 ) 17 -COOH | nonadekaanihappo | nonadekyylihappo | ||
| CH 3 (CH 2 ) 18 -COOH | eikosaanihappo | arakidihappo | öljy maapähkinä , kalaöljyt ja kasviöljyt | |
| CH 3 (CH 2 ) 20 -COOH | dokosaanihappo | beheenihappo | ||
| Aromaattiset yksihapot | C 6 H 5 -COOH | bentsoehappo | bentseeni | |
| HO-C 6 H 4 -COOH | 2-hydroksibentsoehappo | salisyylihappo | hedelmät ( metyylisalisylaattina ) | |
| Tiolihapot | CH 3 CH (SH) -COOH | 2-merkaptopropaanihappo | tiomaitohappo |
Huom: muistisääntö laite muistaa nimet lineaarisen happojen, nousevassa järjestyksessä hiiliatomien lukumäärä, on seuraava virke: " O n M Angel S aucisse G rillée P voideltu" ( O xalique, M alonique, S uccinic , G- lutarinen, A- dipinen, P- imeelinen). Dihappoja käytetään polyamidien ja polyesterien synteesissä .
Muun tyyppisiä karboksyylihapot voidaan mainita: dikarboksyylihappoja , trikarboksyylihapoista , happojen alfa -hydroxylés , ketohapot , aminohapot ja rasvahapot .
Fysikaaliset ja rakenteelliset ominaisuudet
osavaltio
Karboksyylihapot ovat nestemäisiä normaaleissa olosuhteissa, kunhan niiden hiiliketjussa on alle kahdeksan hiiliatomia. Ne ovat vankkoja sen lisäksi.
Pienimolekyylipainoisilla hapoilla on voimakas haju; esimerkiksi butaanihappo on vastuussa hankaavan voin hajusta.
Napaisuus, liukoisuus
Karboksyylihappofunktio on erittäin polaarinen ja on sekä vetysidosten luovuttaja että vastaanottaja . Tämä mahdollistaa vetysidosten muodostumisen esimerkiksi polaarisen liuottimen , kuten veden, alkoholin ja muiden karboksyylihappojen kanssa.

Tämän ominaisuuden ansiosta pienet karboksyylihapot (butaanihappoon asti) ovat täysin vesiliukoisia. Happomolekyylit pystyvät myös muodostamaan stabiileja dimeerejä vetysidoksella, mikä selittää, miksi niiden kiehumispiste on korkeampi kuin vastaavien alkoholien.
Happamuus
Vesiliuoksessa happo hajoaa osittain karboksylaatti-ioniksi tasapainoyhtälön mukaan :
Nämä ovat heikkoja happoja veteen ( s K välillä 4 ja 5).
Kuten alkoholit, karboksyylihapoilla on happama ja emäksinen luonne: deprotonointi karboksylaatti-ioneiksi on helppoa, mutta protonointi on vaikeampaa. Ne on siis pienempi s K kuin alkoholeja. Itse asiassa karboksyylihappojen happamuus selittyy karboksyyliryhmän induktiivisella vaikutuksella : C = O-sidos on hyvin polarisoitunut ( hapen elektronegatiivisuus suurempi kuin hiilen), mikä tekee hiilestä elektrofiilisen. , Ja siksi se houkuttelee elektroneja muuta happea. Nyt tämä toinen happi on itsessään sidoksissa vetyyn, ja tämä sidos on myös polarisoitunut , joten vedyn elektroni, joka on lähestynyt happea, puolestaan houkuttelee elektrofiilistä hiiltä. Tästä vedystä tulee siis erittäin helposti liikkuvaa, joten karboksyyliryhmän happamuus.
Karboksyylihapon liukoisuus kasvaa pH: n mukana .
Spektroskopia
Infrapuna (IR) -karboksyylihapolla on kaksi valenssikaistaa:
| Tärinä | C = O | VAI NIIN |
|---|---|---|
| Aaltoluku (cm −1 ) | 1 680 - 1 710 | 2 500-3 200 |
| Intensiteetti | (vahva) | suuri, keskisuuri tai vahva |
Rakenne

Mukaan vsepr-teoria :
- hiiliatomin (sidosten) ympärillä oleva geometria on trigonaalista tyyppiä;
- karbonyylifunktion (kaksoissidos + vapaat dubletit) ympärillä oleva geometria on myös trigonaalista tyyppiä;
- geometria noin happiatomi funktionaalinen hydroksyyliryhmä (joukkovelkakirjat + vapaa dubletti) on sitä tetraedrisen tyypin (AXE 2 E 2 ).
Karboksyylihapolla on useita mesomeerisiä muotoja .
Reaktiivisuus
Kuten muun muassa on esitetty, karboksyylihapon eri mesomeeriset kaavat:
- happiatomit ovat nukleofiilisiä kohtia samoin kuin Lewisin emäkset;
- keskeinen hiili on elektrofiilinen;
- elektrofiilinen vetyatomi on hapan.
Johdannaiset
Karboksyylihapoilla on monia johdannaisia:
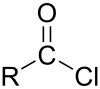
-
Happoanhydridi
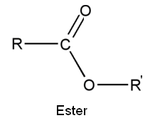

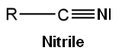
Ryhmän (nukleofugen) poistumisen kannalta helppousjärjestys on:
Cl - (asyylikloridin), RCOO - (anhydridi), RO - (esteri), - NH 2 ja - NR 1 R 2 (amidit).
Vähennys
Hapetus
- Hiilidioksidi (CO 2)
Synteesi
Synteesi hapettamalla
alkoholit tai aldehydit Karboksyylihappoja voidaan saada hapettamalla aldehydit , täten itse asiassa kaksoishapettamalla primääriset alkoholit .of alkeenien esimerkki: etikkahapon synteesi hapettamalla propeenia
Synteesi happojohdannaisesta
Se on yksinkertaisesti erilaisten happojohdannaisten hydrolyysit.
esteri- hydrolyysi happamassa ympäristössä: uudelleenesteröinti
- hydrolyysi emäksisessä väliaineessa: esterin saippuoituminen
Synteesi reagoimalla Grignard-reagenssilla hiilidioksidilla
ReaktioSynteesi tapahtuu matalassa lämpötilassa ( −40 ° C ). Hiilidioksidi on sitten kiinteässä muodossa, nimeltään kuivajää . Se laitetaan liikaa. Reaktion jälkeen hydrolyysi suoritetaan happamassa väliaineessa karboksyylihapon saamiseksi.
MekanismiEnsimmäinen vaihe : Grignard-reagenssin lisääminen CO 2: een

Toinen vaihe : hydrolyysi happamassa väliaineessa
Maloninen synteesi
Malonisynteesi on joukko reaktioita, jotka mahdollistavat monien primaaristen tai sekundaaristen karboksyylihappojen synteesin dietyylimalonaatista .
Hän koostuu:
- happo-emäs-reaktio dietyylimalonaatin ja etanoaatin ( natrium , kalium jne. ) välillä;
- nukleofiilinen substituutio , jossa haluttu ryhmä (ensisijainen tai toissijainen) Lisätään Lopullisessa karboksyylihappo;
- kaksinkertainen saippuointi kahden esterin toimintojen substituoitua dietyylimalonaatti, minkä jälkeen tehdään happamaksi väliaineen;
- dekarboksylointi ( hiilidioksidin vapautuminen kuumennettaessa);
- lopputuotteen uudelleenjärjestely karboksyylihapoksi tautomerismin avulla .
Tämä synteesi on sitäkin mielenkiintoisempi a priori , se mahdollistaa minkä tahansa karboksyylihapon syntetisoinnin, koska tertiäärisen ryhmän lisäksi näyttää siltä, että voimme laittaa mitä haluamme R : n tilalle .
Huomautuksia ja viitteitä
- R. Panico ja J.-C. Richer, IUPAC- nimikkeistön orgaanisia yhdisteitä , Masson, 1994, s. 70, 118- ( ISBN 978-2-225-84479-9 ) . Jäsentäryhmä (ja etuliitteet), jota käytetään kuvaamaan joitain korvaavan nimikkeistön tärkeitä ominaisuusryhmiä, on saatavana IUPAC- viitteestä verkossa (englanniksi): pääte- ja etuliitteet pääominaisuudelle Jotkut ryhmät korvaavassa nimikkeistössä .
- Robert Panico, Jean-Claude Richer ja Jean Rigaudy , orgaanisen kemian nimikkeistö ja terminologia - toiminnalliset luokat. Stereokemia , tekniikatekniikat , 1996, s. 20 ( ISBN 2 85 059-001-0 ) .
- http://www.acdlabs.com/iupac/nomenclature/93/r93_705.htm











