Hydratsiini
| Hydratsiini | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 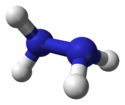 Hydratsiinin mitat ja 3D-malli |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Henkilöllisyystodistus | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| IUPAC-nimi | hydratsiini | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Synonyymit |
diatsaani, diamiini |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100,005,560 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O EY | 206-114-9 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 8058 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hymyilee |
NN , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1 / H4N2 / c1-2 / h1-2H2 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ulkomuoto | hygroskooppinen, väritön, savuinen neste, jolla on pistävä haju. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kemialliset ominaisuudet | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Raaka kaava | N 2 H 4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Moolimassa | 32,0452 ± 0,0007 g / mol H 12,58%, N 87,42%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dipolaarinen hetki | 1,75 D | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molekyylihalkaisija | 0,390 nm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fyysiset ominaisuudet | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fuusio | 2 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° kiehuu | 114 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Liukoisuus | sekoittuu veteen ja polaarisiin orgaanisiin liuottimiin |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Liukoisuusparametri δ |
37,3 MPa 1/2 ( 25 ° C ) 36,2 J 1/2 · cm -3/2 ( 25 ° C ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tilavuusmassa |
1010 kg · m -3
yhtälö:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Leimahduspiste | 38 ° C ( vrt. ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Räjähdysrajat ilmassa | 1,8 - 100 tilavuusprosenttia | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kyllästävä höyrynpaine | vedetön: 21 mbar ( 20 ° C ), liuos 64 % m : ssä: yhtälö:
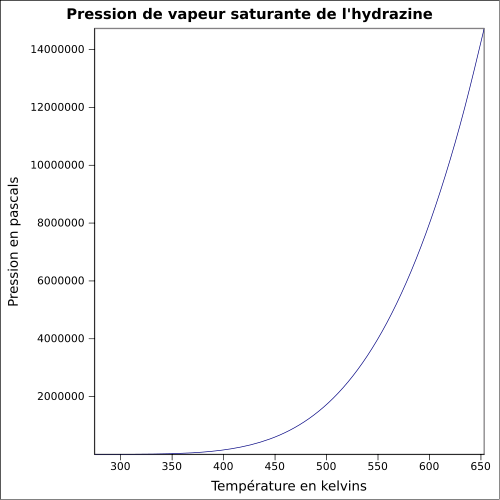
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dynaaminen viskositeetti | 0,9 mPa · s ajan 25 ° C: ssa | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kriittinen piste | 147,0 bar , 379,85 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lämpökemia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0- kaasu, 1 bar | 238,68 J · K -1 · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 neste, 1 bar | 121,52 J · K -1 · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| A f H 0 -kaasu | 95,35 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 neste | 50,63 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ vap H ° |
41,8 kJ · mol -1 ( 1 atm , 113,55 ° C ); 44,7 kJ · mol -1 ( 1 atm , 25 ° C ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C s |
yhtälö:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PCS | 667,1 kJ · mol -1 ( 25 ° C , kaasu) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PCI | -622,08 kJ · mol -1 (kaasu) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sähköiset ominaisuudet | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 re ionisaatioenergia | 8,1 ± 0,15 eV (kaasu) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Optiset ominaisuudet | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Taitekerroin | 1,469 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Varotoimenpiteet | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
     Vaara H226, H301, H311, H314, H317, H331, H350, H410, P201, P261, P273, P280, P301 + P310, P305 + P351 + P338, H226 : Syttyvä neste ja höyry H301 : Myrkyllistä nieltynä H311 : Myrkyllistä joutuessaan iholle H314 : Voimakkaasti ihoa syövyttävää ja silmiä vaurioittavaa H317 : Voi aiheuttaa allergisia iho reaktio H331 : Myrkyllistä hengitettynä H350 : Saattaa aiheuttaa syöpää (osoittavat altistumisreitti jos on kiistatta osoitettu, että mikään muu altistumisreittien syy vaara) H410 : Erittäin myrkyllistä vesieliöille, pitkäaikaisia haittavaikutuksia P201 : Lue erityisohjeet ennen käyttöä. P261 : Vältä pölyn / savun / kaasun / sumun / höyryjen / suihkeen hengittämistä. P273 : Vältä päästämistä ympäristöön. P280 : Käytä suojakäsineitä / suojavaatetusta / silmiensuojainta / kasvonsuojainta. P301 + P310 : Nieltynä: Ota välittömästi yhteys MYRKYTYSTIETOKESKUKSEEN tai lääkäriin. P305 + P351 + P338 : Roiskeet silmiin: Huuhtele varovasti vedellä useita minuutteja. Poista piilolinssit, jos uhri käyttää niitä ja ne voidaan helposti poistaa. Jatka huuhtelua. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
   B3, D1A, D2A, E, B3 : Palava neste D1A : Erittäin myrkyllinen aine, joka aiheuttaa välittömät vakavat vaikutukset D2A : Erittäin myrkyllinen aine, joka aiheuttaa muita myrkyllisiä vaikutuksia E : Syövyttävä materiaali 0,1%: n paljastus ainesosaluettelon mukaan |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3 3 3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Muu | Voi hyökätä hermostoon. Tappava suurina annoksina. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kuljetus | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
0113 : GUANYL NITROSAMINOGUANYLIDENE HYDRAZINE Kostutettu vähintään 30 painoprosentilla vettä Luokka: 1 Luokituskoodi: 1.1A : Aineet ja esineet, joihin liittyy massaräjähdysvaara (massaräjähdys on räjähdys, joka melkein välittömästi vaikuttaa melkein kaikkiin lastaus). Ensisijainen räjähtävä materiaali. Etiketti: 1 : Räjähteet ja esineet 
663 : erittäin myrkyllinen ja syttyvä materiaali (leimahduspiste enintään 60 ° C ) YK-numero : 1163 : ASYMMETRIC DIMETHYLHYDRAZINE Luokka: 6.1 Luokituskoodi: TFC : Syttyvät syövyttävät myrkylliset aineet. ; Etiketit: 6.1 : Myrkylliset materiaalit 3 : Syttyvät nesteet 8 : Syövyttävät materiaalit   
663 : erittäin myrkyllinen ja syttyvä materiaali (leimahduspiste enintään 60 ° C ) YK-numero : 1244 : METYYLIHYDRAZIINI Luokka: 6.1 Luokituskoodi: TFC : Syttyvät syövyttävät myrkylliset aineet. ; Etiketit: 6.1 : Myrkylliset materiaalit 3 : Syttyvät nesteet 8 : Syövyttävät materiaalit   
886 : erittäin syövyttävä ja myrkyllinen materiaali YK-numero : 2029 : VEDETTY HYDRAZIINI Luokka: 8 Luokituskoodi: CFT : Syövyttävät aineet nestemäiset, syttyvät, myrkylliset; Tarrat: 8 : Syövyttävä materiaalit 3 : Palavat nesteet 6.1 : Myrkylliset aineet Pakkaus: Pakkaus ryhmä I : erittäin vaaralliset aineet;   
86 : syövyttävä tai lievästi syövyttävä ja myrkyllinen YK-numero : 2030 : HYDRAZIINIHYDRAATTI, joka sisältää yli 37 prosenttia mutta enintään 64 prosenttia (massa) hydratsiinia; tai HYDRAZINE AQUEOUS SOLUTION, joka sisältää yli 37 mutta enintään 64 painoprosenttia hydratsiinia Luokka: 8 Luokituskoodi: CT1 : Myrkylliset syövyttävät aineet : Nesteet; Tarrat: 8 : Syövyttävät aineet 6.1 : Myrkylliset aineet Pakkaus: Pakkaus ryhmä I / II : erittäin / melko vaarallisia aineita;  
86 : syövyttävä tai vähäistä syövyttävyyttä ja myrkyllisyyttä osoittava YK-numero : 2030 : HYDRAZIINIHYDRAATTI, joka sisältää yli 37 mutta enintään 64 painoprosenttia hydratsiinia tai HYDRAZINE AQUEOUS SOLUTION, joka sisältää yli 37 mutta enintään 64 painoprosenttia hydratsiinia Luokka: 8 Luokituskoodi: CT1 : Myrkylliset syövyttävät aineet : Nesteet; Tarrat: 8 : Syövyttävät aineet 6.1 : Myrkylliset aineet Pakkaus: Pakkaus ryhmä III : joilla on pieni vaara.  
663 : erittäin myrkyllinen ja syttyvä materiaali (leimahduspiste enintään 60 ° C ) YK-numero : 2382 : SYMMETRIC DIMETHYLHYDRAZINE Luokka: 6.1 Luokituskoodi: TF1 : Syttyvät myrkylliset aineet: Nesteet; Tarrat: 6.1 : Myrkylliset aineet 3 : Palavat nesteet Pakkaus: Pakkaus ryhmä I : erittäin vaaralliset aineet;  
60 : myrkyllinen tai vähäistä myrkyllisyyttä aiheuttava aine YK-numero : 2572 : FENYYLIDYDRAZIINI Luokka: 6.1 Luokituskoodi: T1 : Myrkylliset aineet ilman toissijaista riskiä: Orgaaniset, nesteet; Label: 6.1 : Myrkylliset aineet Pakkaus: Pakkaus ryhmä II : kohtalaisen vaarallisia aineita; 
3165 : LENTOKONEIDEN HYDRAULISEN MOOTTORIN POLTTOAINESÄILIÖ, joka sisältää vedettömän hydratsiinin ja monometyylihydratsiinin (polttoaine M86) seosta Luokka: 3 Luokituskoodi: FTC : Syttyvä, myrkyllinen, Syövyttävät nesteet Tarrat: 3 :Syttyvätnesteet 6.1 : Myrkylliset aineet 8 : Syövyttävät aineet Pakkaus: Pakkaus ryhmä I : erittäin vaaralliset aineet;   
60 : materiaali myrkyllisiä tai esittää vähäisessä määrin myrkyllisyys YK-numero : 3293 : HYDRAZINE vesiliuosta, joka sisältää enintään 37 prosenttia (massasuhde) hydratsiinia luokka: 6,1 Luokituskoodi: T4 : Myrkylliset aineet ilman lisävaaraa: Epäorgaaniset, neste; Label: 6.1 : Myrkylliset aineet Pakkaus: Pakkaus ryhmä III : joilla on pieni vaara.  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| IARC- luokitus | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ryhmä 2B: Mahdollisesti karsinogeeninen ihmisille | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ekotoksikologia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LogP | -3,1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hajukynnys | matala: 3 ppm korkea: 4 ppm |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SI- ja STP- yksiköt, ellei toisin mainita. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Hydratsiinia , virallinen nimi diazane , on kemiallinen kaava N 2 H 4 ja rakennekaava H 2 -N-NH 2 , on kemiallinen yhdiste, väritön neste, jonka haju muistuttaa ammoniakkia . Se sekoittuu veteen kaikissa suhteissa.
Hydratsiinit myös muodostavat perheen kemiallisia yhdisteitä, jotka on johdettu hydratsiinia (H 2 -N-NH 2 substituoimalla yksi tai useampia H-atomeja mukaan hiilivetyradikaaleja (esimerkiksi 2,4-dinitrofenyylihydratsiinin ).
Hydratsiinin vuosituotanto on 260 000 tonnia. Suurinta osaa tästä tuotannosta käytetään vaahdotusaineena vaahdotettujen polymeerien valmistuksessa . Loput tästä tuotannosta on jaettu eri aloilla, kuten orgaanisen kemian synteesin huumeiden tai epäorgaanisen kemian tuotantoon natriumatsidia , räjähtävä aine paisuttaa " turvatyynyjen " (puhallettava turvallisuus pussit). Hydratsiinia voidaan käyttää myös rakettimoottoripolttoaineena .
Molekyylirakenne ja ominaisuudet
Hydratsiinin rakenne esitetään kahtena ammoniakkimolekyylinä kytkettynä toisiinsa poistamalla yksi vety kummallekin molekyylille. Kukin -NH 2 alayksikkö on pyramidin muotoinen. Kahden typpiatomin välinen etäisyys on 145 pm , ja molekyyli omaksuu antiklinaalisen konformaation. Vääntömomentti on kaksinkertainen etaaniin nähden . Sen rakenteelliset ominaisuudet muistuttavat vetyperoksidikaasun ominaisuuksia , joka omaksuu "epäsymmetrisen" konformaation, joka on samanlainen kuin lineaarinen alkaanirakenne, jolla on suuri vääntömomentti.
Sen emäksen ominaisuudet ovat verrattavissa ammoniakkiin , mutta 15 kertaa heikompia.
Kunkin amiinin substituentti tekee elektronisesta dubletista vähemmän käytettävissä protonin imemiseen ja siten vähemmän emäksisen. Hydratsiini on parempi nukleofiili kuin ammoniakki johtuen vierekkäisten typpiatomien ei-sitovien dublettien välisestä syrjäytymisestä.
Toinen protonaatio on vaikeampaa:
[N 2 H 5 ] ++ H + → [N 2 H 6 ] 2+ ; K = 8,4 x 10 -16Hydratsiini on paljon vahvempi pelkistin emäksisessä ympäristössä kuin happamassa ympäristössä. (E = -0,23 V pH = 0 ja E = -1,16 V pH = 14). Kun hydratsiini reagoi hapettimien kanssa, voi muodostua erilaisia typpipitoisia tuotteita, mutta yleensä se on dityppi. Hydratsiinin reaktio dioksidin kanssa muodostaa ditypen ja veden samalla kun vapautuu suuri määrä lämpöä.
Hydratsiini N 2 H 4hajoaa lämmön ja ultraviolettisäteiden vaikutuksesta typeksi N 2, Vety H 2ja ammoniakki NH 3.
Jotkut suolat hydratsiinia räjähtäviä : nitraatti hydratsiinia , kloraatti hydratsiinia perkloraatti hydratsiinia ja atsidin hydrazonium.
Fysikaalis-kemialliset ominaisuudet
Vedetön hydratsiini on väritön, savuton neste, jolla on amiinihaju. Hajukynnys on 3 ppm .
Synteesi
Theodor Curtius syntetisoi yksinkertaisen hydratsiinin ensimmäisen kerran vuonna 1889 takaoven kautta.
Hydratsiini tuotetaan Olin Raschigin prosessilla natriumhypokloriitista ja ammoniakista , menetelmä keksittiin vuonna 1907. Tämä prosessi perustuu klooriamiinien reaktioon ammoniakin kanssa.
NH 2 : lla+ NH 3→ H 2 N - NH 2+ HCl .Tarvittava monokloramiini, jota reaktio tuottaa etukäteen: NH 3 + HOCI → NH 2 : lla + H 2 OVariantti Olin Raschig- prosessin on hapetus urean mukaan natriumhypokloriittia :
(H 2 N) 2 C = O+ NaOCI: + 2 NaOH → N 2 H 4+ H 2 O+ NaCI + Na 2 CO 3.Atofina-PCUK-syklissä hydratsiini valmistetaan useissa vaiheissa asetonista , ammoniakista ja vetyperoksidista. Asetoni ja ammoniakki reagoivat ensin antamaan imiinin , minkä jälkeen reaktio hapetetaan vetyperoksidin kanssa oksatsiridiinissä , heterosykli - kolme atomia, jotka käsittävät hiiliatomin, typpiatomin ja happiatomin, minkä jälkeen seuraa ammoniolyysi, joka johtaa hydratsoniin , prosessi joka yhdistää kaksi typpiatomia. Hydratsoni reagoi ylimäärän asetonin kanssa ja tuotettu asetoniasiini hydrolysoidaan hydratsiiniksi muodostaen asetonin regeneroinnin. Toisin kuin Raschig-prosessi, tämä menetelmä ei tuota suolaa. PCUK liittyy ranskalaiseen kemikaalien valmistajaan Ugine Kuhlmanniin .
Hydratsiini voidaan valmistaa myös menetelmällä, joka tunnetaan nimellä ketatsiini- ja peroksidimenetelmä .
Vuonna 2001 Marc Strous, mikrobiologina Nijmegenin yliopiston Alankomaissa havaittu, että hydratsiinia valmistetaan hiivat ja valtameren bakteeri , Brocadia anammoxidans , kautta anaerobinen ammoniumtypen hapetus reaktio suoritetaan erikoistunut organelles kutsutaan anammoxosomes . Ne ovat ainoat tällä hetkellä tunnetut elävät organismit, jotka pystyvät luonnollisesti tuottamaan hydratsiinia.
Johdannaiset
Monet hydratsiinisubstituutiojohdannaiset tunnetaan, ja useat niistä tuotetaan luonnollisesti. Joitain esimerkkejä :
- gyromitrine (in) ja agaritine (in) ovat fenyylihydratsiineihin löytyy lajien sieniä viljellään ja markkinoinut Agaricus bisporus . Gyromitriini metaboloituu monometyylihydratsiiniksi ;
- iproniatsidin , hydralatsiini ja feneltsiini (fi) ovat lääkkeitä valmistettu hydratsiini;
- 1,1-dimetyylihydratsiinia (UDMH) ja 1,2-dimetyylihydratsiinia (fi) ovat hydratsiinit, jossa kaksi vetyatomia on korvattu metyyliryhmällä ;
- 2,4-dinitrofenyylihydratsiinia (2,4-DNPH) on yleisesti käytetty testaamiseen ja ketonien ja aldehydien on orgaanisessa kemiassa ;
- fenyylihydratsiinia , C 6 H 5 NHNH 2 , hydratsiini on ensimmäinen, joka on löydetty.
Käyttö kemiassa
Hydratsiineja käytetään monien orgaanisten molekyylien synteesissä, ja monilla niistä on käytännön merkitystä lääketeollisuudessa , tuberkuloosin vastaisena lääkkeenä , samoin kuin tekstiileissä väriaineena ja valokuvauksessa.
Sitä esiintyy myös teollisuudessa yleensä ja erityisesti sekoitettuna höyrykattiloiden syöttöveden kanssa. Sen tarkoituksena on tuhota viimeiset happimolekyylit ja siten estää teräshöyrylinjojen syöpyminen.
Reaktio karbonyylien kanssa
Hydratsiinin kondensaation karbonyyliradikaalin kanssa havainnollistamiseksi mainitaan reaktio asetonin kanssa, joka johtaa di-isopropylideenihydratsiinin muodostumiseen. Tämä reagoi jälleen hydratsiinin kanssa muodostaen hydratsonin:
2 (CH 3 ) 2 CO+ N 2 H 4→ 2 H20+ [(CH 3 ) 2 C = N] 2. [(CH 3 ) 2 C = N] 2+ N 2 H 4→ 2 (CH 3 ) 2 C = N - NH 2.Asetoni ja di-isopropylideenihydratsiini ovat välituotteita PCUK-Atofina-synteesissä. Alkylointi suora hydratsiinien alkyylihalogenideja , kun läsnä on emästä muodon alkyloidut johdannaiset hydratsiinit, mutta reaktio on yleensä tehotonta johtuen huonosta valvonnan substituutioaste (kuten amiinit yhteinen). Hydratsonin pelkistäminen hydratsiiniksi on tyylikäs tapa tuottaa dialkyloituja 1,1-hydratsiineja.
Toisessa reaktiossa, 2-syaani pyridiini reagoi hydratsiinin kanssa muodostaen amidoitu hydratsidit, jotka voidaan muuntaa triatsiinit käyttäen 1,2-diketonit.
Wolff-Kishnerin reaktio
Hydratsiinia käytetään orgaanisessa kemiassa on Wolff-Kishner , reaktio, joka muuntaa karbonyyliryhmä ryhmä on ketonin tai aldehydin osaksi metyleenisillan (tai metyyli -ryhmä ) kautta molekyyli hydratsoni . Tuotannon erittäin vakaa dityp- hydratsiinista edistää reaktiota.
Polysyklisten molekyylien synteesi
Koska hydratsiinilla on kaksi amiinifunktiota, se on keskeinen osa monien heterosyklisten yhdisteiden valmistuksessa kondensoimalla osan kanssa, jolla on kaksi elektrofiilistä toimintoa . Kanssa asetyyliasetoni , se tiivistyy antaa 3,5-dimetyylipyratsoliliuos . Einhorn-Brunner-reaktiossa hydratsiinit reagoivat imidien kanssa, jolloin saadaan triatsoleja .
Sulfonointi
On hyvä nukleofiili, N 2 H 4 on altis hyökkäykselle sulfonyylihalogenideja ja asyylihalogenidit. Tosyyli hydratsiinia myös muodostaa hydratsoneja hoidon jälkeen karbonyylit.
Ftalimidien hajoaminen
Hydratsiinia käytetään N- ftalimidin jakamiseksi alkyylijohdannaisiksi. Tämä pilkkomisreaktio sallii ftalimidianionin käytön amiinin esiasteena Gabrielin synteesissä.
Pelkistin
Hydratsiini on suosittu pelkistin, koska sen hajoamisen sivutuotteet ovat yleensä typpikaasua ja vettä. Siten sitä käytetään antioksidanttina , hapenpoistoaineena ja korroosionestoaineena kattiloiden ja lämmityspiirien vedessä (tässä tehtävässä N, N-dietyylihydroksyyliamiini on nyt edullinen , vähemmän myrkyllinen, mutta sitä käytetään edelleen laajalti korroosiota vastaan suurissa erityisesti lämpö- ja ydinvoimalat ). Sitä käytetään myös vähentämään suoloja ja metallioksideista metalliseen olomuotoon elektrolyysissä nikkeliä sekä uuttamalla plutoniumin peräisin käytetyn ydinpolttoaineen .
Hydratsiinisuolat
Hydratsiini muuttuu kiinteiksi suoloiksi käsittelemällä mineraalihapoilla. Yleisin suola on hydratsiini vetysulfaatti, N 2 H 5 HSO 4 , joka tulee todennäköisesti kutsutaan hydratsiinia bisulfaatti. Hydratsiinibisulfaattia käytetään vaihtoehtoisena hoitona syövän aiheuttamaan kakeksiaan . Suolan hydratsiini ja N- 5 H- 5 azothydric happo oli tieteellinen kiinnostus, koska sen korkea typpipitoisuus ja räjähtäviä ominaisuuksia.
Teolliseen käyttöön
Hydratsiinia käytetään monissa prosesseissa, esimerkiksi kuitujen ja elastaania , kuten katalyytti ja polymeroinnin , paisutteen, ja polttokennot , kuten juoksutetta, ja hitsaus , kehittää valokuvia, kuten extender ketju polymerointiin polyuretaani , kuten pelkistävä yhdiste veden säätämiseen ydinvoimaloiden lämpövoimaloissa ja toissijaisissa piireissä sekä lämmön stabilointiaineena. Lisäksi on äskettäin testattu tekniikkaa, jossa käytetään hydratsiinikerroksia puolijohteissa, ja sitä voidaan soveltaa nestekidenäyttöihin käytettävien ohutkalvotransistoreiden valmistukseen . Hydratsiinia 70-prosenttisessa liuoksessa, jossa on 30-prosenttista vettä, käytetään EPU: n (hätävoimayksikkö) käyttämiseen F-16 ( General Dynamics F-16 Fighting Falcon ) hävittäjiin .
Sotilaskäytössä, hydratsiinin peräisin oleva aine, epäsymmetrinen dimetyyli hydratsiinia (UDMH) , yhdistettynä ammoniumnitraatin on perusraaka-aine on astrolite (in) , räjähtävä erittäin voimakas keksittiin 1960-luvulla.
Rakettipolttoaine
Hydratsiinia ensin käytettiin rakettien polttoaineena on toisen maailmansodan varten Messerschmitt Me 163 tasot (ensimmäinen raketti kone), nimellä B-Stoff (itse asiassa, hydratsiinihydraattia ). Tämä B-Stoff sekoitettiin metanolin ( M-Stoff ) kanssa, jolloin saatiin C-Stoff , jota käytettiin polttoaineena T-Stoffin kanssa , vetyperoksidikonsentraatti , jota käytettiin hapettimena kosketuksessa, jonka kanssa se syttyi itsestään. erittäin energinen reaktio.
Nykyään hydratsiinia käytetään yleensä yksinään monimoottorina pienen työntövoiman moottoreissa (mutta erittäin tarkoissa) moottoreissa, jotka mahdollistavat satelliittien ja avaruuskoettimien sijainnin kiertoradalla ; tässä tapauksessa työntövoima aikaansaadaan hydratsiinin katalyyttisellä hajoamisella eikä palamisella. Tämä hajoaminen on todellakin hyvin eksoterminen reaktio . Se saadaan johtamalla hydratsiini katalysaattorin yli, jonka aktiivinen komponentti on metallinen iridium, joka on kerrostettu suurelle alumiinioksidin (alumiinioksidi) pinnalle , tai hiilinanokuidut, tai viime aikoina molybdeeninitridi alumiinioksidille tai jopa molybdeeninitraatti . Sen hajoaminen ammoniakiksi , typeksi ja vedyksi johtuu seuraavista reaktioista:
Tämä hajoaminen laukaisee muutamassa millisekunnissa ja antaa työntövoiman mitata hyvin tarkasti. Nämä reaktiot ovat hyvin eksotermisiä (katalyytti kammiossa voi saavuttaa 800 ° C: ssa muutamassa millisekunnissa), ja tuottaa suuri määrä kuumien kaasujen pienestä määrä nestettä hydratsiinia, joten se on hyvä ponneainetta varten tilaa työntövoimaa .
Tiettyjä hydratsiinijohdannaisia käytetään myös nestemäisinä ponneaineina : monometyylihydratsiini H 2 N - NHCH 3(tai MMH), ja epäsymmetrinen dimetyylihydratsini , H 2 N - N (CH 3 ) 2(tai UDMH). Niitä käytetään yleensä typen peroksidia N 2 O- 4hapettimena, jonka kanssa ne muodostavat varastoitavan hypergolisen nestemäisen ponneaineen .
Polttokennot
Italian katalyytti valmistaja Acta on ehdotettu käytettäväksi hydratsiinia vaihtoehtoinen ratkaisu vedyn polttokennojen . Tärkein etu tämä tuote on sen kyky tuottaa yli 200 mW / cm 2 , enemmän kuin vastaava vetypolttokennoihin ilman kalliita katalyyttejä, jotka sisältävät platinaa . Koska polttoaine on huoneen lämpötilassa nestemäistä, sitä voidaan käsitellä ja varastoida helpommin kuin vetyä. Varastamalla hydratsiinia säiliöön, joka sisältää karbonyylin, jossa on hiili- happi kaksoissidos , polttoaine reagoi ja muodostaa kiinteän, turvallisen materiaalin, jota kutsutaan hydratsooniksi . Täytä sitten vain säiliö kuumalla vedellä vapauttamaan hydratsiinihydraatti nestemäisessä muodossa. Nestemäisen polttoaineen käsittely on käytännössä paljon turvallisempaa kuin vetykaasun, ja nesteellä on suurempi redoksipotentiaali (1,56 V ) kuin vetyä kohden 1,23 V. Hydratsiinimolekyyli rikkoutuu paristossa muodostaen typpi- ja vetyatomeja , jotka sitoutuvat happiatomiin muodostaen vettä.
turvallisuus
Myrkyllisyys, ekotoksisuus
Hydratsiini on erittäin myrkyllistä ja vaarallisesti epästabiilia, etenkin vedettömässä muodossa . Sitä käytetään yleensä stabiilina monohydraattina .
Akuutin altistumisen korkeille hydratsiinipitoisuuksille oireet voivat ilmetä ihmisillä silmien , nenän ja kurkun ärsytyksenä , huimauksena, päänsärkynä , pahoinvointina , keuhkopöhönä , kouristuksina , koomana . Akuutti altistuminen voi myös vahingoittaa maksaa , munuaisia ja keskushermostoa ihmisillä. Neste on syövyttävää ja voi aiheuttaa kontaktiekseemaa ihmisillä ja eläimillä. Haitallisia vaikutuksia keuhkoihin , maksaan, pernaan ja kilpirauhaseen on raportoitu eläimillä, jotka ovat altistuneet kroonisesti hydratsiinille hengitettynä. Kasvu useissa keuhkojen, nenän ontelo, ja maksan kasvainten on havaittu jyrsijöillä alttiina hydratsiinia.
Sen myrkyllisyys arvioidaan säännöllisin väliajoin tiedon kehittyessä.
Viitteet
- HYDRAZINE (vedetön) , kansainvälisen kemikaaliturvallisuusohjelman käyttöturvallisuustiedote (t) , kuultu 9. toukokuuta 2009
- (en) Yitzhak Marcus, The Properties of Solvents , voi. 4, Englanti, John Wiley & Sons Ltd,1999, 239 Sivumäärä ( ISBN 0-471-98369-1 )
- laskettu molekyylimassa välillä " Atomic painot Elements 2007 " on www.chem.qmul.ac.uk .
- (in) James E. Mark, Physical Properties of Polymer Handbook , Springer,2007, 2 nd ed. , 1076 Sivumäärä ( ISBN 978-0-387-69002-5 ja 0-387-69002-6 , luettu verkossa ) , s. 294
- (en) Robert H. Perry ja Donald W. Green , Perry's Chemical Engineers 'Handbook , USA, McGraw-Hill,1997, 7 th ed. , 2400 Sivumäärä ( ISBN 0-07-049841-5 ) , s. 2-50
- Merkintä "Hydratsiini" IFA: n (saksalainen työturvallisuudesta ja -terveydestä vastaavan elimen) kemikaalitietokantaan GESTIS ( saksaksi , englanniksi ), käytetty 11. helmikuuta 2010 (vaaditaan JavaScriptiä)
- " Eri kaasujen ominaisuudet ", osoitteessa flexwareinc.com (käytetty 12. huhtikuuta 2010 )
- (en) "Hydrazine" , NIST / WebBookissa , käytetty 11. helmikuuta 2010
- (in) David R. LiDE, CRC Handbook of Chemistry and Physics , CRC Press,2009, 90 th ed. , 2804 Sivumäärä , Kovakantinen ( ISBN 978-1-4200-9084-0 )
- (in) David R. LiDE , CRC Handbook of Chemistry and Physics , Boca Raton, CRC Press,18. kesäkuuta 2002, 83 th ed. , 2664 Sivumäärä ( ISBN 0849304830 , online-esitys ) , s. 5-89
- (in) David R. Lide, Handbook of Chemistry and Physics , Boca Raton, CRC,2008, 89 th ed. , 2736 Sivumäärä ( ISBN 978-1-4200-6679-1 ) , s. 10-205
- IARC: n ihmisille karsinogeenisten riskien arviointia käsittelevä työryhmä " Evaluations Globales de la Carcinogenicité pour l'Homme, Groupe 2B: Mahdollisesti karsinogeeninen ihmisille " , http://monographs.iarc.fr , IARC,16. tammikuuta 2009(katsottu 22. elokuuta 2009 )
- Indeksinumero EY-asetuksen N: o 1272/2008 liitteen VI taulukossa 3.1 (16. joulukuuta 2008)
- SIGMA-ALDRICH
- " Hydratsiini " tietokannassa kemikaalien Reptox että CSST (Quebec organisaatio, joka vastaa työsuojelun), pääsee 24 huhtikuu 2009
- " Hydrazine " osoitteessa hazmap.nlm.nih.gov (käytetty 14. marraskuuta 2009 )
- ”hydratsiini” , ESIS-tietokannassa , käyty 17. helmikuuta 2009
- Miessler, Gary L. ja Tarr, Donald A. epäorgaaninen kemia, kolmas painos . Pearson Prentice Hall (2004). ( ISBN 978-0-13-035471-6 ) .
- epäorgaaninen kemia, DF Shriver, Peter William Atkins
- Orgaanisen kemian säätiöt, Michael Hornby, Josephine Peach
- (sisään) Holleman, AF, Wiberg, E. "Inorganic Chemistry" Academic Press: San Diego, 2001. ( ISBN 978-0-12-352651-9 ) .
- INRS-turvatiedote
- Curtius, Journal für praktische Chemie , 39, 1889, s. 107-39
- Adams, R.; Ruskea, BK, hydratsiinisulfaatti, 1, 309, 1941, cv1p0309
- " Hydrazine: Kemiallisten tuotteiden tiedot, chemindustry.ru, 2007-01-08 " ( Arkisto • Wikiwix • Archive.is • Google • Mitä tehdä? ) (Pääsy 25. maaliskuuta 2013 )
- Riegel, Emil Raymond. "Hydratsiini" Riegelin teollisen kemian käsikirja s. 192 (1992).
- (vuonna) Brian Handwerk , " Bakteerit syövät ihmisen jätevettä, tuottavat rakettipolttoainetta " , National Geographic Society ,9. marraskuuta 2005( luettu verkossa , kuultu 12. marraskuuta 2007 )
- National Geographic http://news.nationalgeographic.com/news/2005/11/1109_051109_rocketfuel.html
- [päivä, AC; Valkoturska, MC; Asetonihydratsoni; osa 6 | sivu 10; cv6p0010;]
- [Wiley, RH; Hexner, PE; 3,5-dimetyylipyratsoli, osa 4, sivu 351; cv4p0351]
- [Friedman, L; Litle, RL; Reichle, WR; p- tolueenisulfonyylihydratsidi; vol 5; sivu 1055, cv5p1055]
- [Weinshenker, NM; Shen, CM; Wong, JY; polymeerikarbodi-imidi; osa 6, sivut 951; (1988); cv6p0951]
- 2013 Ydinvoimala läpäisee kemikaaleja Fundynlahdelle New Brunswickin ydinvoimala raportoi kemikaalivuodosta Fundynlahdella (Canadian Press in Energy and Resources ) 3013-11-05, luettu 3013-11-06
- (fi) R. Vieira , ” New hiili nanofiber / grafiittivillaeriste komposiitti käytettäväksi katalyyttinä tuki hydratsiini katalyyttinen hajoaminen ” , Chemical Communications , n o 9,2002, s. 954–955 ( DOI 10,1039 / b202032g )
- (en) Xiaowei Chen , " Hydratsiinin katalyyttinen hajoaminen tuettujen molybdeeninitridikatalyyttien päällä monopopellanttitrottorissa " , Catalysis Letters , voi. 79,Huhtikuu 2002, s. 21–25 ( DOI 10.1023 / A: 1015343922044 )
- " Nestemäinen omaisuus - Uutiset - Insinööri - Uutiset: tekniset uutiset, insinööritiedot, uusin tekniikka, valmistusuutiset, valmistustiedot, autoteutiset , ilmailu-, avaruus- ja materiaaliuutiset, tutkimus ja kehitys " ( Arkisto • Wikiwix • Archive.is • Google • Mitä tehdä? )
- ARC, Monografia, osa 71 (1999) Joidenkin orgaanisten kemikaalien, hydratsiinin ja vetyperoksidin uudelleenarviointi .
- Sylvie Tissot, Annick Pichard, " Välitön myrkyllisyyden kynnysarvo hydratsiini (NH 2 NH 2 ) - loppuraportti " [PDF] , ineris.fr , Kansallinen teollisuusympäristö ja riskit ,elokuu 2003(käytetty 29. lokakuuta 2015 ) .








