Helium
| Helium | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Ylimääräinen nestemäinen helium ( T ≤ 2 K ). | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sijainti jaksollisessa taulukossa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Symboli | Hei | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sukunimi | Helium | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomiluku | 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ryhmä | 18 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aika | 1 e jakso | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lohko | Estä s | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Element perhe | jalokaasu | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektroninen kokoonpano | 1 s 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Elektronit by energiataso | 2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomic ominaisuudet elementin | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomimassa | 4,002602 ± 0,000002 u | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Atomisäde (laskettu) | 128 pm ( 31 pm ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kovalenttinen säde | 28 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Van der Waalsin säde | 140 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hapetustila | 0 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oksidi | tuntematon | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ionisointienergiat | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 re : 24.587387 eV | 2 e : 54,417760 eV | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vakaimmat isotoopit | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Yksinkertaiset kehon fyysiset ominaisuudet | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Tavallinen tila | Kaasu | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
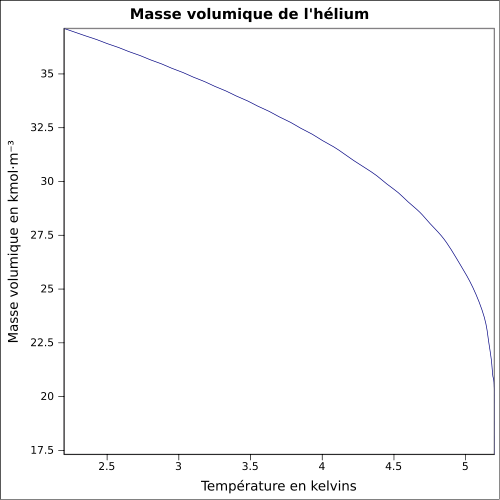
| Tilavuusmassa |
0,1786 g · L -1 ( 0 ° C , 1 atm ); 0,125 kg · L -1 (neste, -268,93 ° C ) yhtälö:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kristallijärjestelmä | Kompakti kuusikulmainen | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Väri | Väritön | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fuusiopiste | 0,95 K ( 26 atm ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kiehumispiste | -268,93 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fuusioenergia | 5,23 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Höyrystysenergia | 0,08 kJ · mol -1 ( 1 atm , -268,93 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kriittinen lämpötila | -267,96 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kriittinen paine | 2,26 atm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Molaarinen tilavuus | 22,414 × 10-3 m 3 · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Höyrynpaine |
yhtälö:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Äänen nopeus | 972 m · s -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Massalämpö | Cp 20,79 J · mol -1 · K -1
yhtälö:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Lämmönjohtokyky | 152,0 mW · m -1 · K -1 ( 26,85 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Eri | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100 028 334 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N O EY | 231-168-5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Varotoimenpiteet | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Varoitus H280 ja P410 + P403 H280 : Sisältää paineen alaista kaasua; voi räjähtää kuumennettaessa P410 + P403 : Suojaa auringonvalolta. Säilytä hyvin ilmastoidussa tilassa. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 AT, V : Paineistetun kaasun kriittinen lämpötila = −267,9 ° C Ilmoitus 1,0%: lla luokituskriteerien mukaan |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Kuljetus | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
1046 : PURISTETTU HELIUM- luokka: 2.2 Merkintä: 2.2 : Palamattomat, myrkyttömätkaasut(vastaa A: n tai ison O: n osoittamia ryhmiä)  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SI- ja STP- yksiköt, ellei toisin mainita. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Helium on alkuaine on järjestysluku 2 He symboli. Se on jalokaasu (tai jalokaasun), käytännöllisesti katsoen inerttejä , ensimmäinen jalokaasun perhe on jaksollisen järjestelmän elementtien . Sen kiehumispiste on alhaisin tunnettujen kappaleiden joukossa, ja se esiintyy kiinteässä muodossa vain, kun siihen kohdistuu yli 25 ilmakehän paine .
Heliumilla on kaksi stabiilia isotooppia : helium 4 ( 4 He), eniten ja helium 3 ( 3 He). Nämä kaksi isotooppia, toisin kuin useimpien kemiallisten alkuaineiden, eroavat ominaisuuksiltaan huomattavasti, koska niiden atomimassojen suhde on tärkeä. Toisaalta kvanttiefektit, jotka ovat herkkiä matalalla energialla, antavat niille hyvin erilaisia ominaisuuksia. Tämä artikkeli käsittelee pääasiassa heliumia 4 ( 4 He). Helium 3 -artikkelissa kootaan 3 He -isotoopin erityisominaisuudet .
Sana helium konstruoitiin kreikkalainen Helios ( Ἥλιος / Helios , " Sun " ), tämä elementti jotka on havaittu ensimmäistä kertaa auringon spektrin päällä18. elokuuta 1868, tähtitieteilijä Jules Janssen , täydellisen auringonpimennyksen aikana .
Helium on, sen jälkeen kun vety , kaikkein alkuaine Universe . Suurin osa tästä heliumista tuotettiin alkunukleosynteesin aikana, mutta muut prosessit tuottavat sitä, erityisesti a-radioaktiivisuus ( ks. Luku Luonnollinen runsaus ). On Maan mukaan arvio siitä Bureau of Land Management että Yhdysvalloissa vuonna 2006, heliumia henkilöstö Yhteensä 52 miljardin kuutiometrin.
Heliumilla on useita käyttökohteita voimakkaassa kasvussa, kun taas teollisuustuotanto on vähentynyt taloudellisista syistä: sen niukkuus on huolestuttavaa. Vuonna 2016 heliummarkkinat ovat kuitenkin taloudellisesta näkökulmasta rauhalliset ja ne ovat viime aikoina muuttuneet ylijäämäisiksi.
Kahdeksan heliumin isotooppia tunnetaan. Helium 3 (kaksi protonia ja yksi neutroni) ja helium-4 (kaksi protonia ja kaksi neutronia) ovat vakaita, toiset ovat erittäin epävakaita, käytännössä varmaa nykyisiä vasta koulutuksen aikana. Maapallon ilmakehässä on vain yksi helium-3- atomi jokaista miljoonaa helium-4- atomia kohden . Toisin kuin useimmat alkuaineet, heliumin isotooppinen runsaus vaihtelee suuresti sen alkuperästä riippuen erilaisista muodostumisprosesseista. Runsain isotooppi, helium 4 , tuotetaan maapallolla , jonka α radioaktiivisuus raskaiden elementtejä: α tuotetut hiukkaset on olemassa täysin ionisoidaan heliumin 4 ytimiä . Helium-4 on ydin epätavallinen vakautta, koska sen nukleoneista on järjestetty täydellistä kerroksiin .
Koko maailmankaikkeudessa suurin osa läsnä olevasta heliumista muodostui (valtavat määrät, noin 25% kaikista aineista) alkusukleosynteesin aikana . Lähes kaikki muu maailmankaikkeudessa tuotettu helium on (tai on ollut) tähtien nukleosynteesin aikana.
Helium-3 on esillä olevan maan päällä vain pieniä määriä; suurin osa on peräisin maapallon muodostumisesta, vaikkakin vähänkin putoaa siihen tähtienväliseen pölyyn loukussa . Jäljet ovat edelleen myös tuotettu β radioaktiivisuus on tritiumia . Kiviä maankuoren on isotooppisuhteet vaihtelee jopa 10-kertainen , ja nämä suhteet voidaan käyttää määrittämään alkuperää kiviä ja koostumus maapallon vaipan . Helium-3 on runsaampaa tähdet, mutta se on tuotettu ydinfuusion , tähdet eivät vapauta hyvin vähän (kuten deuterium ja litium , tai boori ), koska se n 'näkyy vain väliketju johtaa helium 4 : se "kulutetaan", kun se tuotetaan tähdissä. Tämän seurauksena tähtienvälisessä väliaineessa isotooppisuhde on noin 100 kertaa suurempi kuin maapallolla. Extraplanetary materiaaleja, kuten regolith päässä Moon tai asteroidit, on jälkiä heliumin 3 päässä aurinkotuulen . Kuun pinta sisältää pitoisuuden , joka on luokkaa 10-8 . Useat kirjoittajat ovat aloittaneet Gerald Kulcinskin vuonna 1986 ja ehdottaneet kuun tutkimista, helium-3: n uuttamista regoliitista ja sen käyttämistä energian tuottamiseen ydinfuusion avulla.
Helium-4 voidaan jäähdyttää noin 1 K haihduttamalla. Helium-3 , joka on alempi kiehumispiste, voidaan jäähdyttää 0,2 K samalla menetelmällä. Seokset, joissa on yhtä suuria osia heliumia 3 ja 4, eroavat alle 0,8 K , koska ne eivät ole enää sekoittuvia erojensa vuoksi ( helium 4- atomi on bosoni, kun taas heliumiatomi 3 on fermion , ne seuraavat kahta erilaista kvanttitilastoa) . Laimennus jääkaapit käyttävät tätä ominaisuutta, jotta saavutetaan millikelvins.
Muita heliumin isotooppeja voidaan tuottaa ydinreaktioilla , jotka ovat epävakaita ja hajoavat nopeasti muihin ytimiin. Lyhyimmän puoliintumisajan isotooppi on helium 2 (2 protonia, ilman neutroneja: diproton , joka hajoaa kahdeksi protoniksi 3 × 10 −27 s ). Helium 5 ja helium 7 reikiintymistä emissio neutronin kanssa puoli-elämän 7,6 x 10 -23 s ja 2,9 x 10 -21 s , vastaavasti. Helium 6 ja helium 8 luhistuu mukaan β radioaktiivisuus kanssa puoli-elämän 0,8 s ja 0,119 s , vastaavasti. Isotopes 6 ja 8 on löysä rakenne, jossa neutronien kiertävät kaukana sydän, sitä kutsutaan ydinvoiman halogeeni .
Yksi heliumrunko
Helium on väritön, hajuton ja myrkytön kaasu. Se on käytännössä kemiallisesti inertti , monoatominen kaikissa olosuhteissa. Laajalla lämpötila- ja painealueella se käyttäytyy kokeellisesti kuin ihanteellinen kaasu , mikä tekee siitä etuoikeutetun aineen fysikaalis-kemiallisten teorioiden kokeilemiseen. Kaksi stabiilia heliumin isotooppia ovat ainoat kemialliset yhdisteet, joilla ei ole kolmoispistettä .
Kaasu
Heliumkaasun lämmönjohtavuus on suurempi kuin kaikkien kaasujen, vetyä lukuun ottamatta, ja sen ominaislämpö on poikkeuksellisen korkea. Sen Joule-Thomson-kerroin on negatiivinen huoneenlämmössä, mikä tarkoittaa, että toisin kuin useimmat kaasut, se lämpenee, kun se voi rentoutua vapaasti. Joule-Thomson inversio lämpötilan on noin 40 K tai -233,15 ° C paineessa 1 atm . Jäähtyessään alle tämän lämpötilan helium voidaan nesteyttää jäähdyttämällä sen laajenemisen vuoksi.
Helium on myös vähiten vesiliukoinen kaasu kaikista tunnetuista kaasuista. Atomien pienen koon vuoksi diffuusionopeus kiintoaineiden läpi on kolme kertaa ilman ja noin 65% vedyn.
Heliumin taitekerroin on lähempänä yhtenäisyyttä kuin minkä tahansa muun kaasun. Äänen nopeus heliumissa on suurempi kuin missään muussa kaasussa paitsi vedyssä.
Toisin kuin plasma , kaasu on erinomainen sähköeriste.
Plasma
Suurin osa maapallon ulkopuolisesta heliumista löytyy plasmatilasta , jonka ominaisuudet poikkeavat selvästi atomiheliumin ominaisuuksista. Plasmassa heliumin elektronit eivät ole sitoutuneet ytimeen, mikä johtaa erittäin korkeaan sähkönjohtavuuteen, vaikka ionisaatio on osittainen. Varautuneet hiukkaset ovat hyvin herkkiä sähkö- ja magneettikentille. Esimerkiksi aurinkotuulessa ionisoitu helium ja vety ovat vuorovaikutuksessa maapallon magnetosfäärin kanssa aiheuttaen Birkelandin virtausten ja napa-auroran ilmiöitä .
Kuten muilla jalokaasuilla, heliumilla on metastabiilit energiatasot, jotka antavat sen pysyä innoissaan sähköpurkauksessa, jonka jännite on alle ionisaatiopotentiaalin. Tämä sallii sen käytön purkauslampuissa .
Nestemäinen
Toisin kuin muut alkuaineet, helium pysyy nestemäisenä absoluuttiselle nollalle alle 25 atm: n paineessa . Tämä on suora seuraus kvanttimekaniikasta: tarkemmin sanottuna järjestelmän perustilassa olevien atomien energia on liian korkea jähmettymisen mahdollistamiseksi (ks. Luku # Kiinteä ).
Alla kiehumispiste on 4,22 K ja yläpuolella lambda tuote on 2,176 8 K , helium-4 esiintyy normaalia värittömänä nesteenä kutsutaan heliumia I . Kuten muut kryogeeniset nesteet , se kiehuu kuumennettaessa ja supistuu, kun sen lämpötila lasketaan. Helium I on taitekerroin lähellä, että kaasu: 1026; mikä tekee sen pinnan niin vaikeasti havaittavaksi, että käytämme usein polystyreenivaahdon uimaria sen tason näkemiseen. Tämän väritön neste on erittäin alhainen viskositeetti ja tiheys on 0,125 = 1/8 , joka on vain neljäsosa arvon ennustettu klassisen fysiikan . Tämän ominaisuuden selittämiseksi on käytettävä kvanttimekaniikkaa, ja siksi nestemäistä heliumia sen eri muodoissa kutsutaan kvanttinesteeksi , mikä tarkoittaa, että kvanttimekaniikan vaikutukset, jotka ovat yleensä herkkiä vain mikroskooppisessa mittakaavassa, ilmenevät makroskooppisessa mittakaavassa, koska helium atomi 4 on bosoni . Tämä tulkitaan seurauksena siitä, että kiehumispiste on niin lähellä absoluuttista nollaa, että satunnaiset lämpöliikkeet eivät enää voi peittää atomien ominaisuuksia.
Superfluid
Nestemäisellä heliumilla lambda-pisteen alapuolella alkaa olla melko epätavallisia ominaisuuksia tilassa, jota kutsutaan helium II: ksi .
Siirtymässä helium I: stä helium II : een lambda-pisteessä, helium laajenee. Lämpötilan laskiessa helium II jatkaa laajenemistaan noin 1 K: een , missä se alkaa jälleen supistua kuten useimmat kappaleet.
Helium II voi virrata kapillaarien 10 -7 kohteeseen 10 -8 m ilman viskositeetti mitattavissa. Kuitenkin, kun mitataan viskositeetti kahden toisiinsa nähden pyörivän levyn välillä, löydämme viskositeetin, joka on verrattavissa kaasumaiseen heliumiin. Nykyinen teoria selittää tämän tosiasian käyttämällä kahden aineen malli on László Tisza (in) varten heliumin II . Tässä mallissa nestemäinen helium, lambda-pisteen alapuolella, koostuu perustilassa olevien heliumatomien ja viritettyjen atomien seoksesta, jotka käyttäytyvät enemmän kuin tavallinen neste.
Suihkulähde antaa esimerkin tästä teoriasta . Tässä kokeessa pystysuora putki, jonka yläpäässä on pieni suutin , upotetaan alaosastaan helium II -hauteeseen . Sen tukkii sintrattu levy , jonka läpi vain neste, jolla ei ole viskositeettia, voi kiertää. Jos lämmitämme putkea, esimerkiksi sytyttämällä se, muutamme supernesteosan tavalliseksi nesteeksi. Kahden nesteen tasapainon palauttamiseksi kylvyn kanssa superneste tunkeutuu sintratun tulpan läpi, ja tilavuuden säästämiseksi osa putken sisällöstä työntyy ylemmän suuttimen läpi muodostaen suihkun, joka voi olla keskeytä lopettamalla lämmitys.
Lämmönjohtavuus on heliumin II on suurempi kuin minkä tahansa muun tunnetun elin. Tämä estää helium II : n kiehumisen, koska kaikki lämmön sisäänmeno kulkee välittömästi pinnalle, jossa se yksinkertaisesti haihtuu kaasuksi. Tämä johtokyky on miljoona kertaa suurempi kuin helium I : llä ja useita satoja kertoja kuparilla. Tämä johtuu siitä, että lämmön johtuminen tapahtuu poikkeuksellisen kvanttimekanismin avulla. Useimmissa materiaaleissa, jotka ovat hyviä lämmönjohtimia, on valenssikaista vapaita elektroneja, joita käytetään lämmön johtamiseen. Helium II ei ole tällaista nauhaa vielä hyvin lämpöä johtavasta. Lämpövirta tottelee yhtälöt samanlainen kuin aallon yhtälöt äänen etenemistä ilmassa. Kun lämpöä tuodaan, se kulkee helium II: ssa 20 m s −1 1,8 K : n lämpötilassa . Näitä aaltoja kutsutaan toiseksi ääneksi .
Toisin kuin tavalliset nesteet, helium II ryömii pintoja pitkin, jopa ilmeisesti painovoimaa vastaan . Se pääsee sulkemattomasta astiasta indeksoimalla sivuille, ellei se kohdistu vähemmän kylmään paikkaan, jossa se haihtuu. Pinnasta riippumatta se liikkuu noin 30 nm : n kalvossa . Tätä elokuvaa kutsutaan Rollinin elokuvaksi sen fyysikon, Bernard V.Rollinin muistoksi. Tämän vaikutuksen ja helium II: n kyvyn läpi kulkea nopeasti pienten aukkojen seurauksena nestemäistä heliumia on vaikea rajoittaa. Ellei astiaa ole rakennettu älykkäästi, helium II kiipeää seinien läpi ja kulkee venttiilien läpi, kunnes se saavuttaa lämpimämmän alueen, jossa se haihtuu. Rollins-kalvoa pitkin etenevät aallot noudattavat samoja yhtälöitä kuin matalassa vedessä olevat aallot, mutta palauttava voima on van der Waalsin voima painovoiman sijasta. Nämä aallot tunnetaan kolmannena äänenä .
Kiinteä
Helium jähmettyy vain voimakkaiden paineiden vaikutuksesta. Tuloksena oleva käytännössä näkymätön ja väritön kiinteä aine on erittäin kokoonpuristuva; laboratoriopakkaus voi vähentää sen määrää yli 30%. Kun kuutioinen kimmokerroin on luokkaa 5 × 107 Pa , se on viisikymmentä kertaa kokoonpuristuvampi kuin vesi. Normaaleissa paineolosuhteissa, toisin kuin muut alkuaineet, helium ei kiinteyty ja pysyy nestemäisenä absoluuttiseen nollaan . Kiinteä helium vaatii vähintään 26 atm: n minimipaineen . Kiinteän heliumin erottaminen nestemäisestä heliumista on usein melko vaikeaa , koska niiden taitekertoimet ovat melkein identtisiä. Kiinteällä aineella on korkea piilevä lämpö (fuusiolämpö) ja kuusikulmainen kristallirakenne, kuten veden.
Kemialliset ominaisuudet
Kuten kaikilla jalokaasuilla , heliumilla on täysi valenssikerros, mikä tarkoittaa erittäin vähäistä kemiallista reaktiivisuutta. Koska sillä ei ole kykyä reagoida alikerroksiin, se on (yhdessä neonin kanssa ) vähiten reaktiivinen kaikista yksinkertaisista kappaleista .
Heliumia voidaan kuitenkin muodostaa epästabiileja yhdisteitä ( excimers ) volframi, jodia, fluoria, rikin ja fosforin plasman vaiheessa , mukaan vastuuvapauden tai muuten. He Ne , Hg He 10 , W He 2 ja molekyyli-ionit He 2 + , He 2 ++ , HeH + , He D + luotiin tällä tavalla. Tämä tekniikka on mahdollistanut myös neutraalin molekyylin He 2 , jolla on enemmän kaistajärjestelmiä, ja HgHe: n tuotannon, jonka koheesio näyttää tukeutuvan vain polarisaatiovoimiin . Teoriassa muut komponentit, kuten heliumfluorihydridi (HHe F ), ovat myös mahdollisia. Vuonna 2013, litium heliide Lihe muodostettiin kaasumaisessa tilassa laserablaation hyvin alhaisessa lämpötilassa ( 1 kohteeseen 5 K ).
Ensimmäinen osoittautunut vakaa helium yhdisteet ovat endohedral fullereeni kompleksit , kuten hän @ C 60 , jossa heliumatomin loukkuun häkki C 60 fullereeni . Sen jälkeen, se on osoitettu, että hyvin korkeassa paineessa (yli 113 GPa ) on mahdollista muodostaa stabiili yhdiste, heliumia ja natrium, Na 2 hän . Tällaisia molekyylejä voi löytyä myös korkeapaineisilta jättiläisplaneetoilta, kuten Jupiter ja Saturnus .
Maapallon sisältä tulee ulos ( laavoissa ja tulivuorikaasuissa ) heliumia , jossa on runsaasti heliumia 3 , jonka uskotaan olevan alkukantaista (ts. Hankittu maapallon muodostumisen aikana , lähes 4,6 miljardia vuotta sitten ). Jos se olisi kaasumaisessa tilassa tai liuennut alemman vaipan mineraaleihin , sillä olisi ollut riittävästi aikaa degasoida melkein kokonaan, kun otetaan huomioon sen haihtuvuus ja lämpötilat maan sisällä. Siksi se on varastoitava stabiilina mineraaleina alemman vaipan olosuhteissa , mutta mitään ei tunneta. 2018 laskenta vapaa entalpia tuhat hypoteettinen mutta mahdollisia heliumia yhdisteiden ennustetaan yksi (ja vain yksi) vapaa entalpia yhdiste tarpeeksi pieni ansa helium vaipan sijasta jättää. Ilmainen, rauta dioksidi ja heliumin FeO 2 Hän.
Biologiset ominaisuudet
Normaaleissa olosuhteissa neutraali helium on myrkytöntä, sillä ei ole biologista merkitystä ja sitä esiintyy pieninä määrinä ihmisen veressä. Jos hengitetään tarpeeksi niin, että normaaliin hengitykseen tarvittava happi siirtyy, tukehtuminen on mahdollista.
Hengitys
| Äänitiedosto | |
| Teksti luettu heliumilla | |
| Käytä tarvittaessa selaimen edellistä sivunäppäintä kuulemistilaisuuden lopussa . (en) Helium on väritön, hajuton, mauton, myrkytön, inertti monatominen kemiallinen alkuaine, joka johtaa jaksollisen taulukon jalokaasusarjaa ja jonka atomiluku on 2. Sen kiehumis- ja sulamispisteet ovat alhaisimmat alkuaineiden joukossa ja se esiintyy vain kaasuna paitsi ääriolosuhteissa . | |
| Onko sinulla vaikeuksia käyttää näitä medioita? | |
|---|---|
Heliumia hengittäneen henkilön ääni muuttaa väliaikaisesti sävyä kohti korkeaa harmonista - helium on kolme kertaa vähemmän tiheä kuin ilma, äänen nopeus kasvaa siten - ja kun perustaajuudella d 'kaasulla täytetty ontelo on verrannollinen nopeuteen äänen, hengitysteitse heliumin vastaavat lisäystä , että resonanssitaajuudet on phonatory laitteen , jotka moduloivat perustaajuus antama äänihuulten . Päinvastainen vaikutus, sävyn alentaminen, voidaan saada hengittämällä tiheämpää kaasua, kuten rikkiheksafluoridia .
Puhtaan heliumin inhalaatio pieninä annoksina on yleensä turvallista, koska se on inertti kaasu . Kaupassa myytävän heliumin, kuten ilmapallojen täyttämiseen käytetyn, käyttö voi kuitenkin olla vaarallista, koska se voi sisältää monia epäpuhtauksia, jälkiä muista kaasuista tai voiteluöljyn aerosoleista.
Heliumin ylimääräisen hengittäminen voi olla vaarallista, koska helium on yksinkertaisesti tukehtuva aine , joka korvaa normaaliin hengitykseen tarvittavan hapen. Puhtaan heliumin hengittäminen aiheuttaa tukehtumisen muutamassa minuutissa. Heliumin hengittäminen suoraan paineistetuista sylintereistä on erittäin vaarallista korkean virtausnopeuden vuoksi, joka voi tuottaa barotrauman, joka repii keuhkokudosta ja voi olla hengenvaarallinen. Tämä onnettomuus on kuitenkin melko harvinaista, koska Yhdysvalloissa tapahtui vain kaksi kuolemaa vuosina 2000–2004.
Korkeassa paineessa (yli 20 atm tai 2 MPa ) heliumin ja dioksigeenin ( heliox ) seos voi johtaa korkean paineen hermo-oireyhtymään , eräänlaiseen anestesia-aineeseen. Lisäämällä seokseen vähän typpeä ongelma voidaan välttää. Siitä huolimatta vedenalaisessa sukelluksessa korkean paineen hermo-oireyhtymää voidaan torjua vain lisäämällä vetyä , typen lisääminen on erittäin huumaavaa heti, kun kokonaispaine saavuttaa 5 baaria.
Terapeuttinen käyttö
Heliumia annetaan seoksissa, jotka sisältävät vähintään 20% dioksidia potilaille, joilla on ylemmän tai alemman hengitysteiden tukkeuma. Heliumin matala viskositeetti mahdollistaa siten hengitystyön vähentämisen.
turvallisuus
Kryogeenisen heliumin turvatoimenpiteet ovat samanlaisia kuin nestetypelle vaaditut ; sen erittäin matala lämpötila voi aiheuttaa palovammoja .
Suuren määrän hengittäminen yhdellä otoksella aiheuttaa vähäisen tukehtumisen , mikä johtaa lyhyeen mutta vaaralliseen tajunnan menetykseen . Paineistettua heliumia hengittävillä ihmisillä on myös joitain tapauksia aivojen emboliasta tai vakavista keuhko-ongelmista.
Lisäksi nestefaasin ja kaasufaasin välinen laajenemisnopeus on sellainen, että se voi aiheuttaa räjähdyksiä nopean höyrystymisen yhteydessä, ellei paineenrajoituslaitetta ole asennettu.
Säiliöt helium kaasun 5 - 10 K on myös käsiteltävä, jos ne sisältävät nestemäisen heliumin, koska suuri ja nopea lämpölaajeneminen, joka tapahtuu, kun heliumin alle 10 K lisätään. Huoneenlämpötilassa.
Käyttää
Korkeasta hinnastaan huolimatta heliumia käytetään moniin käyttötarkoituksiin, jotka edellyttävät joitain sen ainutlaatuisista ominaisuuksista, kuten matalaa kiehumispistettä , matalaa tiheyttä , matalaa liukoisuutta , korkeaa lämmönjohtavuutta tai sen kemiallisesti ja biologisesti inerttiä luonnetta . Se löytyy kaupallisesti nestemäisessä tai kaasumaisessa muodossa. Nestemäisessä muodossa on pieniä dewars- säiliöitä , joihin mahtuu 1000 l heliumia, tai suurissa ISO-säiliöissä, joiden nimellistilavuus on jopa 40 000 l . Kaasumaisessa muodossa pieniä määriä heliumia toimitetaan korkeissa paine- sylintereissä, joissa on enintään 8,5 m 3 vakiona, kun taas suuria määriä toimitetaan paineistetuissa säiliöaluksissa, joiden kapasiteetti voi olla jopa 5000 m 3 .
Teollinen
Heliumia käytetään inertisyytensä, korkean lämmönjohtavuutensa , läpinäkyvyytensä neutronien suhteen ja koska se ei muodosta radioaktiivisia isotooppeja reaktoreissa, lämmönsiirtonesteenä tietyissä lämpökaasulla jäähdytetyissä ydinreaktoreissa .
Heliumia käytetään suojakaasussa aikana kasvu yksikiteisen piin valmistamiseksi integroitujen piirien ja optiset kuidut , tuotantoa varten titaanin ja zirkoniumin ja kaasukromatografialla , koska se on inertti.
Kemiallisen inertiansa, ihanteellisten termodynaamisten ja lämpöominaisuuksiensa , korkean äänenopeuden ja suuren Laplace-kertoimen ansiosta se on hyödyllinen myös yliäänen tuulitunneleissa tai ohimeneviä ilmiöitä tutkivissa asennuksissa.
Näiden samojen ominaisuuksien ansiosta sitä voidaan käyttää suljetuissa kiintolevyissä niiden kapasiteetin lisäämiseksi. Koska mikään tiiviste ei ole täydellinen, näillä levyillä on ilmaisin, joka ilmoittaa levylle vaarallisesta heliumin menetyksestä ajan myötä.
Helium sekoitettuna raskaampaan kaasuun, kuten ksenoniin, on hyödyllinen lämpöakustisessa jäähdytyksessä , koska lämpökapasiteetti on suuri ja alhainen Prandtl-luku . Heliumin kemiallisella inertialla on ympäristöetuja verrattuna muihin jäähdytysjärjestelmiin, jotka vaikuttavat otsonireikään tai ilmaston lämpenemiseen .
Koska heliumia diffundoituu kiintoaineiden läpi kolme kertaa nopeammin kuin ilmaa, vuotoja havaitaan ultrakorkeassa alipainelaitteessa tai korkeapainesäiliössä.
Sitä käytetään myös elintarvikkeiden kanssa (elintarvikelisäaine, jonka Euroopan unioni on hyväksynyt viitteellä E939 ) pakkausten sulkemisen tarkastamiseksi (katso luettelo elintarvikelisäaineista ).
Tutkijat
Heliumin käyttö vähentää poikkeuksellisen matalan taitekertoimen vuoksi tiettyjen teleskooppien tai lasien linssien välisen tilan lämpötilan vaihteluista johtuvia vääristymiä . Tätä menetelmää käytetään erityisesti aurinkoteleskooppeihin, joissa lämpötilan vaihtelut ovat merkittäviä, mutta joissa ilmakehän ja tyhjiön välistä paine-eroa tukeva kotelo olisi liian raskas.
Uraania ja toriumia sisältävien kivien ja mineraalien ikä voidaan arvioida mittaamalla niiden heliumpitoisuus prosessilla, jota kutsutaan helium dating -menetelmäksi .
Nestemäistä heliumia käytetään myös tiettyjen metallien jäähdyttämiseen suprajohtavuuden edellyttämiin erittäin mataliin lämpötiloihin , esimerkiksi suprajohtaviin magneetteihin, joita käytetään erityisesti magneettikuvausilmaisimiin . LHC on CERNin käyttää 120 t nestemäisen heliumin lämpötilan ylläpitämiseksi magneetit 1,9 K . Yleisemmin, alhaisen lämpötilan heliumia käytetään kryogeniikka .
Kaupallinen ja vapaa-aika
Koska sen alhainen liukoisuus hermokudoksen , heliumia seokset kuten trimix , helioxilla ja heliumia käytetään varten syväsukelluksen vähentää vaikutuksia typpinarkoosin . Yli 150 m: n syvyydessä pieniä määriä vetyä lisätään helium-dioksidihapposeokseen korkeapaineisen hermo-oireyhtymän torjumiseksi .
Näissä syvyydessä heliumin matala tiheys vähentää huomattavasti hengitystoimintaa.
He-Ne laserit on erilaisia sovelluksia, erityisesti lukijoita viivakoodi .
Ilmalaivat, ilmapallot ja raketit
Koska helium on ilmaa kevyempi, sitä voidaan käyttää ilmalaivojen ja vapaiden tai kiinnitettyjen ilmapallojen täyttämiseen. Vaikka vedyllä on noin 7% enemmän kantokykyä, heliumin etuna on palamaton (ja jopa palonestoaine).
Ilmakehän etsintä, erityisesti meteorologiaa varten, tapahtuu ilmapalloilla, suurimmaksi osaksi aikaa heliumilla.
Rakettitekniikassa heliumia käytetään siirtymäaineena polttoaineen ja hapettimen hallitsemiseksi mikropainesäiliöissä paineistuksella ja vedyn ja hapen seoksen varmistamiseksi, joka syöttää propulsiosuuttimia. Sitä käytetään myös näiden aineiden puhdistamiseen maalaitteista ennen laukaisua ja nestejetyksen esijäähdyttämiseen avaruusajoneuvoista . Esimerkiksi Saturn V -raketti kuluttaa lentoon noin 370 000 m 3 heliumia.
Heliumin resurssit ja puhdistus
Luonnollinen runsaus
Helium on tunnetun maailmankaikkeuden toiseksi yleisin alkuaine vedyn jälkeen ja muodostaa 23% sen barioonimassasta . Suurin osa heliumista muodostui alkeellisella nukleosynteesillä muutamassa minuutissa Suuresta Bangista . Siksi sen runsauden mittaaminen auttaa kiinnittämään tietyt kosmologisten mallien parametrit. Tähtien koko suurimman osan olemassaolosta se muodostuu vedyn ydinfuusion avulla. Elämänsä lopussa tähdet käyttävät heliumia raaka-aineena raskaampien alkuaineiden luomiseen paljon nopeammilla, jopa räjähtävillä prosesseilla. Viime kädessä helium maailmankaikkeudessa tulee vain hyvin pienestä osasta tähtiä.
Maapallon ilmakehässä heliumin pitoisuus on 5,2 × 10-6 tilavuusprosenttia. Tämä alhainen pitoisuus on melko vakaana, koska tasapaino jatkuvaa tuotantoa heliumin kiviä ja paeta tilaan , jonka eri mekanismeja . Maan heterosfäärissä osa ylemmästä ilmakehästä, helium ja muut kevyet kaasut ovat yleisimpiä ainesosia.
Lähes kaikki maapallon helium tulee α-radioaktiivisuudesta . Se esiintyy pääasiassa uraanin ja toriumin yhdisteet , mukaan lukien pitchblende , karoniittimalmia, ja monatsiitti , koska ne lähettävät α hiukkasia , jotka ovat ytimet ionisoituneen heliumin Hän 2+ , joka välittömästi Neutraloidaan elektroneja. On arvioitu, että litosfäärissä tuotetaan vuosittain 3000 tonnia heliumia . Maankuoressa heliumin pitoisuus on 8 × 10 −6 tilavuusprosenttia. Merivedessä se on vain 4 × 10 −12 . Mineraalivettä , tulivuorikaasuja ja meteorirautaa on myös pieniä määriä . Koska helium on vangittu maakaasun tavoin läpäisemättömillä kalliokerroksilla, korkeimmat heliumin pitoisuudet löytyvät maakaasukentistä, joista suurin osa kaupallisesta heliumista uutetaan. Sen tilavuuspitoisuus suhteessa maakaasuun vaihtelee muutamasta miljoonasosasta 7 prosentin pitoisuuteen, joka tunnistettiin San Juanin piirikunnassa New Mexico .
Vuonna 2016 "Helium" -niminen yritys ilmoitti tunnistaneensa tämän elementin kolme mahdollista valtavaa kenttää Tansaniassa , riittävän suuret - sen mukaan - toimittamaan maailmaa useiden vuosikymmenien ajan, ja tästä syystä se etsii 40 miljoonaa dollaria investointi poraamisen kokeilemiseksi Tansaniassa vuonna 2017. Jotkut asiantuntijat uskovat kuitenkin, että tämän talletuksen hyödyntäminen ei olisi kannattavaa pitkään aikaan, koska heidän mukaansa maailmanmarkkinat ovat viime aikoina alkaneet ylituotantona taloudellisemman käytön ja suurimmat markkinat Yhdysvalloissa , Qatarissa ja Venäjällä .
Uuttaminen ja puhdistaminen
Suuressa määrin helium uutetaan jakotislauksella maakaasusta, joka voi sisältää jopa 7%. Koska heliumin kiehumispiste on alhaisempi kuin millään muulla kappaleella, matalaa lämpötilaa ja korkeaa painetta käytetään melkein kaikkien muiden kaasujen (pääasiassa ditypen ja metaanin ) nesteytykseen . Tuloksena saatu raaka helium puhdistetaan sitten altistamalla alemmille ja matalammille lämpötiloille, jolloin saostuu käytännössä kaikki typpi ja muut jäljellä olevat kaasut kaasuseoksesta. Lopuksi aktiivihiiltä käytetään lopulliseen puhdistusvaiheeseen, jolloin saadaan heliumia, jonka laatu on 99,995%. A-luokan heliumin tärkein epäpuhtaus on neon . Puhdistuksen loppuunsaattamiseksi suurin osa tuotetusta heliumista nesteytetään kryogeenisellä prosessilla. Nesteytys on välttämätöntä nestemäistä heliumia käyttävissä sovelluksissa, ja lisäksi heliumin toimittajat voivat vähentää etäkuljetusten kustannuksia, koska suurempien nestemäisten heliumsäiliöiden kapasiteetti on vähintään viisi kertaa suurempi kuin suurempien perävaunujen, jotka kuljettavat paineistettuja heliumkaasupulloja a .
Vuonna 2005 noin 160 miljoonaa kuutiometriä heliumia otettiin maakaasusta tai otettiin varastoista. Noin 83% Yhdysvalloista , 11% Algeriasta ja loput pääosin Venäjältä ja Puolasta . Yhdysvalloissa suurin osa heliumista uutetaan maakaasusta Hugotonissa ja sen lähialueilla Kansasissa, Oklahomassa ja Teksasissa.
Toinen menetelmä heliumin tuottamiseksi ja puhdistamiseksi on raaka maakaasun diffuusio puoliläpäisevien kalvojen tai muiden esteiden läpi.
Helium on mahdollista syntetisoida pommittamalla litiumia tai booria korkean energian protoneilla, mutta tämä ei ole taloudellisesti kannattava tuotantomenetelmä.
Historia
Löytö
Ensimmäinen havainto heliumista havaitaan 18. elokuuta 1868Kirkkaan keltaisena juovana aallonpituudella on 587,49 nm , että spektri on Kromosfäärin että auringon . Tämä linja on havaittu Ranskan tähtitieteilijä Jules Janssen aikana yhteensä Eclipse on Guntur (Intia) . Aluksi tämän linjan uskotaan olevan natriumia . 20. lokakuutasamana vuonna, Englanti tähtitieteilijä Norman Lockyer havaittu keltainen viiva auringon spektrin, jota hän kutsui Fraunhofer-linja D 3 , koska se on lähellä tunnettu linjat D 1 ja D 2 natriumia. Hän päättelee, että sen aiheuttaa maapallolla tuntematon aurinkoelementti. Lockyer ja englantilainen kemisti Edward Frankland nimeävät tämän elementin kreikkalaisen Sun-sanan ἥλιος ( helios ) jälkeen.
Vuonna 1882 Luigi Palmieri onnistui ensimmäistä kertaa osoittamaan heliumin läsnäolon maapallolla suorittamalla Vesuviuksen laavan spektrianalyysi .
26. maaliskuuta 1895British kemisti Sir William Ramsay eristää helium maapallolla käsittelemällä kleveite (erilaisia pitchblende , joka sisältää vähintään 10% harvinaisten maametallien ) kanssa mineraali- happojen . Ramsay etsii argonia , mutta erotettuaan typen ja hapen rikkihapon vapauttamasta kaasusta hän huomasi spektroskoopissa kirkkaan keltaisen viivan , joka osui samaan aikaan auringon spektrissä havaitun D3- linjan kanssa.
Lockyer ja brittiläinen fyysikko William Crookes ovat tunnistaneet nämä näytteet heliumiksi . Riippumatta, se on eristetty cleveiitti saman vuoden kemistit Per Theodor Cleve ja Abraham Langlet (in) on Uppsala , joka kertyy tarpeeksi kaasua voi tarkasti määrittää sen atomipaino .
Myös amerikkalainen geokemisti William Francis Hillebrand oli eristänyt heliumin muutama vuosi ennen Ramsayn löytöä havaitsemalla epätavallisia spektriviivoja tutkittaessa uaniniittinäytettä. Mutta Hillebrand määrittelee nämä linjat typpityyppiseksi. Hänen onnittelukirjeensä Ramsaylle esittelee mielenkiintoisen löytötieteen ja lähes löydettävyyden tieteessä.
Vuonna 1907 Ernest Rutherford ja Thomas Royds osoittivat, että α-hiukkaset ovat heliumin ytimiä , antamalla hiukkasten päästä sisään putken ohuesta lasiikkunasta, josta ne evakuoivat, ja luomalla sitten putkeen purkautumisen uuden kaasun spektrin tutkimiseen. se. Hollantilainen fyysikko Heike Kamerlingh Onnes nesteytti heliumia ensimmäistä kertaa vuonna 1908 jäähdyttämällä kaasua alle 1 K . Hän yrittää jähmettyä sitä laskemalla lämpötilaa edelleen, mutta epäonnistuu, koska heliumilla ei ole kolmoispistettä . Se on Onnesin opiskelija Willem Hendrik Keesom , joka onnistuu jähmettymään 1 cm 3 heliumin paineessa vuonna 1926.
Vuonna 1938 Neuvostoliiton fyysikko Pyotr Leonidovich Kapitsa huomasi, että helium-4: llä ei ollut juurikaan viskositeettia lähellä absoluuttista nollaa olevissa lämpötiloissa. Vuonna 1972 amerikkalaiset fyysikot Douglas D. Osheroff , David M. Lee ja Robert C. Richardson havaitsivat saman ilmiön helium 3: ssa , mutta lämpötilassa, joka oli paljon lähempänä absoluuttista nollaa . Helium 3: n ilmiö tulkitaan atomiparien, jotka ovat fermioneja , muodostumiseksi bosonien muodostamiseksi analogisesti Cooperin elektroniparien kanssa suprajohtavuuden perusteella .
Tuotanto ja käyttö
Öljynporauksen jälkeen vuonna 1903 Dexterissä , Kansasissa , tuotettu kaasusuihku oli palamaton. Erasmus Haworth (in) , geologi ja Kansasin osavaltion keränneet näytteitä tuotetun kaasun ja toi Kansasin yliopistossa , Lawrence . Apteekkien Hamilton Cadyn (en) ja David McFarlandin avulla todettiin, että kaasu tilavuusprosentteina, 72% typpeä, 15% metaania (palava prosenttiosuus vain enemmän happea) ja 12% tunnistamatonta kaasua. Lisäanalyysi osoittaa Cadylle ja McFarlandille, että 1,84% kaasunäytteestä on heliumia. Tämä osoittaa, että maapallon maailmanlaajuisesta niukkuudesta huolimatta helium on keskittynyt suurina määrinä Amerikan suurten tasangon alle ja saatavissa tuotantoon maakaasun hyödyntämisen sivutuotteena. Suurimmat heliumivarannot ovat Hugoton-kentällä ja lähialueilla Kansasin lounaisosassa, jatkuen Texasiin ja Oklahomaan.
Tämän ansiosta Yhdysvalloista tuli maailman johtava heliumin tuottaja. Sir Richard Threlfallin (vuonna) ehdotuksesta Yhdysvaltain laivasto tukee kolmea pientä kokeellista heliumin tuotantolaitosta ensimmäisen maailmansodan aikana . Tavoitteena on toimittaa kiinnitetyt sulkupallot tällä palamattomalla, ilmaa kevyemmällä kaasulla. Tällä ohjelmalla tuotetaan yhteensä 5700 m 3 92% heliumia, vaikka aiemmin sitä on tuotettu alle 100 l . Osa tästä kaasua käytetään maailman ensimmäinen heliumilla täytetyt ilmalaivalla, Yhdysvaltain laivaston C-7, vihittiin neitsytmatkalleen alkaen Hampton Roads vuonna Virginiassa ja Bolling Field in Washington on1. st joulukuu 1921.
Vaikka matalan lämpötilan kaasun nesteytysprosessia ei kehitetty riittävän ajoissa, jotta sillä olisi merkittävä rooli ensimmäisen maailmansodan aikana, tuotantoa jatketaan. Heliumia käytetään ensisijaisesti ilmapallojen täyttämiseen . Tämä käyttö lisää kysyntää toisen maailmansodan aikana , samoin kuin kaarihitsauksen kysyntä .
Helium massaspektrometri on myös elintärkeää Manhattanin atomipommi hanke.
Yhdysvaltain hallitus loi vuonna 1925 National helium Reserve Amarillo , Texas , jonka tavoitteena on toimittaa aerostats, sotilaita sodan aikana, ja siviilien rauhan aikana. Yhdysvaltojen Saksan vastaiseen sotasaartoon johtuen heliumin saanti siellä oli rajoitettua ja Hindenburg oli täytettävä vedellä, mikä aiheutti katastrofaalisia seurauksia sen palamisen yhteydessä. Heliumin kulutus toisen maailmansodan jälkeen laski, mutta varantoa lisättiin 1950-luvulla nestemäisen heliumin saannin varmistamiseksi rakettien laukaisua varten avaruuskilpailun ja kylmän sodan aikana . Vuonna 1965 heliumin kulutus Yhdysvalloissa ylitti kahdeksan kertaa sodan aikana saavutetun enimmäismäärän.
Heliumin lain muutosten jälkeen vuonna 1960 ( julkisoikeus 86-777 ) Yhdysvaltain kaivosvirasto perusti viisi yksityistä tehdasta heliumin saamiseksi maakaasusta. Tätä heliumin säilyttämisohjelmaa varten puhemiehistö rakentaa 684 km: n putkilinjan Bushtonista Kansasista Cliffsideen, lähellä Amarilloa, osittain köyhtyneelle kentälle. Näin toimitettu helium-dinityppiseos ruiskutetaan ja varastoidaan tarpeeseen asti, jolloin se uutetaan ja puhdistetaan.
Vuonna 1995 kerättiin miljardi kuutiometriä kaasua, mutta varalla on 1,4 miljardia Yhdysvaltain dollaria velkaa, mikä johtaa Yhdysvaltojen kongressin toimintaan asteittain vuonna 1996. Seurannut Helium yksityistäminen Act of 1996 (Public Law 104-273) ohjaa Yhdysvaltain sisäministeriö aloittamaan tyhjennyksen varauksesta vuonna 2005.
Vuosina 1930–1945 tuotettu helium oli noin 98,3% puhdasta (~ 2% typpeä), mikä oli ihanteellinen aerostaateille. Vuonna 1945 tuotettiin pieni määrä 99,9% heliumia kaarihitsaukseen. Jo vuonna 1949 kaupallisia määriä 99,995% A-luokan heliumia oli saatavilla.
Useiden vuosien ajan Yhdysvallat tuotti yli 90% maailman kaupallisesti saatavasta heliumista, ja uuttolaitokset Kanadassa, Puolassa, Venäjällä ja muissa maissa tuottivat loput. Tällä nopeudella tutkimuksen (elokuu 2010), Yhdysvaltain varannot loppuvat ennen vuotta 2040 (lähes kolmasosa maailman tarpeista toimittaa Yhdysvallat, jonka maailmanlaajuinen tuotantokapasiteetti on noin 142 miljoonaa kuutiometriä (vuonna 2010), kun taas kulutus oli 180 miljoonaa kuutiometriä ja että helium näyttää olevan "välttämätöntä useimmissa sovelluksissa" ).
-1990-
luvun puolivälissä uusi tehdas alkoi tuottaa Arzewissa , Algeriassa . 1,7 × 10 7 m 3 vuodessa se voi kattaa koko Euroopan kysynnän eli noin 16% maailman tuotannosta. Samaan aikaan Yhdysvaltojen kulutus ylitti 15 000 tonnia vuonna 2000. Vuosina 2004–2006 rakennettiin kaksi uutta laitosta, yksi Ras Laffaniin ( Qatar ), joka tuotti 9,2 tonnia nestemäistä heliumia päivässä, eli 1,88 × 10 7 m 3 vuodessa, ja toinen Skikdassa (Algeria). Algeriasta tuli nopeasti toiseksi suurin heliumin tuottaja. Tänä aikana heliumin kulutus ja tuotantokustannukset kasvoivat. Vuosien 2002 ja 2007 välillä heliumin hinnat kaksinkertaistuivat, ja pelkästään vuonna 2008 suuret toimittajat korottivat hintojaan noin 50 prosenttia . Tämä liittyy heliumin erittäin vähäiseen tuotantoon ja kulutukseen, mikä vaikeuttaa niiden vastaamista, koska harvat tuottajat haluavat sijoittaa näille markkinarakoille .
Robert Richardson ( fysiikan Nobel-palkinto ) vuonna 2010 varoitti kansainvälistä yhteisöä puuteriskistä, väittäen hintojen nousua, jotta heijastuisi tämän elementin niukkuuteen ja tuhlata sitä vähemmän .
Yritys 45-8 Energy, jonka pääkonttori sijaitsee Metzissä , jätti lokakuussa 2019 yksinoikeuden tutkimuksen heliumille Nièvren departementin lounaaseen , Ranskaan. Prefektuurin vastauksen odotetaan syyskuussa 2020.
Huomautuksia ja viitteitä
- (fr) Tämä artikkeli on osittain tai kokonaan otettu Wikipedian englanninkielisestä artikkelista " Helium " ( katso kirjoittajaluettelo ) .
- Bose-Einstein- tilastot ja Fermi-Dirac-tilastot .
- Katso YouTube-leike, jonka on kirjoittanut ucilowtemp .
- (en) David R. Lide, CRC: n kemian ja fysiikan käsikirja , CRC Press Inc,2009, 90 th ed. , 2804 Sivumäärä , Kovakantinen ( ISBN 978-1-420-09084-0 )
- (in) Beatriz Cordero Verónica Gómez, Ana E. Platero-Prats, Marc Revés Jorge Echeverría, Eduard Cremades, Flavia ja Santiago Barragan Alvarez , " Covalent radius revisited " , Dalton Transactions ,2008, s. 2832 - 2838 ( DOI 10,1039 / b801115j )
- "Atomien ja atomien ionien ionisointienergiat", julkaisussa CRC Handbook of Chemistry and Physics, 91. painos (Internet-versio 2011), WM Haynes, toim., CRC Press / Taylor ja Francis, Boca Raton, FL, P. 10-203
- (en) Robert H. Perry ja Donald W. Green , Perry's Chemical Engineers 'Handbook , USA, McGraw-Hill,1997, 7 th ed. , 2400 Sivumäärä ( ISBN 0-07-049841-5 ) , s. 2-50
- "Helium" vaarallisten aineiden tietopankissa , käyty 1.5.2010
- Chemical Abstracts -tietokanta kysyttiin SciFinder Webin kautta 15. joulukuuta 2009 ( hakutulokset )
- Sigma-Aldrich- arkki yhdistettä Helium ≥99.995% , kuultu 17. elokuuta 2018.
- " Helium " kemiallisten tuotteiden tietokannassa Reptox of the CSST (Quebec-organisaatio, joka vastaa työturvallisuudesta ja työturvallisuudesta), käyty 25. huhtikuuta 2009
- Paul Depovere, Elementtien jaksollinen taulukko . Maailmankaikkeuden perusihme , De Boeck Supérieur ,2002, s. 103.
-
(en) Eric Hand, ” Massiivisia heliumikenttiä löytyy Tansanian rift-alueelta ” , Science , voi. 353, n o 6295,8. heinäkuuta 2016, s. 109-110 ( DOI 10.1126 / science.353.6295.109 , luettu verkossa
 , käytetty 11. heinäkuuta 2016 ).
, käytetty 11. heinäkuuta 2016 ).
- Audrey Chauvet, " Maailman heliumivarannot tyhjentyvät " , www.20minutes.fr ,30. elokuuta 2010(käytetty 22. kesäkuuta 2019 ) .
- (en) John Emsley , Luonnon rakennuspalikat: AZ-opas elementteihin , Oxford New York, Oxford University Press ,2001, 538 Sivumäärä ( ISBN 978-0-19-850340-8 ja 978-0-198-50341-5 , OCLC 248877093 , luettu verkossa ) , s. 175–179.
-
(in) Achim Weiss, " Elements of menneisyyden: alkuräjähdyksen ydinsynteesi ja havainnointi " , Max Planck Institute for Gravitational Physics (näytetty 23 kesäkuu 2009 ) ;.
(en) A. Coc et ai. , " Päivitetty Big Bang Nucleosynthesis WMAP -havaintojen ja valoelementtien runsauden edessä " , The Astrophysical Journal , voi. 600,2004, s. 544 ( DOI 10.1086 / 380121 ). -
(sisään) Don L. Anderson, GR Foulger Anders Meibom, " Helium Fundamentals " , MantlePlumes.orgMantlePlumes.org,
2006(käytetty 20. heinäkuuta 2008 ) .
Vain
tiivistelmä. Tuote tarjotaan myyntiin. - (in) Aaron Novick , " puoliintumisaika Tritium " , Physical Review , vol. 72, 1947, s. 972 ( DOI 10.1103 / PhysRev.72.972.2 , lue verkossa )Pääsy on rajoitettu PROLA-tilaajille.
- (in) GN Zastenker ja E. Salerno, F. Buehler, P. Bochsler, M. Bassi, YN Agafonov, NA Eismont, VV Khrapchenkov, H. Busemann , " Suoriin mittauksiin perustuva tähtienvälisen neutraalin heliumin isotooppinen koostumus ja runsaasti " , Astrophysics , voi. 45, n ° 2Huhtikuu 2002, s. 131–142 ( DOI 10.1023 / A: 1016057812964 , lue verkossa ) Vain tiivistelmä . Tuote tarjotaan myyntiin.
- (in) " Helium-3: n kuun kaivostoiminta " , Wisconsin-Madisonin yliopiston fuusioteknologian instituutti, 2007(käytetty 9. heinäkuuta 2008 ) .
- (en) EN Slyuta AM Abdrakhimov EM Galimov, " Arvio helium-3 todennäköisiä varantoja Kuun regolith vuonna Lunar ja Planetary Science XXXVIII " [PDF] ,2007(käytetty 23. kesäkuuta 2009 ) .
- (sisään) Eric R. Hedman , " Kiehtova hetki Gerald Kulcinskin kanssa " , The Space Review ,16. tammikuuta 2006( lue verkossa ).
- (sisään) Peter Häussinger1 Reinhard Glatthaar2 Wilhelm Rhode3 Helmut Kick4 Christian Benkmann5 Josef Weber6 Hans-Jörg Wunschel7 Viktor Stenke8 Edith Leicht9 Hermann Stenger10, Noble kaasut , Wiley-VCH Verlag GmbH & Co , et ai. " Ullmannin teollisen kemian tietosanakirja ",15. maaliskuuta 2001( online-esitys ).
- (en) LW Brandt, (Clifford A. Hampel, toim.) The Encyclopedia of the Chemical Elements , Reinhold Book Corporation , New York, 1968, luku. "Helium" , s. 256–268 .
- (in) Ray F. Weiss , " liukoisuus heliumin ja neon veden ja meriveden " , J. Chem. Eng. Data , voi. 16, n ° 21971, s. 235–241 ( DOI 10.1021 / je60049a019 )Ensimmäinen sivu.
- (in) Jack A. Stone ja Alois Stejskal , " käyttäminen helium standardina taitekerroin " , Metrologia , Voi. 41,2004, s. 189–197 ( DOI 10.1088 / 0026-1394 / 41/3/012 ) Tiivistelmä .
- (in) The Encyclopedia of the Chemical Elements , op. cit. , s. 261 .
- (in) F. Buhler ja WI Axford, HJA Chivers, K. Martin , " Helium-isotoopit vuoden aurorassa " , J. Geophys. Res. , voi. 81, n o 1,1976, s. 111–115 ( DOI 10.1029 / JA081i001p00111 ) Tiivistelmä .
- (en) The Encyclopedia of the Chemical Elements , op. cit. s. 262 .
- (in) PC Hohenberg ja PC Martin , " Superfluid Helium Microscopic Theory of superfluid Helium " , Annals of Physics , voi. 281, n luu 1-2,Lokakuu 2000, s. 636–705 ( DOI 10.1006 / aphy.2000.6019 ) Tiivistelmä . Artikkeli on saatavana ScienceDirect-tilaajille.
- (sisään) The Encyclopedia of the Chemical Elements , op. cit. , s. 263 .
- (in) HA Fairbank ja CT Lane , " Rollin Film Rates in Liquid Helium " , Physical Review , voi. 76, n o 8,Lokakuu 1949, s. 1209–1211 ( DOI 10.1103 / PhysRev.76.1209 ) Tiivistelmä . Tuote tarjotaan myyntiin.
- (sisään) BV Rollin ja F. Simon , " Nestemäisen helium II: n" elokuva "-ilmiöstä " , Physica , voi. 6, n o 21939, s. 219–230 ( DOI 10.1016 / S0031-8914 (39) 80013-1 ) Tiivistelmä . Artikkeli on saatavana ScienceDirect-tilaajille.
- (in) Fred Ellis, " kolmas ääni " , Wesleyan Quantum Nesteet Laboratory ,Syyskuu 2005(käytetty 23. kesäkuuta 2009 ) .
- (sisään) D. Bergman , " Hydrodynamiikka ja kolmas ohut ääni He II -elokuvissa " , Physical Review , voi. 188, n o 1,Lokakuu 1949, s. 370–384 ( DOI 10.1103 / PhysRev.188.370 ) Tiivistelmä . Saatavana PROLA-tilaajille tai myytävänä.
- (en) " Jaksolliset taulukot: helium " (käytetty 23. kesäkuuta 2009 ) .
- (in) Naima Tariq Nada Taisan, Vijay Singh ja Jonathan Weinstein, " Spektroskooppiset havaitseminen Lihe Molecule " , Physical Review Letters , vol. 110, n ° 15,8. huhtikuuta 2013, s. 153201 ( PMID 25167262 , DOI 10.1103 / PhysRevLett.110.153201 , luettu verkossa , käytetty 10. joulukuuta 2017 ).
- SB " Helium sitoutuu korkea paine natrium " Sillä tiede- , n o 474,huhtikuu 2017, s. 10.
- (in) Xiao Dong, Artem R. Oganov et ai. , " Stabiili heliumin ja natriumin yhdiste korkeassa paineessa " , Nature Chemistry ,6. helmikuuta 2017( lue verkossa )
- " Maapallolla tuntemattoman heliumin kemia voi esiintyä jättiläisplaneetoilla " , osoitteessa futura-sciences.com ,9. helmikuuta 2017(käytetty 9. helmikuuta 2017 )
- (sisään) Jurong Zhang Jian Lv, Hefei Li, Feng Xiaolei Cheng Lu et ai. , " Harvinainen heliumia sisältävä FeO 2 -yhdiste, joka stabiloitui maapallon olosuhteissa " , Physical Review Letters , voi. 121, n ° 25,21. joulukuuta 2018, s. 1-6, kohta n o 255703 ( DOI 10,1103 / PhysRevLett.121.255703 , lukea verkossa [PDF] ).
- (in) R. Mark Wilson, " helium-laakeri yhdiste syvälle maapallon löytyy laskennallisesti " , Physics Today ,10. tammikuuta 2019( DOI 10.1063 / PT.6.1.20190110a ).
- (in) " Focus: Heliumin koti maan sisällä " , Physics (in) , voi. 11,21. joulukuuta 2018, Artikkeli n: o 133 ( lue verkossa ).
- (in) J. Ackerman ja G. Maitland , " laskeminen suhteellisen äänen nopeus kaasuseoksen " , vedenalainen Biomed. Res. , voi. 2, n o 4,Joulukuu 1975, s. 305–310 ( lue verkossa ).
- (in) Joe Wolfe, " Physics puhe " , phys.unsw.edu.au. (käytetty 23. kesäkuuta 2009 ) .
- Miksi helium muuttaa ääntä? osoitteessa futura-sciences.com .
- (en) Martin Grassberger ja Astrid Krauskopf , “ Itsemurha-tukehtuminen heliumilla: Raportti kolmesta tapauksesta. Suizid mit Helium Gas: Bericht über drei Fälle. » , Wiener Klinische Wochenschrift , voi. 119, nos . 9-10,2007, s. 323-325 ( DOI 10.1007 / s00508-007-0785-4 )Yhteenveto saksaksi. Ensimmäinen sivu käytettävissä. Tuote tarjotaan myyntiin.
- (sisään) Daniel Engber, " Pysy poissa tuosta ilmapallosta! " , Slate.com,2006(käytetty 23. kesäkuuta 2009 ) .
- (vuonna) JC Eostain , C. Lemaire , MC-Gardette Chauffour , J. Doucet ja R. Naquet , " Arvio ihmisen alttiudesta korkeapaineiselle hermo-oireyhtymälle " , Journal of Applied Physiology , voi. 54, n o 4,Huhtikuu 1983, s. 1063-1070 ( lue verkossa )Saatavana henkilökohtaisella tai institutionaalisella tilauksella.
- (sisään) WL Hunger Jr. ja PB Bennett , " Korkeapainehermostosyndrooman syyt, mekanismit ja ehkäisy " , Underwater Biomedical Research , voi. 1, n o 1,1974, s. 1-28 ( ISSN 0093-5387 , OCLC 2068005 , PMID 4619860 , lue verkossa ).
- (sisään) Glenn D. Considine (toim.) Van Nostrandin Encyclopedia of Chemistry , Wylie-Interscience, ( ISBN 0-471-61525-0 ) , luku . "Helium" , s. 764–765 .
- (in) IE Beckwith ja CG Miller III , " Aerotermodynamiikka ja siirtyminen suurnopeus tuulitunnelissa NASA: n Langley'ssa " , Annual Review of Fluid Mechanics , voi. 22,1990, s. 419–439 ( DOI 10.1146 / annurev.fl.22.010190.002223 ).
- (in) CI Morris, Shock Induced Combustion in High Speed Wedge Flows , Stanford University Thesis , 2001 [ luettu verkossa (katsottu 23. kesäkuuta 2009)] .
- https://www.lemondeinformatique.fr/actualites/lire-un-disque-dur-helium-16-to-pour%C2%A0datacenter%C2%A0chez-toshiba-75335.html
- (in) James R. Belcher ja William V. Slaton, Richard Raspet Henry E. Bass, Jay Lightfoot , " Working kaasujen lämpö- moottoreissa " , The Journal of akustisen seuran Amerikan , vol. 105, n ° 5,1999, s. 2677–2684 ( DOI 10.1121 / 1.426884 )Saatavana tilauksesta.
- (in) Arjun Makhijani Kevin Gurney Paikkaaminen otsoniaukko: Tiede, teknologia ja politiikka , MIT Press , 1995 ( ISBN 0-262-13308-3 ) .
- (in) H. Jakobsson , " Simulation Dynamics Large maanpäällisten Solar teleskooppi " , Tähtitieteelliset & avaruusfysikaaliset Transactions , Voi. 13, n o 1,1997, s. 35-46 ( DOI 10,1080 / 10556799708208113 ) Tiivistelmä . Tilausartikkeli.
- (in) O. Engvold ja RB Dunn RN Smartt, WC Livingston , " Tests tyhjiö VS heliumin aurinko teleskooppi " , Applied Optics , Voi. 22,1983, s. 10–12 ( DOI 10.1364 / AO.22.000010 , lue verkossa ) Tiivistelmä . Tuote tarjotaan myyntiin.
- (in) " CERN - LHC: Facts and Figures - LHC booklet guide " ( Arkisto • Wikiwix • Archive.is • Google • Mitä tehdä ) [PDF] , CERN ( avattu 23. kesäkuuta 2009 ) .
- (in) " kryogeenitekniikka: matala lämpötila, korkea suorituskyky | CERN ” , home.cern (käytetty 7. helmikuuta 2019 ) .
- (in) B. Fowler ja KN Ackles, G. Porlier , " Effects of inertin kaasun narkoosi on käyttäytyminen-A Critical Review " , vedenalainen Biomedical Research Journal ,1985( PMID 4082343 , lue verkossa ).
- (vuonna) JR Thomas , " Rotilla tapahtuva typpinarkoosin kääntyminen heliumpaineella " , Underwater Biomed. Res. , voi. 3, n o 3,1976, s. 249–259 ( PMID 969027 , lue verkossa ).
- (fi) JC Eostain ja MC-Gardette Chauffour, C. Lemaire, R. Naquet , " Effects of a H 2 -Hän-O 2seos HPNS: ssä 450 msw: iin saakka ” , Vedenalainen Biomed. Res. , voi. 15, n ° 4,1988, s. 257-270 ( ISSN 0093-5387 , OCLC 2068005 , pMID 3212843 , lukea verkossa ).
- (in) Scott J. Butcher ja Richard L. Jones, Jonathan R. Mayne, Timothy C. Hartley, Stewart R. Petersen , " Heikentynyt liikunta hengityksen mekaniikka kanssa itsenäistä hengityslaitetta paranevat heliox " , European Journal of Applied Physiology , Alankomaat, Springer, voi. 101, n ° 6,joulukuu 2007, s. 659–669 ( DOI 10.1007 / s00421-007-0541-5 )Ensimmäinen sivu ilmainen, artikkeli rajoitettu Springer-tilaajille.
- (en) Albert Stwertka, Opas elementteihin: Tarkistettu painos , Oxford University Press , New York, 1998, ( ISBN 0-19-512708-0 ) , s. 24 .
- (in) BM Oliver ja James G. Bradley, Harry Farrar IV , " heliumpitoisuuden maapallon alailmakehän " , Geochimica ja Cosmochimica Acta , vol. 48, n o 9,1984, s. 1759–1767 ( DOI 10.1016 / 0016-7037 (84) 90030–9 ) Ilmainen tiivistelmä , artikkeli saatavilla ScienceDirect-tilauksesta.
- (in) " The Atmosphere: Introduction in JetStream - Online School for Weather " , kansallinen sääpalvelu , 29. elokuuta 2007 ( avattu 23. kesäkuuta 2009 ) .
- (en) Ø. Lie-Svendsen ja MH Rees , " Helium paeta maanpäällisestä ilmakehästä: Ionin ulosvirtausmekanismi " , Journal of Geophysical Research , voi. 101, n ° A21996, s. 2435–2444 ( DOI 10.1029 / 95JA02208 ) Tiivistelmä , artikkeli AGU-tilauksesta.
- (in) Nick Strobel, " Nick Strobel n tähtitieteen Notes veikko. Atmospheres " ,2007(käytetty 23. kesäkuuta 2009 ) .
- (in) Melvin A. Cook , " Missä on maapallon radiogeenisen heliumia? » , Nature , voi. 179,1957, s. 213 ( DOI 10.1038 / 179213a0 ) Tiivistelmä , myytävänä oleva tuote.
- (sisään) LT Aldrich ja Alfred O. Nier , " Hepr 3: n esiintyminenheliumin luonnonlähteissä ” , Phys. Ilm. , voi. 74,1948, s. 1590–1594 ( DOI 10.1103 / PhysRev.74.1590 ) Tiivistelmä , artikkeli PROLA-tilauksesta.
- (sisään) P. Morrison ja J. Pine , " Helium-isotooppien radiogeeninen alkuperä kalliossa " , Annals of New York Academy of Sciences , voi. 62, n ° 3,1955, s. 71–92 ( DOI 10.1111 / j.1749-6632.1955.tb35366.x )Ei tiivistelmää , kiitoksia, artikkeli Wiley InterSciencen tilaamisesta.
- (in) RE Zartman , " Helium Argon and Carbon in Natural Gases " , Journal of Geophysical Research , voi. 66, n o 1,1961, s. 277–306 ( DOI 10.1029 / JZ066i001p00277 , lue verkossa )AGU-tilauksella tai myynnissä.
- (in) Ronald F. Broadhead , " helium New Mexico - geologia jakelu demandand etsintä- mahdollisuuksia " , New Mexico geologian , vol. 27, n o 4,2005, s. 93–10 ( lue verkossa [PDF] ).
- (en) Hand, E (2016) Tansanian rift-alueelta löytyi massiivisia heliumikenttiä ; Science 8.7.2016: Vuosikerta 353, numero 6295 , s. 109-110 DOI : 10.1126 / tiede 353.6295.109 .
- (in) Mark Winter, " Helium: olennaiseen " , Sheffieldin yliopisto ,2008(käytetty 23. kesäkuuta 2009 ) .
- (in) The Encyclopedia of the Chemical Elements , op. cit. , s. 258 .
- (en) EM Smith ja TW Goodwin, J. Schillinger , “ Haasteita heliumin maailmanlaajuiselle saatavuudelle seuraavalla vuosikymmenellä ” , Advances in Cryogenic Engineering , voi. 49A, n o 710, 2003, s. 119–138 ( DOI 10.1063 / 1.1774674 , lue verkossa [PDF] ).
- (in) " Mineraalituotteiden yhteenvedot - helium " [PDF] , Yhdysvaltain geologinen tutkimuskeskus ,2004(käytetty 23. kesäkuuta 2009 ) .
- (en) VP Belyakov , SG Durgar'yan, BA Mirzoyan et ai. , " Kalvotekniikka - uusi suuntaus teollisessa kaasun erottamisessa " , Chemical and Petroleum Engineering , voi. 17, n o 1,yhdeksäntoista kahdeksankymmentäyksi, s. 19–21 ( DOI 10.1007 / BF01245721 )Ensimmäinen sivu ilmaiseksi, jatko SpringerLink-tilaukselle tai maksettu.
- (in) PI Dee ja ETS Walton , " A Photographic Investigation of the Transmutation of Lithium and Boor by the Protons and the litium ions by the heavy isotope of Hydrogen " , Proceedings of the Royal Society of London , voi. 141, n ° 8451933, s. 733-742 ( DOI 10.1098 / rspa.1933.0151 )Maksettu tai tilausoikeus muille kuin Royal Societyn jäsenille .
- (sisään) RK Kochhar , " ranskalaiset tähtitieteilijät Intiassa 1600--1900- luvuilla " , Journal of the British Astronomical Association , voi. 101, n ° 21991, s. 95–100 ( lue verkossa ).
- (in) The Encyclopedia of the Chemical Elements , op. cit. , s. 256 .
- (in) William Thomson, Frankland ja Lockyer löytää keltainen protuberansseja antaa erittäin kirkas linja päättänyt olla kaukana D tavoite Tähän mennessä ei ole tunnistettu minkään maanpäällisen liekki. Se näyttää osoittavan uutta ainetta, jota he ehdottavat kutsuvan heliumiksi. , Rep. Brit. Assoc. xcix , 1872.
- Cleveitiksen määritelmä .
- (sisään) The Encyclopedia of the Chemical Elements , op. cit. , s. 257 .
- (in) William Ramsay , " oli Gas Näytetään spektrissä Helium, maineikkain syy D3 Yksi Lines koronaalisiin Spectrum. Alustava huomautus ” , Proceedings of the Royal Society of London , voi. 58,1895, s. 65–67 ( DOI 10.1098 / rspl.1895.0006 )Maksettu tai tilaaminen muille kuin Royal Societyn jäsenille .
- (in) William Ramsay , " Helium, kaasumainen ainesosana tiettyjä kivennäisaineita. Osa I ” , Proceedings of the Royal Society of London , voi. 58,1895, s. 80–89 ( DOI 10.1098 / rspl.1895.0010 )Maksettu tai tilaaminen muille kuin Royal Societyn jäsenille .
- (in) William Ramsay , " Helium, kaasumainen ainesosana tiettyjä kivennäisaineita. Osa II ” , Proceedings of the Royal Society of London , voi. 59,1895, s. 325–330 ( DOI 10.1098 / rspl.1895.0097 )Maksettu tai tilaaminen muille kuin Royal Societyn jäsenille .
- (De) NA Langlet , " Das Atomgewicht des Heliums " , Zeitschrift für anorganische Chemie , voi. 10, n o 1,1895, s. 289–292 ( DOI 10.1002 / zaac.18950100130 )Myynnissä tai tilaamalla Wiley InterScience.
- (in) ER Weaver, Industrial & Engineering Chemistry , 1919, chap. " Helium-kirjallisuuden bibliografia " .
- (in) Pat Munday, American National Biography , John A. Garraty ja Mark C. Carnes (toim.), Oxford University Press , 1999 " henkilötiedot merkintä WF Hillebrand (1853-1925), geochemist ja Yhdysvaltain Bureau of Standards ylläpitäjän » , Voi. 10-11, s. 227–228 .
- (in) Dirk van Delft , " kupillinen helium, suuri tiede " , fysiikan tänään ,2008, s. 36–42 ( lue verkossa [PDF] ).
- (sisään) " Coldest Cold " , Time Inc. ,1929(käytetty 23. kesäkuuta 2009 ) .
- (in) P. Kapitza , " viskositeetti nestemäisen heliumin X alapuolella-pisteen " , Nature , voi. 141,1938, s. 74 ( DOI 10.1038 / 141074a0 ).
- (sisään) DD Osheroff ja RC Richardson, DM Lee , " Todisteet kiinteän Hep 3 : n uudesta vaiheesta " , Phys. Ilm. Lett. , voi. 28, n ° 14,1972, s. 885–888 ( DOI 10.1103 / PhysRevLett.28.885 ) Tiivistelmä . Artikkeli, jonka tekijänoikeudet omistaa PROLA.
- (in) DF McFarland , " Composition of gas from a well at Dexter, Kan " , Kansan tiedeakatemian transaktiot , voi. 19,1903, s. 60–62 ( DOI 10.2307 / 3624173 , lue verkossa )Ensimmäinen sivu. Koko artikkeli JSTOR-ehdoin.
- (in) " Heliumin löytäminen maakaasussa " , American Chemical Society ,2004(käytetty 23. kesäkuuta 2009 ) .
- (sisään) HP Cady ja DF McFarland , " Helium in Natural Gas " , Science , voi. 24,1906, s. 344 ( DOI 10.1126 / tiede.24.611.344 )Ei abstrakteja . Tuote myytävänä tai AAAS-jäsenet.
- (sisään) HP Cady ja DF McFarland , " Helium in Kansas Natural Gas " , Transaction of the Kansas Academy of Science , voi. 20,1906, s. 80–81 ( DOI 10.2307 / 3624645 , lue verkossa [ arkisto27. toukokuuta 2012] )<Ei abstrakteja . Artikkeli JSTOR-olosuhteissa.
- (in) Eugene M. Emme, (toim.) Aeronautics and Astronautics: American Chronology of Science and Technology in the Exploration of Space, 1915-1960 , NASA , Washington, DC, 1961 [ luettu verkossa (katsottu 23. kesäkuuta 2009 )] , luku. ” Ilmailun ja astronautian kronologia, 1920–1924 ” , s. 11–19 .
- (vuonna) N. Hilleret, S. Turner (toim.) CERN Accelerator School, tyhjiötekniikka: julkaisut: Scanticon Conference Center, Snekersten, Tanska, 28. toukokuuta - 3. kesäkuuta 1999 , CERN , Geneve, Sveitsi, 1999 [ lue rivi ( sivu tarkasteltu 23. kesäkuuta 2009)] , luku. " Vuototunnistus " , s. 203–212 . "Heliumivuodon havaintomenetelmän alku on löydettävä Manhattan-projektista ja uraanin erotinlaitosten ennennäkemättömistä tiivistysvaatimuksista. Tiiviyden todentamiseksi tarvittava herkkyys johti Dr. AOC Nierin suunnitteleman ja heliumin massaan kalibroidun massaspektrometrin valintaan. "
- (in) John G. Williamson , " energia Kansas " , Transactions of Kansas tiedeakatemian , Kansas Tiedeakatemia , vol. 71, n o 4,talvi 1968, s. 432–438 ( lue verkossa )Ensimmäinen sivu. Koko artikkeli JSTOR-ehdoin.
- (in) - , " Conservation Helium Sale " , Federal Register , Vuosikerta 70, n ° 193,6. lokakuuta 2005, s. 58464 ( lue verkossa [PDF] ).
- (in) " Tiivistelmä: Federal Helium Reserve -myynnin vaikutus " , nap.edu ( ISBN 978-0-309-07038-6 , käyty 23. kesäkuuta 2009 ) .
- (in) PV Mullins, RM Goodling Helium , Bureau of Mining / Minerals Yearbook 1949, 1951 [ luettu verkossa ( luettu 21. kesäkuuta 2009)] , s. 599–602 .
- (in) -tutkimus Nationin heliumivarannon myymisestä ,elokuu 2010.
- (in) GR Matos, JB Peterson, " Helium End User Statistic " , Yhdysvaltain geologinen tutkimuskeskus (tarkastettu 23. kesäkuuta 2009 ) .
- (in) Karen H. Kaplan , " Helium pula haittaa tutkimuksen ja teollisuuden " , fysiikan Tänään , American Institute of Physics , vol. 60, n ° 6,kesäkuu 2007, s. 31–32 ( DOI 10.1063 / 1.2754594 , lue verkossa ).
- (in) Sourish Basu ja Philip Yam (toim.) , " Updates: Into Thin Air " , Scientific American , Scientific American, Inc. , Voi. 297, n ° 4,lokakuu 2007, s. 18 ( lue verkossa ).
- Ludovic Pillevesse, " prefektuuri myöntää syyskuussa yksinoikeuden lupa heliumtutkimukseen Nièvressä ", Le journal du Centre ,31. elokuuta 2020( lue verkossa )
Katso myös
Bibliografia
klo. (en) Z. Cai, R. Clarke, N. Ward, WJ Nuttall, BA Glowacki, " Modeling Helium Markets " [PDF] , Cambridgen yliopisto ,2007(käytetty 22. kesäkuuta 2009 ) .
Aiheeseen liittyvät artikkelit
- Ylivirtaus
- Kryogeenia
- Jalokaasukemia
- Kalefaction tai Leidenfrost Effect
- Lihan säilöntä
- Vuototunnistus
-
Metastabiili helium

Ulkoiset linkit
- " Kamerlingh löysi nestemäisen heliumin vuonna 1908 " , BibNum (kuultu 21. kesäkuuta 2009 ) , kommentoi tekstiä.
- (en) " Heliumin tekniset tiedot " (käytetty 23. huhtikuuta 2016 ) , kunkin sivun isotoopin tiedossa olevat tiedot alasivuilla
- Auktoriteettitiedot :
- Ilmoitukset yleisissä sanakirjoissa tai tietosanakirjoissa :
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | Hei | |||||||||||||||||||||||||||||||
| 2 | Li | Olla | B | VS | EI | O | F | Syntynyt | |||||||||||||||||||||||||
| 3 | N / A | Mg | Al | Joo | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | Se | Sc | Ti | V | Kr | Mn | Fe | Co | Tai | Cu | Zn | Ga | Ge | Ässä | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Y | Zr | Huom | Mo | Tc | Ru | Rh | Pd | Ag | CD | Sisään | Sn | Sb | Sinä | Minä | Xe | |||||||||||||||
| 6 | Cs | Ba | Tämä | PR | Nd | Pm | Sm | Oli | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lukea | Hf | Sinun | W | Re | Luu | Ir | Pt | Klo | Hg | Tl | Pb | Bi | Po | Klo | Rn | ||
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Voisi | Olen | Cm | Bk | Vrt | On | Fm | Md | Ei | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| 8 | 119 | 120 | * | ||||||||||||||||||||||||||||||
| * | 121 | 122 | 123 | 124 | 125 | 126 | 127 | 128 | 129 | 130 | 131 | 132 | 133 | 134 | 135 | 136 | 137 | 138 | 139 | 140 | 141 | 142 | |||||||||||
|
alkali Metals |
Alkalinen maa |
Lantanidit |
siirtyminen metallit |
Huono metalli |
Metalli- aukot |
Ei- metallit |
halogeeni geenit |
Noble kaasujen |
Kohteet luokittelemattomat |
| Aktinidit | |||||||||
| Superaktinidit | |||||||||